持続可能性
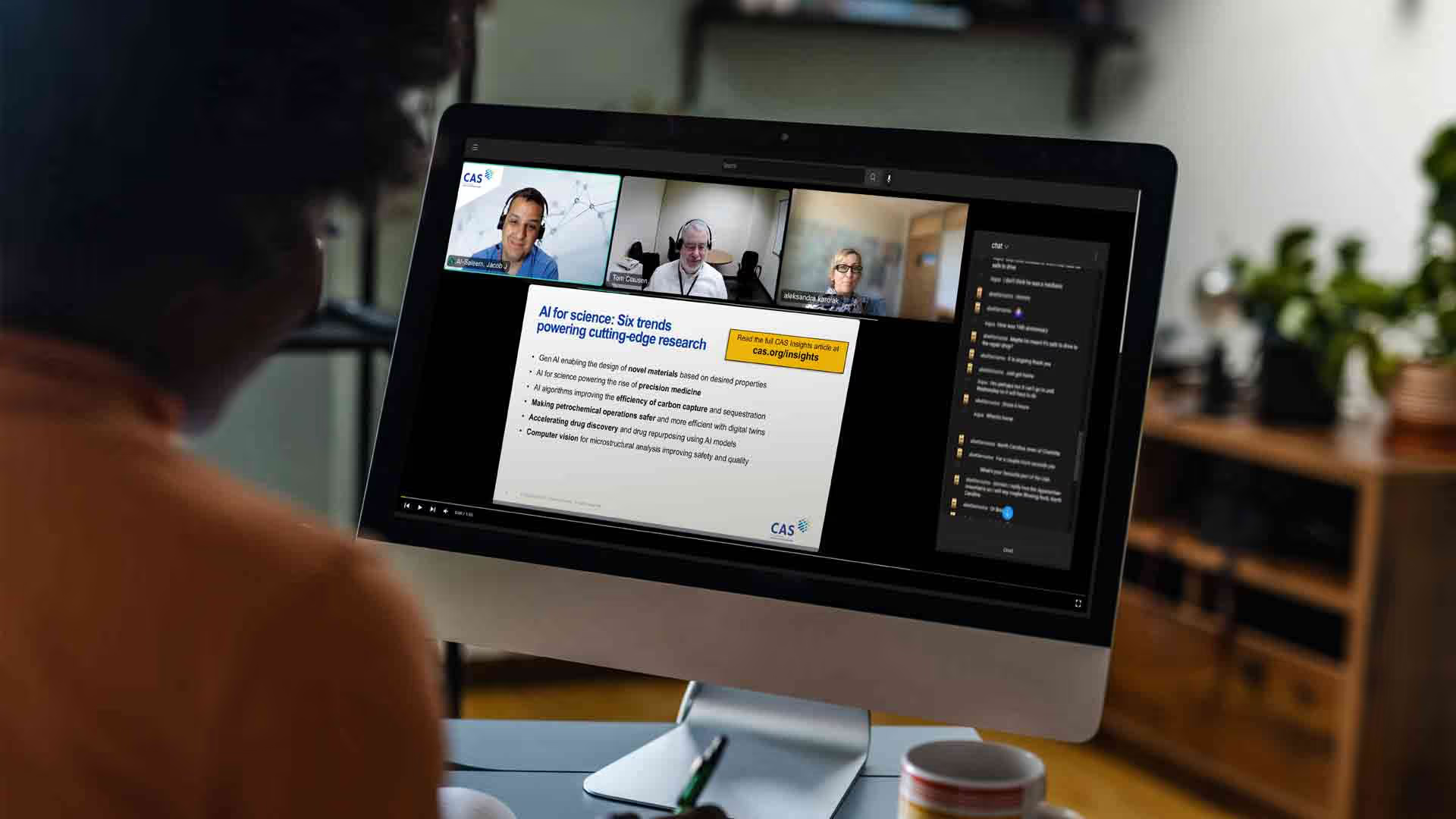
Emerging green chemistry trends explored in CAS Insights webinar
From AI-powered solutions to mechanochemistry, this CAS Insights webinar recap explores the latest green chemistry trends to watch.
Read the reportRead the articleDownload the summarySee the infographicRead the publicationRead the recapWatch the video