2020 年,新药创新势头依然强劲。 美国食品药品监督管理局(FDA)去年共批准了 53 种药物,为二十多年来第二高的批准数量,这是制药行业生产力的一个积极指标。 化学结构创新是FDA去年批准了的许多小分子药物背后的驱动力。
FDA在2020年批准的新药包括小分子、抗体、抗体-药物偶联物、多肽和寡核苷酸。 其中,具有环结构的小分子药物仍占主导地位,在批准的新药中,有31款药物为具有环结构的小分子(不包括诊断性显像剂)。 在这些小分子药物中,65%(即20款药物)的化学结构是新颖的,这意味着它们至少有一个基于新分子形状的新分子实体(NME)。 在本文中,我们将探讨一些新药及其分子形状对临床的影响。
分子形状的重要性
化学结构创新和药物取得临床与商业成功的潜力之间存在着明显的联系。 事实上,与其他小分子药物相比,化学结构新颖的药物被FDA指定为突破性疗法的可能性要高出2.5倍,成为重磅药物的可能性要高出2倍。
我们最近在《ACS Medicinal Chemistry Letters》上发表的一篇论文阐述了通过药物的化学结构来评估药物创新的价值。 因为化学结构和药理活性之间有着直接的关系,所以将药物的创新性与其分子结构联系起来是有意义的。 大多数小分子药物的作用取决于它们与蛋白质上特定位点的结合能力,这些位点是人体内自然产生的某些分子的作用位点。 例如:一种药物可能比天然分子的结合力更强,从而阻止了该分子实现其生物学功能。 因此,药物结合到所需位点的能力是其分子结构的功能。
常用来分析药物结构的概念工具之一是药物的骨架。 它被定义为分子结构的一部分,由所有的环和连接环的链段组成。 药物结构的这一部分很重要,因为它的作用是固定特定的化学基团,这些化学基团必须以特定的方式定位,以便与药物靶点的结合位点相互作用。 具有相似药理活性的药物具有相同的骨架并不罕见。 可以通过忽略某些化学细节(例如,特定类型的元素和键)来进一步简化骨架,并将其视为一个抽象形状,如下图所示。
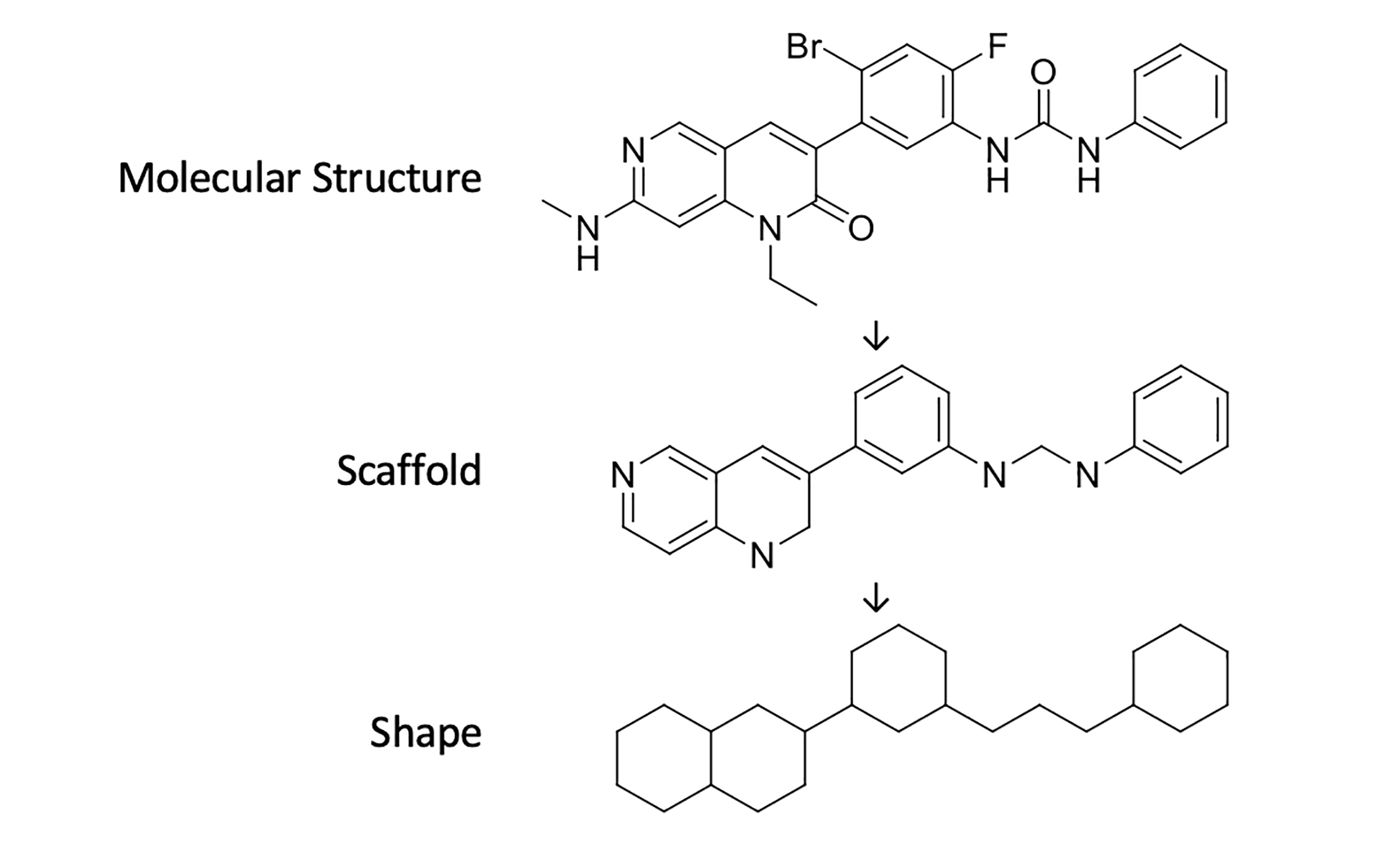
尽管分子形状简单,但它们经常被用来比较化学结构,而且可以被用来评价药物的化学结构创新。 如果一款最近被批准的药物的分子形状从未出现在任何以前被批准的药物的化学结构中,我们就认为它在结构上是新颖的。 这类药物有效地开辟了“化学空间”的新区域,因此我们称其为原创药物。
骨架和形状的概念只适用于至少有一个环的分子,大多数药物分子都满足这一条件。 FDA在2020年批准的33款小分子药物中,有31款至少有一个环。 根据我们的新分类方案,其中有20款是化学结构新颖的原创药物。
更多有关结构新颖性体现药物创新的见解,请查看《ACS Medicinal Chemistry Letters》上发表的文章(开放获取)——《Structural Approach to Assessing the Innovativeness of New Drugs Finds Accelerating Rate of Innovation》。
新的化学结构特征改善了患者的预后
化学结构创新的动机往往是希望改善直接影响患者预后的药物特性,如疗效和毒性。 这一点可以从FDA在2020年批准的三款用于治疗罕见或“孤儿”疾病的新药中看出,由于患者人数少,这些疾病往往缺乏足够的治疗选择。
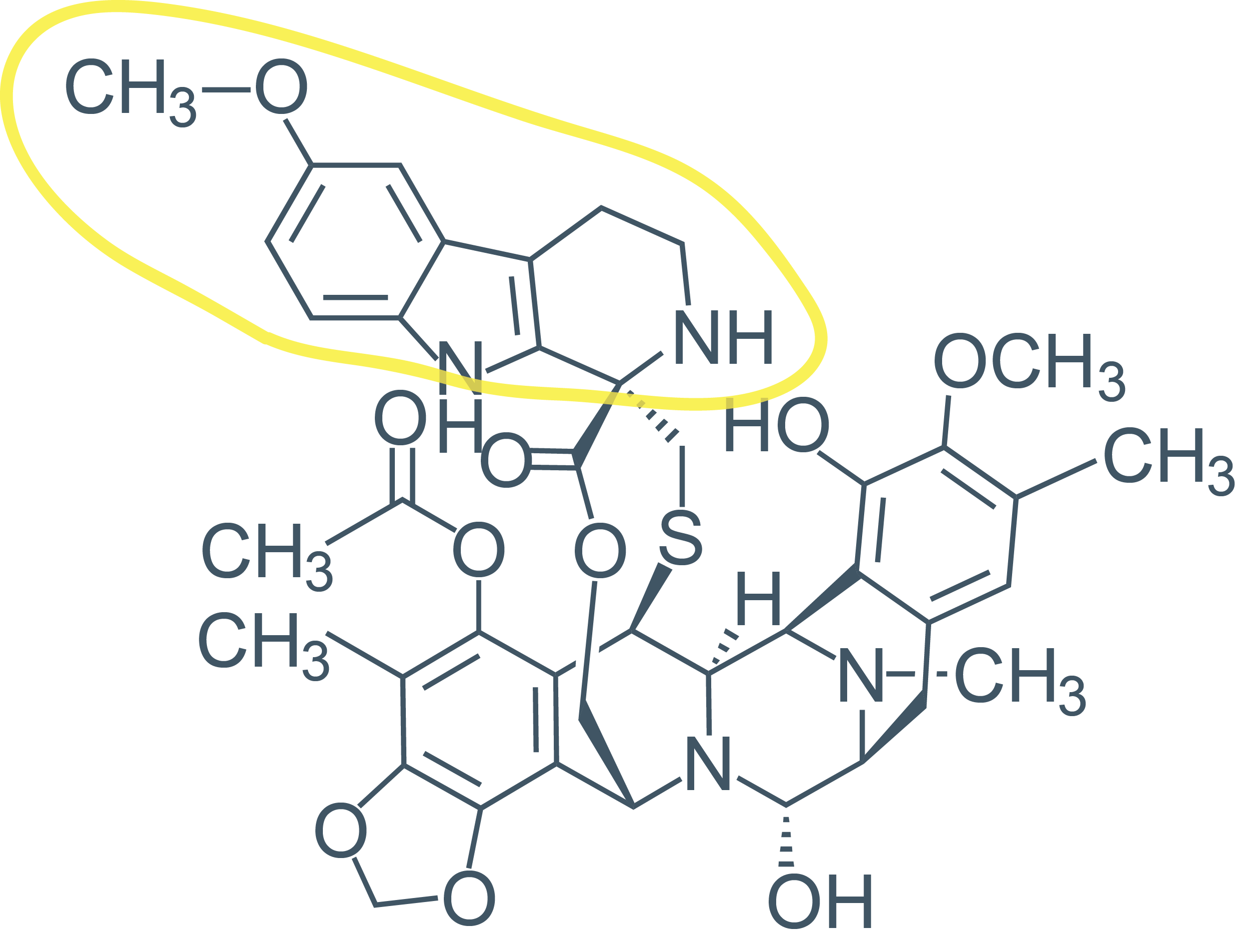
由PharmaMar开发的Zepzelca (lurbinectedin) 是一款被批准用于治疗转移性小细胞肺癌的DNA烷化剂。 Lurbinectedin的分子形状在1992年首次被报道(16年前Lurbinectedin的新药研究申请[IND]被提交给FDA),目前被报道的其他物质中有不到150个物质与Lurbinectedin具有相同的分子形状。 Lurbinectedin包含一个环系,但它是一个极其复杂的环系,由十个环组成。 图中突出显示的结构部分是一个三环系(tryptoline),为药物化学中一个众所周知的结构砌块。 Tryptoline被发现稠合在一些天然产物和药物希力士(他达拉非)的环系中。 在之前被FDA批准的药物trabectedin(FDA在2015年批准其用于治疗转移性脂肪肉瘤或平滑肌肉瘤)的化学结构中,用Tryptoline替代了四氢异喹啉环系。 Tryptoline已经被用于Lurbinectedin的化学结构设计中。这一替代创造了一种新的、没有在以前被批准的药物的化学结构中出现过的环系。 Tryptoline已经被用于Lurbinectedin的化学结构设计中。这一替代创造了一种新的、没有在以前被批准的药物的化学结构中出现过的环系。
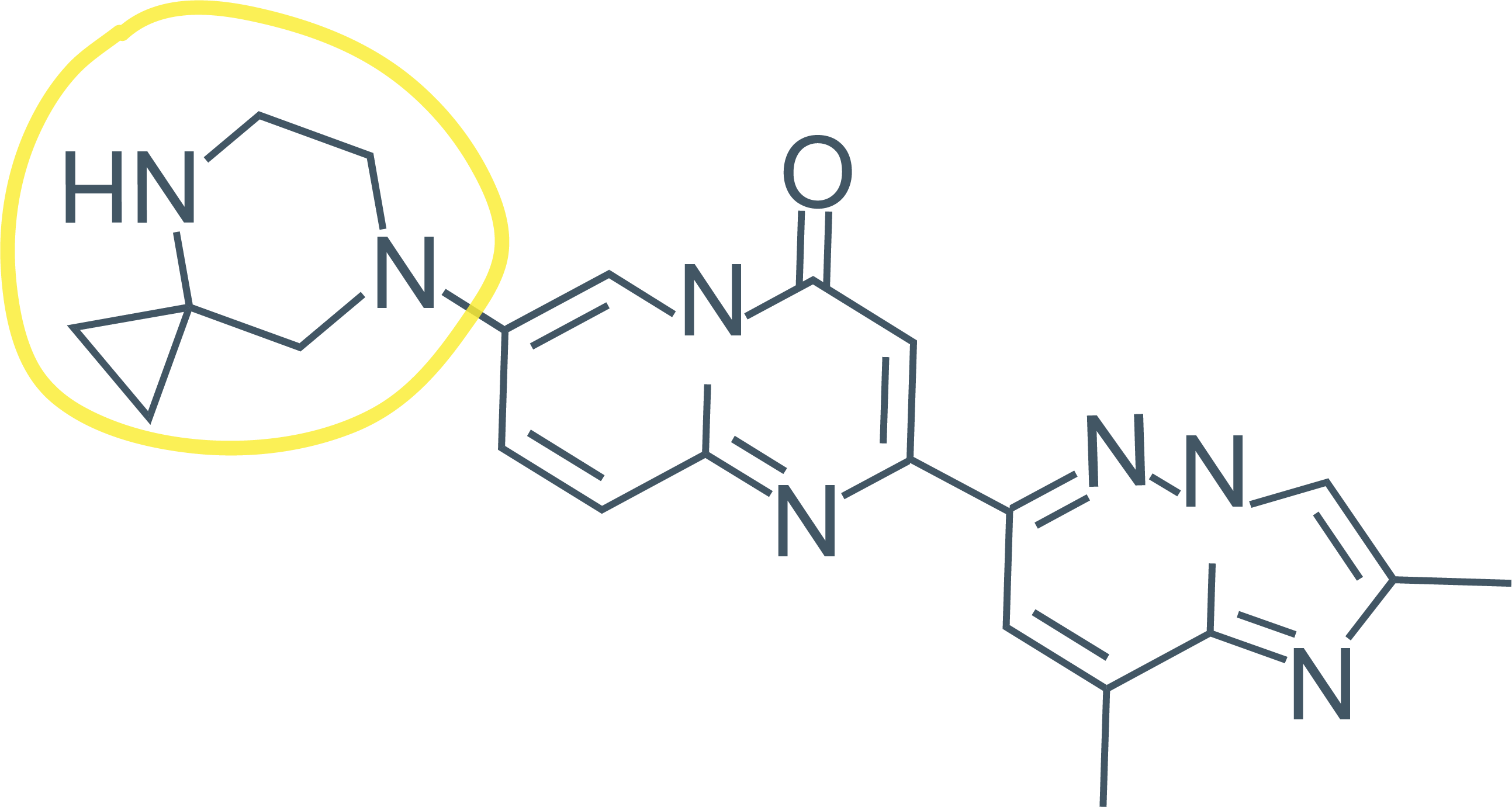
由PTC Therapeutics开发的Evrysdi (risdiplam) 是一种SMN2剪接修饰剂,被FDA批准用于脊髓性肌萎缩症的治疗。这是第一款被批准用于治疗这种罕见的致命遗传疾病的口服药物。 Risdiplam的分子形状首次被报道是在2013年(在它的IND提交给FDA的三年前),目前被报道的其他物质中只有不到50个物质具有这种分子形状。 Risdiplam的骨架由三个连接在一起的环系组成。 图中突出显示的环系(4,7-diazaspiro[2.5]octane)是一个从未在以前被批准的药物的化学结构中出现过的环系。 这个新颖的环是螺环系的一个例子,其中两个环通过一个共同的原子连接。 具体来说,它是哌嗪环和三元环的螺稠合。 虽然哌嗪的这种螺环衍生物对已批准的药物来说是新颖的,但哌嗪环本身并不是;它已被用于大量的上市药物的化学结构中。 这样的螺环系由于能够增加分子结构的非平面性,从而增强其三维性,因而在药物化学中越来越受关注。
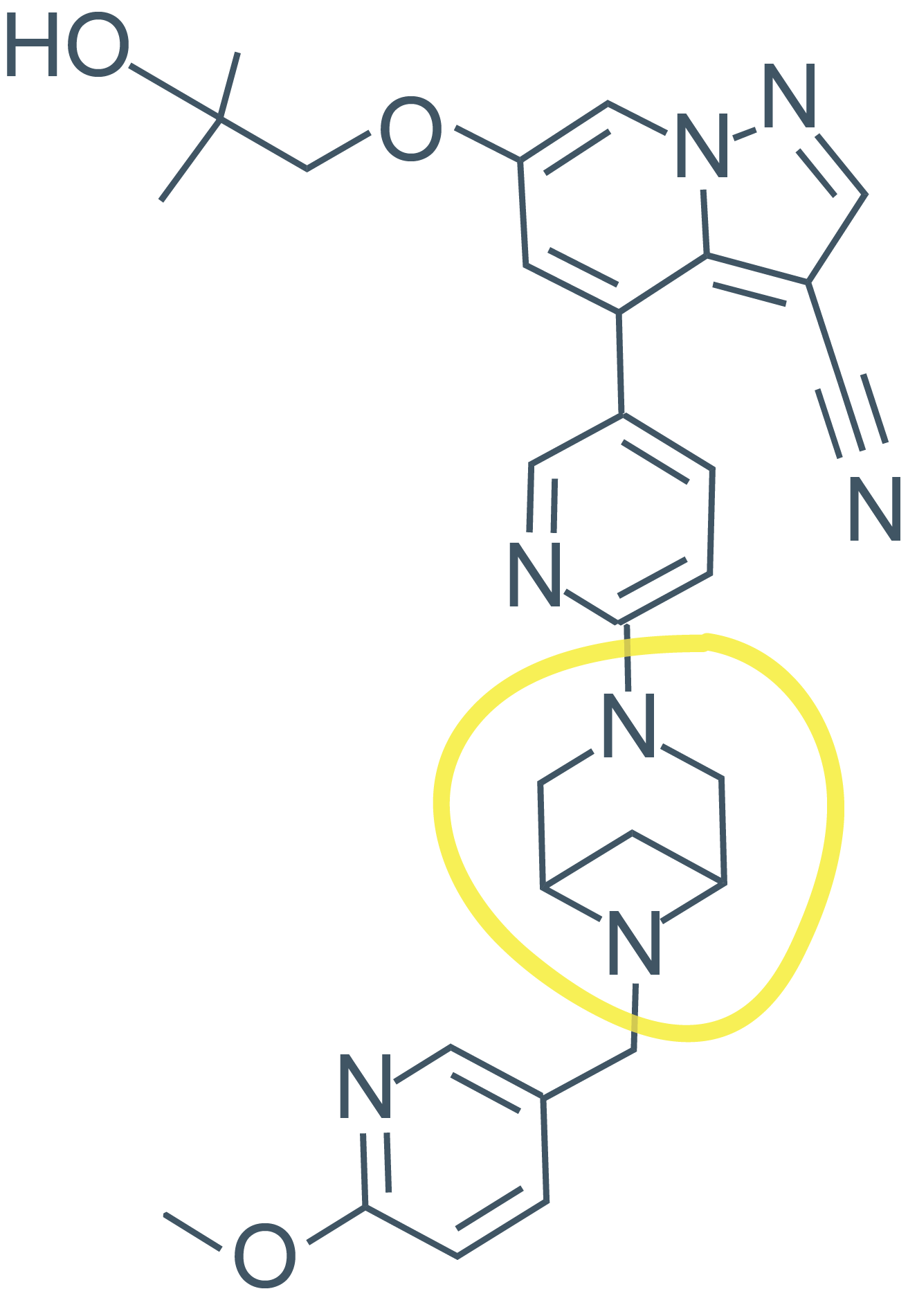
由Array BioPharma开发的Retevmo (selpercatinib) 是一款RET(转染期间重排)抑制剂,用于治疗伴有RET基因突变或融合的肺癌和甲状腺癌。 Selpercatinib是FDA批准的首款选择性RET靶向药物。 Selpercatinib的分子形状首次报道于2018年(在其IND提交给FDA一年后),目前被报道的其他物质中有不到350个物质具有这种分子形状。 Selpercatinib的骨架由四个连接在一起的环系组成。 图中突出显示的环系(3,6-二氮杂二环[3.1.1]庚烷)从未在以前被批准的药物的化学结构中出现过。 这种新颖的环(与上段文中提到的药物Evrysdi中的环一样)也是哌嗪的衍生物。 这种衍生物是通过在哌嗪环上加一个单碳桥而生成的。 最近的研究发现,将这些类型的环合并到药物的化学结构中可以降低其亲脂性(即,其对类脂环境的亲和力)。 这是影响药物活性许多方面的重要性质。 X射线晶体学发现,与2020年批准的第二款 RET 抑制剂 Pralsetinib 相比,selpercatinib的两个中心环(包括其新型桥接的哌嗪)在目标蛋白的配体结合裂缝中埋得更深。 这说明了环结构在药物与靶标的结合中所起的重要作用。
原创药物在肿瘤学领域取得了重大进展
为了进一步了解一些化学结构新颖的获批药物,我们将重点放在肿瘤的治疗领域。 2020年,FDA批准的小分子肿瘤药物有12款,比任何其他治疗领域都多。 下图展示了肿瘤药物分类:原创药物和使用现有分子形状的药物,在获批的这些药物中,原创药物的数量是非原创药物的三倍。
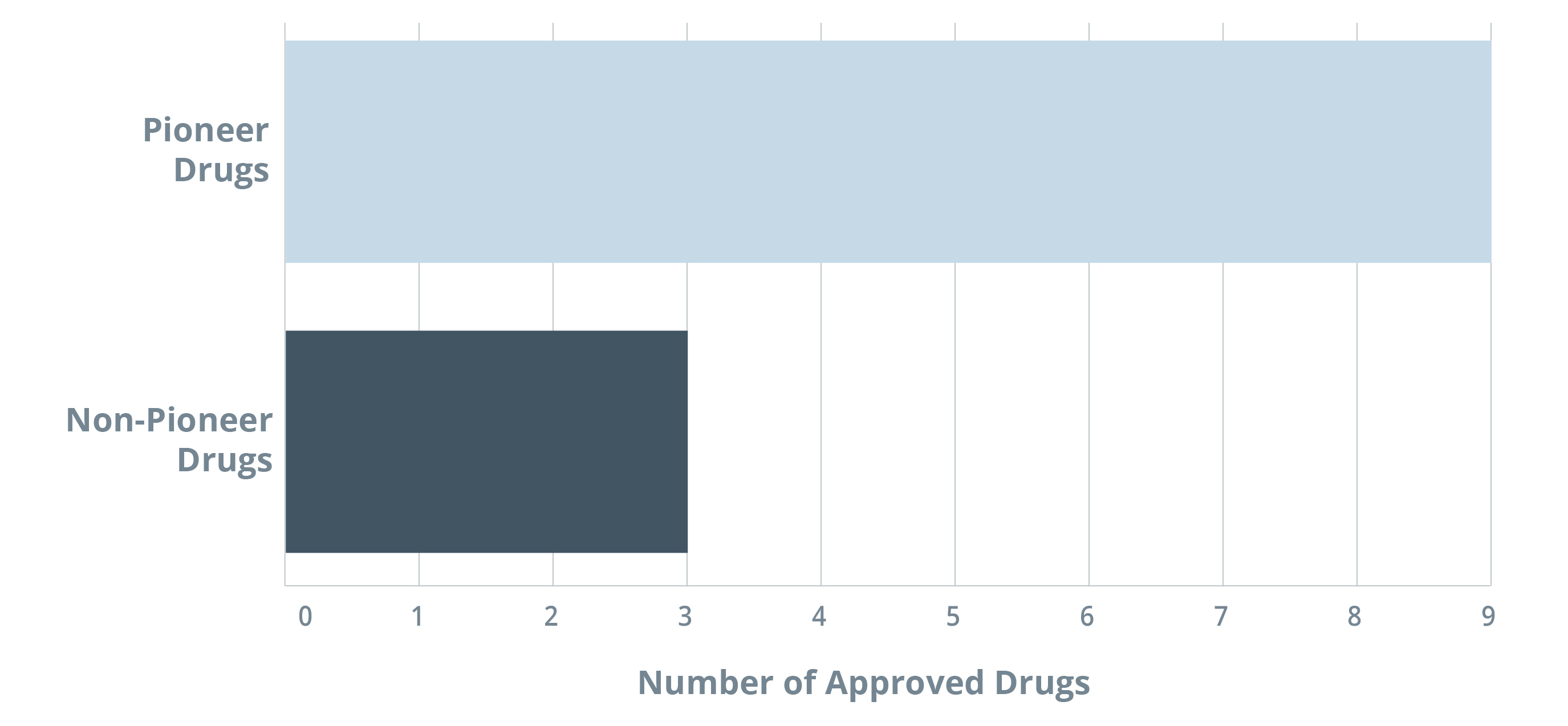
该表表明,在这些药物中,原创药物的数量是非原创药物的三倍。
FDA在2020年批准的12款具有环结构的小分子肿瘤药物中,有9款是化学结构新颖的药物。 作为这些原创药物的一个例子,图6展示了6款被FDA指定为突破性疗法的原创肿瘤新药。 仔细观察这些药物就会发现,它们代表了癌症治疗方面的一系列重要的“首创”,进一步加强了化学结构创新的临床影响。
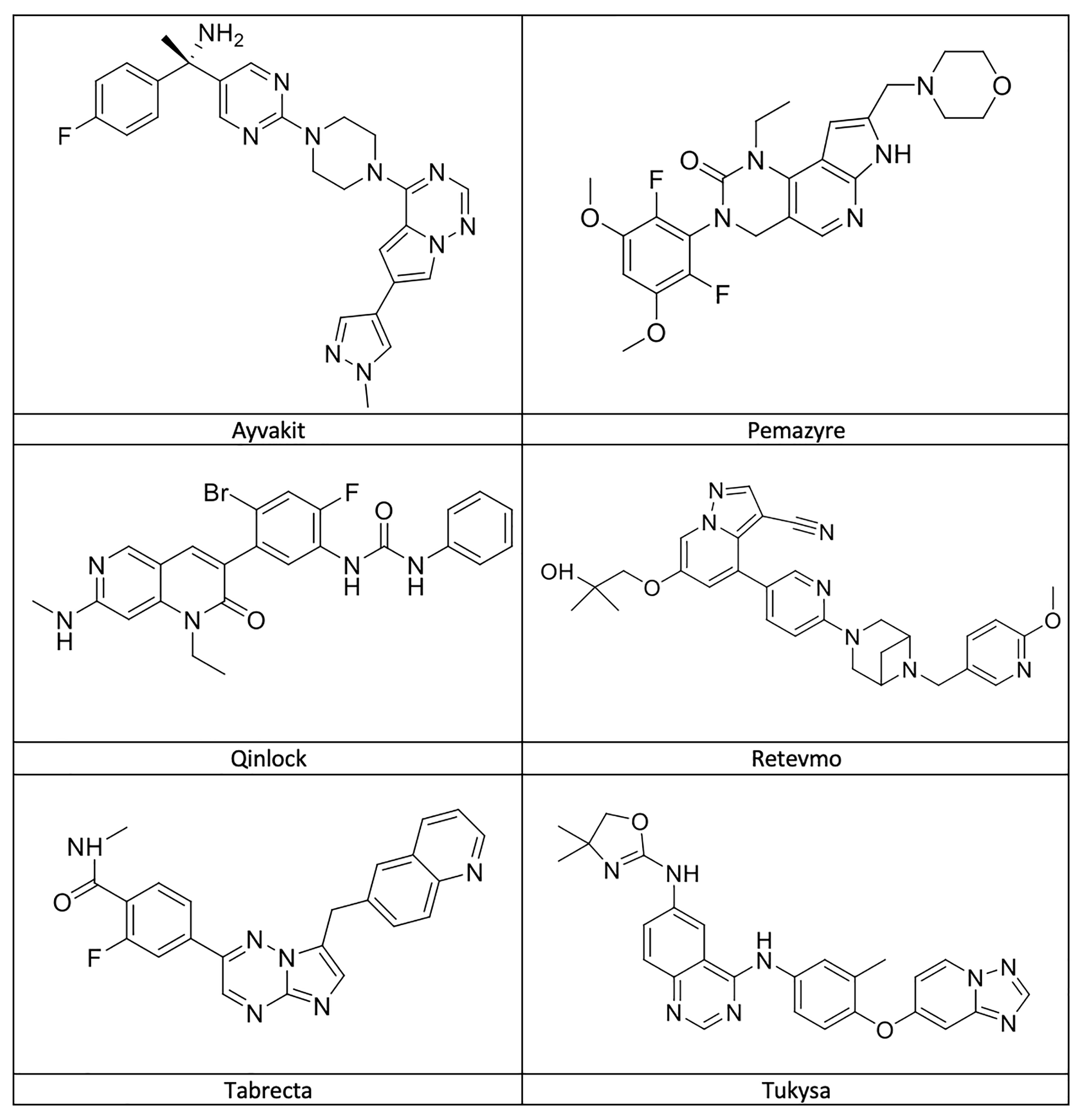
Ayvakit 是首款被FDA批准用于治疗由血小板源性生长因子受体特异性突变引起的胃肠道间质肿瘤的疗法。
Pemazyre 是首款被FDA批准用于治疗转移性胆管癌(胆管癌,这种肿瘤的成纤维细胞生长因子受体发生了突变)的药物。
Qinlock 是一款治疗晚期胃肠道间质瘤的药物,是第一款专门批准用于治疗已接受过三种或三种以上激酶抑制剂治疗的患者的药物。
Retevmo(如上所述)是首款被FDA批准用于治疗非小细胞肺癌和一些甲状腺癌的药物(肿瘤的RET基因发生了改变[突变或融合])。
Tabrecta 是首款被FDA批准用于治疗转移性非小细胞肺癌(肿瘤导致了MET[间充质上皮转化]外显子14跳跃的突变)的药物。
Tukysa 是一款被FDA批准作为联合用药方案的组成成分,用于治疗不可手术、局部晚期或转移性HER2阳性乳腺癌(包括已扩散到大脑的癌症)的药物。
推动化学结构创新能够加速药物开发
正如我们最近基于结构的药物创新分析所显示的那样,FDA在过去几十年批准的药物中,原创药物的比例呈上升趋势。 对FDA在2020年批准的药物进行分析后发现,化学结构的创新趋势可能会持续,因为药物猎人寻求改进现有药物,为目前无法治疗的疾病寻找药物,并在高价值治疗领域建立独有的知识产权。 此外,微生物对现有抗生素的耐药性或新型病毒病原体(如导致COVID-19的冠状病毒SARS-CoV-2)等新威胁的出现,继续加强了开发新疗法以减轻这些威胁的紧迫性。 问题是,我们可以做些什么来加速发现?机器学习和新兴的预测方法在未来几年对这一趋势的影响会达到什么程度呢?
请参阅我们的信息图,比较2020年批准的31种环状小分子药物的结构。

