A epigenética, o estudo das mudanças hereditárias na expressão gênica que não envolvem alterações na sequência do DNA, emergiu como um campo transformador na biologia e na medicina, revelando como a expressão gênica é modulada em resposta a estímulos internos e externos. A regulação epigenética é fundamental para a biologia do desenvolvimento, a patogênese de doenças, as interações gene-ambiente, a herança transgeracional e o desenvolvimento terapêutico. Ao elucidar como os genes são regulados dinamicamente além do genoma estático, a epigenética conecta a genética e as influências ambientais, oferecendo insights sobre os mecanismos das doenças e estratégias terapêuticas inovadoras.
Analisamos a Coleção de Conteúdo do CASTM, o maior repositório de informações científicas com curadoria humana, para descrever o progresso realizado na pesquisa epigenética e identificar os principais conceitos emergentes e desafios. Esta análise abrangente examina os fundamentos científicos, as aplicações clínicas e as inovações tecnológicas que impactam as ciências da vida e a saúde modernas.
Nossa análise constatou um crescimento acentuado e contínuo das publicações nas últimas duas décadas, com mais de 120.000 publicações relacionadas à epigenética atualmente na Coleção de Conteúdo do CAS (Ver a Figura 1). O campo é dominado por artigos de periódicos (97%), com patentes representando apenas 3% das publicações (ver a Figura 1A), indicando que a epigenética permanece na fase de descoberta e validação.
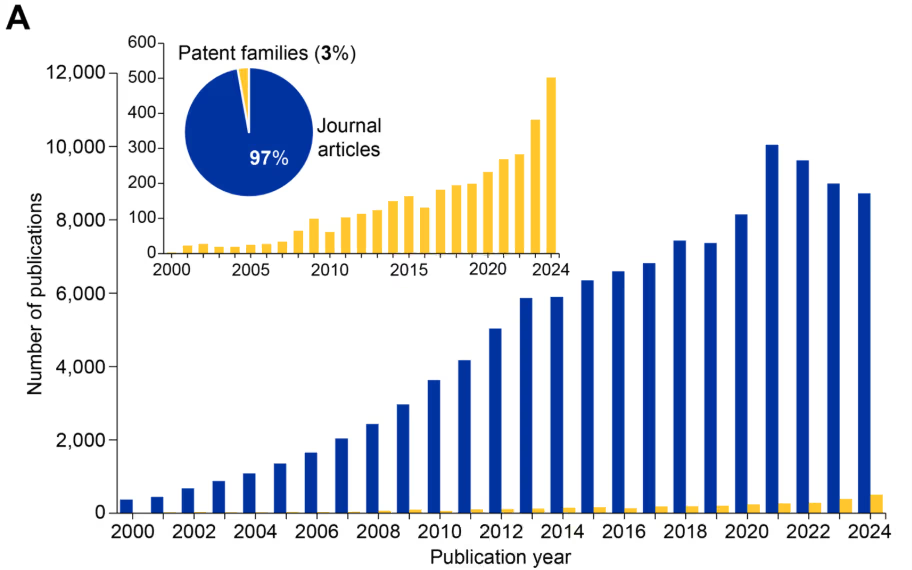


No entanto, o aumento acentuado nas publicações de patentes (veja o gráfico inserido na Figura 1A) indica um interesse comercial crescente e potencial translacional nesse campo em rápida evolução. Notavelmente, as publicações sobre epigenética superaram as publicações sobre genética desde 2014 (Figura 1B). O surgimento da epitranscriptômica como um campo distinto é notável após 2020 (Figura 1B).
Essa trajetória de crescimento está alinhada com aumentos substanciais de financiamento — o financiamento total de pesquisa cresceu de US$ 200 milhões em 2004 para mais de US$ 4,5 bilhões em 2024, apoiando aproximadamente 2.700 projetos anualmente (veja a Figura 1C). O aumento constante no número de projetos e nos níveis de financiamento, com o aumento médio de US$ 1,2 milhão para US$ 1,7 milhão, ressalta o compromisso sustentado do governo e do setor privado com o avanço da pesquisa epigenética e sua tradução clínica.
A importância comercial da epigenética expandiu-se drasticamente, com o mercado global de epigenética avaliado em US$ 1,84 bilhão em 2023 e projetado para atingir US$ 6,77 bilhões até 2033. Esse crescimento é impulsionado por mais de dez medicamentos epigenéticos aprovados pela FDA, incluindo azacitidina (Vidaza®) e vorinostat (Zolinza®), para o tratamento do câncer. Existem também mais de 35 terapias epigenéticas em ensaios clínicos. Esses candidatos têm como alvo principal diversas neoplasias malignas, mas estão começando a mostrar diversificação para além do câncer.
Vamos explorar a epigenética com mais detalhes para entender como ela está evoluindo e o que isso significa para o futuro da medicina:
Mecanismos centrais da regulação epigenética
Mecanismos epigenéticos regulam a expressão gênica por meio de modificações químicas da estrutura do DNA e da cromatina sem alterar a sequência do DNA. Esses mecanismos compreendem quatro classes principais: metilação do DNA, modificações das histonas, regulação do RNA não codificante (ncRNA) e remodelação da cromatina. Ao examinarmos publicações relacionadas à epigenética, observamos inicialmente poucas publicações abordando esses mecanismos, um resultado compreensível, já que o campo estava sendo estabelecido no início dos anos 2000 (ver Figura 2).
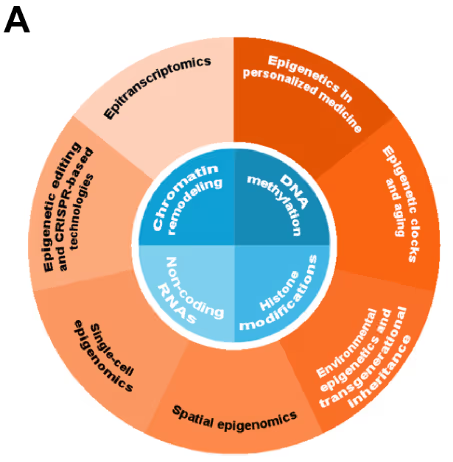

Posteriormente, os quatro mecanismos apresentaram crescimento acelerado, com a metilação do DNA registrando o aumento mais acentuado e passando a dominar o panorama de pesquisa, tanto em publicações de periódicos quanto de patentes. Todos os demais mecanismos também aumentaram, sugerindo o reconhecimento crescente de alvos epigenéticos para desenvolvimento de medicamentos.
Metilação do DNA
A metilação do DNA é um mecanismo epigenético fundamental que envolve a adição de grupos metilo (–CH₃) aos anéis de citosina nos dinucleotídeos CpG no DNA, resultando na repressão transcricional. Essa modificação desempenha um papel crucial na inativação do cromossomo X, na impressão genômica e na supressão de transposons.
A metilação do DNA é catalisada pelas DNMTs (DNA methyltransferases). A DNMT1 mantém os padrões de metilação existentes durante a replicação, enquanto a DNMT3a/3b estabelece novos padrões de metilação durante o desenvolvimento ou em resposta a estímulos ambientais. A DNMT3L, sem atividade catalítica e expressa principalmente no início do desenvolvimento, é restrita às células germinativas e ao timo na idade adulta. As DNMTs têm como alvo as ilhas CpG, regiões com alta frequência de dinucleotídeos CpG, geralmente localizadas perto dos promotores de genes.
Padrões de metilação aberrantes foram identificados em várias doenças, incluindo câncer, doenças cardiovasculares, transtornos de saúde mental, doença de Alzheimer, autismo e síndromes metabólicas. A hipermetilação dos promotores de genes supressores de tumor silencia sua expressão, promovendo a oncogênese, enquanto a hipometilação global pode ativar oncogenes e causar instabilidade genômica. Os padrões de metilação do DNA mudam com a idade, incluindo o acúmulo de erros e a perda de fidelidade na manutenção da metilação.
Modificações de histonas
As modificações de histonas podem ser herdadas por meio da divisão celular e influenciadas por fatores ambientais, potencialmente afetando o desenvolvimento e os estados de doença. As modificações pós-traducionais de histonas, como acetilação, metilação, fosforilação e ubiquitinação, alteram a estrutura da cromatina e a acessibilidade dos genes. Histonas acetiltransferases (HATs) e desacetilases (HDACs) regulam a acetilação ao catalisar a adição e remoção de grupos acetil das histonas, enquanto metiltransferases (HMTs) e desmetilases (HDMs) controlam a metilação. Essas modificações ocorrem principalmente em resíduos de lisina, arginina, serina e treonina nas caudas das histonas, que são saliências do núcleo do nucleossomo com acessibilidade aumentada.
As modificações das histonas afetam a estrutura da cromatina, que é o DNA compactado em torno de proteínas histonas que regulam a expressão gênica, o reparo do DNA e a condensação dos cromossomos durante a mitose. Modificações aberrantes de histonas podem desorganizar os padrões de expressão gênica e contribuir para o desenvolvimento tumoral e a metástase, além de estarem associadas a outras doenças e distúrbios, como Alzheimer, doença de Huntington, autismo, alterações da cromatina associadas ao envelhecimento e desregulação imunológica.
Essas alterações frequentemente formam um "código de histonas", com combinações de modificações em diferentes resíduos que atuam em sinergia ou antagonismo, ajustando com precisão os estados da cromatina. Elas constituem um sistema dinâmico e versátil para regular a estrutura da cromatina e a expressão gênica, e sua natureza reversível as torna alvos promissores para intervenções terapêuticas.
RNAs não codificantes (ncRNAs)
Os ncRNAs constituem uma classe diversa de moléculas regulatórias que desempenham papéis regulatórios críticos na expressão gênica e na dinâmica da cromatina sem codificar proteínas. Esses RNAs ajustam o processamento dos genes, direcionando o RNA mensageiro (mRNA) para degradação ou modulando a maquinaria transcricional.
Três classes surgiram como reguladores epigenéticos primários: microRNAs (miRNAs), RNAs longos não codificantes (lncRNAs) e RNAs que interagem com PIWI (piRNAs). Esses ncRNAs orquestram a regulação epigenética por meio de cinco mecanismos principais:
- Remodelagem da cromatina: os lncRNAs recrutam complexos modificadores da cromatina para locais genômicos específicos, influenciando a estrutura da cromatina e a expressão gênica. Por exemplo, o transcrito específico do X inativo (XIST) medeia a inativação do cromossomo X ao recrutar o complexo repressivo Polycomb 2 (PRC2).
- Regulação transcricional: miRNAs e lncRNAs modulam a transcrição interagindo com fatores de transcrição ou RNA polimerases. Por exemplo, o lncRNA HOX transcript antisense intergenic RNA (HOTAIR) recruta PRC2 para reprimir genes em um cromossomo diferente.
- Controle pós-transcricional: os miRNAs se ligam às regiões 3′ não traduzidas (UTRs) dos RNAs mensageiros (mRNAs) alvo, levando à degradação ou à inibição da tradução. lncRNAs podem atuar como esponjas moleculares para sequestrar miRNAs, o que os impede de direcionar mRNAs.
- Modificação de RNA: Alguns ncRNAs orientam a metilação do RNA (por exemplo, N6-metiladenosina, m6A) ou a edição, afetando a estabilidade e a tradução do RNA.
- Defesa do genoma: os piRNAs e siRNAs suprimem elementos transponíveis, protegendo a integridade genômica. Os siRNAs podem direcionar a formação de heterocromatina em regiões com sequências repetitivas.
Remodelação da cromatina
A remodelação da cromatina modifica dinamicamente a arquitetura da cromatina entre os estados de eucromatina (aberta, transcricionalmente ativa) e heterocromatina (condensada, transcricionalmente silenciosa). A unidade básica da cromatina é o nucleossomo, composto de DNA enrolado em torno de um octâmero de proteínas histonas. O remodelamento da cromatina é realizado por complexos dependentes de ATP, como as famílias switch/sucrose nonfermentable (SWI/SNF), imitation switch (ISWI), proteínas de ligação ao chromodomain helicase DNA (CHD) e INO80, que utilizam a hidrólise de ATP para promover o reposicionamento, a ejeção ou a reestruturação dos nucleossomos.
Os mecanismos de remodelação incluem o deslizamento de nucleossomos, a remoção/troca de histonas e a compactação/descompactação da cromatina. Esses processos atuam em conjunto com a metilação do DNA e as modificações de histonas para regular a expressão gênica, a diferenciação celular e a manutenção da identidade celular.
A desregulação da remodelação da cromatina está associada ao câncer, distúrbios neurológicos e doenças do desenvolvimento. Por exemplo, mutações em remodeladores de cromatina como o domínio de interação rico em AT 1A (ARID1A) (um componente do complexo SWI/SNF) são frequentemente observadas em malignidades. Os remodeladores de cromatina representam alvos terapêuticos promissores para reverter a expressão gênica aberrante. Assim sendo, a remodelação da cromatina é reconhecida como um mediador das influências ambientais (dieta, estresse, toxinas, etc.) na expressão gênica e na saúde.
Avanços recentes em epigenética
Avanços recentes mostraram como modificações epigenéticas, incluindo metilação do DNA, modificações de histonas, regulação de ncRNA e remodelação da cromatina, contribuem para a patogênese da doença, especialmente no câncer. Pesquisas emergentes sobre miRNAs e outros ncRNAs como reguladores epigenéticos identificaram novos alvos terapêuticos, enquanto avanços no perfilamento epigenético individual estão auxiliando o desenvolvimento de abordagens de medicina personalizada. As tendências de publicação mostram as principais áreas de interesse (ver Figura 3).

Epigenética ambiental
Fatores ambientais, como dieta, estresse, toxinas e estilo de vida, podem induzir alterações epigenéticas por meio dos vários mecanismos discutidos anteriormente. Essas modificações podem contribuir para o desenvolvimento de doenças como câncer, distúrbios metabólicos e condições neurológicas, alterando a função celular e a homeostase tecidual. As influências específicas incluem:
- A disponibilidade de nutrientes (por exemplo, folato, vitamina B12) afeta os padrões de metilação do DNA.
- Exposições químicas (como o bisfenol A, pesticidas e poluentes atmosféricos) alteram as marcas epigenéticas, podendo levar a consequências para a saúde a longo prazo.
- O estresse psicológico e fisiológico induz alterações epigenéticas em genes de resposta ao estresse e modula a saúde mental.
- Fatores de estilo de vida (ex.: tabagismo, consumo de álcool, níveis de atividade física) que influenciam o risco de doenças através da modulação de estados epigenéticos.
Epitranscriptômica
A epitranscriptômica concentra-se no estudo das modificações químicas nas moléculas de RNA e seu papel na regulação da expressão gênica e das funções celulares. Assim como a epigenética explora modificações no DNA e nas histonas que influenciam a atividade gênica sem alterar a sequência subjacente do DNA, a epitranscriptômica investiga como modificações no RNA afetam a estabilidade do RNA, a tradução, o splicing e outros processos.
Mais de 170 modificações distintas de RNA em mRNA, tRNA, rRNA e ncRNAs já foram identificadas, sendo a N6-metiladenosina (m6A) a modificação mais abundante e mais amplamente estudada no mRNA eucariótico. As principais modificações incluem: metilação m6A na posição N6 da adenosina, que influencia a estabilidade, o splicing, a exportação e a tradução do mRNA; metilação m5C na posição N5 da citosina em mRNA e tRNA, afetando a estabilidade do RNA e a tradução; pseudouridina (Ψ), um isômero da uridina, que aumenta a estabilidade do RNA e a eficiência de tradução; e a desaminação de adenosina em inosina, que altera as propriedades de pareamento de bases e afeta o splicing e a codificação proteica.
O mecanismo epitranscriptômico compreende três classes principais de proteínas:
- "Escritores": enzimas que adicionam modificações (ex.: complexo METTL3/METTL14 para metilação m6A).
- "Apagadores": enzimas que removem modificações (por exemplo, proteína associada à massa gorda e à obesidade (FTO) e alkB homolog 5, RNA desmetilase (ALKBH5) para desmetilação de m6A).
- "Leitores": proteínas que reconhecem e se ligam ao RNA modificado (por exemplo, proteínas de domínio YTH para reconhecimento de m6A), que regulam coletivamente a dinâmica de modificação do RNA.
As modificações do RNA regulam múltiplos processos celulares, e a desregulação dessas modificações contribui para diversas patologias. No câncer, as modificações m6A são frequentemente alteradas em tumores e associadas à progressão tumoral, metástase e resistência a medicamentos. A edição e as modificações aberrantes do RNA estão associadas a doenças neurodegenerativas, incluindo Alzheimer, Parkinson e ELA (Esclerose Lateral Amiotrófica). Além disso, vírus de RNA, incluindo HIV e SARS-CoV-2, exploram a maquinaria de modificação de RNA do hospedeiro para regular a replicação viral e a evasão imune, incluindo modificações epigenéticas.
Tecnologias de sequenciamento de alto rendimento permitem o mapeamento genômico de modificações de RNA, complementado por espectrometria de massa e técnicas de marcação química para detecção e quantificação de modificações. Esses avanços facilitam o desenvolvimento de terapias direcionadas a enzimas de modificação do RNA.
O direcionamento de componentes da maquinaria de modificação de RNA (escritores, apagadores e leitores) está sendo explorado como uma estratégia para o tratamento de doenças. Por exemplo, os inibidores de FTO, que são desmetilases m6A, mostraram-se promissores na terapia do câncer, enquanto os nucleotídeos modificados nas vacinas de mRNA aumentam a estabilidade e a eficiência da tradução.
De forma geral, a pesquisa atual se concentra em decifrar o "código do epitranscriptoma", desenvolver ferramentas para a manipulação precisa in vivo de modificações de RNA e explorar modificações em ncRNAs. A epitranscriptômica de célula única está revelando padrões de modificação de RNA específicos de cada tipo celular e suas consequências funcionais. Uma tecnologia emergente, a integração multi-ômica, combina dados epigenômicos com transcriptômica, proteômica e metabolômica usando tecnologias como CUT&RUN e integração Hi-C, fornecendo visões holísticas da função celular. Essas abordagens permitem uma análise abrangente de vias metabólicas e a descoberta de biomarcadores em doenças complexas.
Herança transgeracional
A herança transgeracional refere-se à transmissão de alterações epigenéticas induzidas pelo ambiente ao longo de múltiplas gerações, independentemente de alterações na sequência do DNA. Esse fenômeno foi observado em plantas e animais, sugerindo que exposições ambientais vivenciadas por uma geração podem afetar a saúde e o desenvolvimento das gerações subsequentes. No entanto, verificar a extensão e a importância desse processo em seres humanos é um desafio.
Exemplos de herança epigenética transgeracional incluem o Inverno da Fome Holandês (1944-1945), onde padrões alterados de metilação do DNA e aumento dos riscos metabólicos foram observados em gerações subsequentes de indivíduos que foram expostos à fome na Holanda. Estudos em animais também forneceram exemplos de efeitos transgeracionais de desreguladores endócrinos (por exemplo, vinclozolina) sobre a reprodução, o comportamento e a suscetibilidade a doenças, enquanto, em humanos, o tabagismo paterno e o estresse materno foram associados a alterações epigenéticas na prole.
Embora os mecanismos subjacentes à herança epigenética transgeracional não sejam totalmente compreendidos, seu efeito em elevar o perfil de risco para doenças como obesidade, diabetes e distúrbios cardiovasculares em descendentes de indivíduos expostos faz com que essa continue sendo uma área de pesquisa ativa. A compreensão dos efeitos transgeracionais também pode orientar políticas para reduzir a exposição a fatores ambientais nocivos, particularmente durante períodos críticos do desenvolvimento (por exemplo, a gravidez).
Edição epigenética e tecnologias baseadas em CRISPR
O advento da tecnologia CRISPR-Cas9 revolucionou a engenharia genética, e sua aplicação à epigenética não é exceção. A edição epigenética envolve a modificação direcionada de marcas epigenéticas sem alterar a sequência de DNA, oferecendo uma ferramenta poderosa para o estudo da regulação gênica e o desenvolvimento de novas terapias.
O sistema CRISPR-Cas9 emprega RNAs guia (gRNAs) para direcionar a Cas9 cataliticamente inativa (dCas9), fundida a domínios efetores epigenéticos, a lócus genômicos específicos. Os principais domínios efetores incluem DNMT (por exemplo, DNMT3A), desmetilases de DNA (por exemplo, TET1), modificadores de histonas (por exemplo, p300, HDACs) e remodeladores de cromatina, permitindo a adição ou remoção precisa de modificações epigenéticas.
A tecnologia CRISPR-Cas9 permite a ativação ou repressão seletiva da expressão gênica ao direcionar elementos regulatórios, incluindo potenciadores e promotores, possibilitando que pesquisadores testem diretamente os papéis causais de marcas epigenéticas específicas na regulação gênica, na diferenciação celular e nas doenças. Além disso, permite o exame da herança epigenética ao longo das divisões celulares, do desenvolvimento e a geração de modelos de doenças impulsionadas pela desregulação epigenética.
As aplicações terapêuticas incluem silenciar genes causadores de doenças (oncogenes, genes virais) e reativar genes silenciados benéficos (supressores tumorais) em câncer e hipercolesterolemia, entre outros. Essa abordagem oferece o potencial de terapias altamente personalizadas com efeitos colaterais mínimos e aplicações na reprogramação celular para medicina regenerativa. As principais vantagens da edição do epigenoma baseada em CRISPR incluem alta precisão de direcionamento, versatilidade por meio de domínios efetores intercambiáveis e risco mutagênico reduzido em comparação com a edição genética.
O avanço dessa tecnologia exige o desenvolvimento de variantes de Cas de alta fidelidade e projetos otimizados de gRNA para minimizar os efeitos fora do alvo. Além disso, o direcionamento multiplexado permitirá a investigação de redes regulatórias complexas, enquanto métodos de entrega aprimorados (vetores virais, nanopartículas) facilitarão a tradução clínica. As tecnologias emergentes nesse espaço incluem ferramentas de edição de epigenoma, especialmente sistemas baseados em CRISPR/dCas9 fundidos com efetores epigenéticos (DNMTs, TETs, HDACs). Plataformas alternativas incluem TALE549 e proteínas de dedo de zinco para direcionamento específico de lócus.
Epigenômica de célula única
As tecnologias epigenômicas de célula única permitem a análise de modificações epigenéticas com resolução em nível de células individuais. Isso fornece insights sem precedentes sobre diversidade e função celular e supera as desvantagens dos métodos tradicionais de sequenciamento em massa, que analisam marcas epigenéticas médias em milhões de células.
Técnicas como ATAC-seq de célula única (ensaio para cromatina acessível à transposase usando sequenciamento) e ChIP-seq de célula única (sequenciamento por imunoprecipitação de cromatina) para perfilar a acessibilidade da cromatina e as modificações de histonas em células individuais estão na vanguarda dessa tendência. As aplicações incluem o mapeamento de cenários epigenéticos durante a embriogênese, a diferenciação celular e tecidual, as decisões sobre o destino das células e a heterogeneidade do sistema imunológico.
Em pesquisa sobre câncer, a epigenômica de célula única pode revelar heterogeneidade epigenética intratumoral relevante para evolução clonal, resistência a medicamentos e metástase. A tecnologia também é usada para elucidar alterações epigenéticas em neurodesenvolvimento, neurodegeneração e diferenciação de células imunes, contribuindo para nossa compreensão de doenças autoimunes e respostas à imunoterapia.
Epigenômica espacial
A epigenômica espacial é uma tecnologia de ponta que combina o estudo das modificações epigenéticas com o contexto espacial dentro dos tecidos. Essa abordagem faz a ponte entre epigenômica de células únicas e histologia, revelando como a regulação epigenética varia entre regiões teciduais e influencia a organização, função e comunicação celular na saúde e doença.
As aplicações incluem o mapeamento do padrão tecidual durante a organogênese, guiado por alterações epigenéticas; a identificação de assinaturas epigenéticas espacialmente distintas em tumores (núcleo versus margens invasivas), que podem impulsionar metástase ou resistência a fármacos; a caracterização de alterações epigenéticas específicas de regiões em tecidos ou tipos celulares do cérebro, fornecendo insights sobre neurodesenvolvimento, plasticidade e doenças neurodegenerativas; a compreensão da regulação epigenética em diferentes nichos de células imunes; e a influência dos estados epigenéticos no microambiente tecidual.
Epigenética na saúde e na doença
Modificações epigenéticas orientam o desenvolvimento embrionário e decisões de destino celular ao ativar ou silenciar conjuntos específicos de genes. A desregulação desses processos impacta numerosas patologias e, embora o câncer tenha sido a principal área de doença sob investigação, o papel da epigenética em outras condições está sendo explorado.
Câncer
As mutações genéticas há muito são reconhecidas como impulsionadoras do câncer, e alterações epigenéticas agora são entendidas como tendo um papel igualmente crítico na tumorigênese. O cenário de pesquisa revela o domínio do câncer, com 47% das publicações, refletindo tanto a maturidade da área quanto o sucesso da translação clínica (Ver Figura 4).
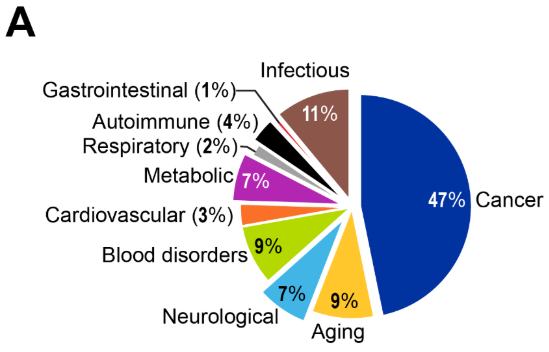

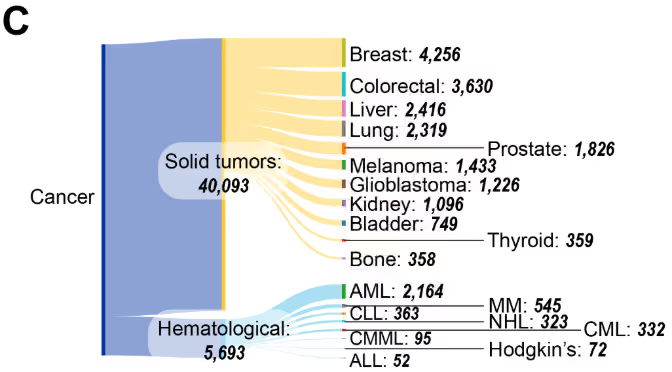
Os tumores sólidos representam a esmagadora maioria das publicações (Figura 4C), com câncer de mama, colorretal, fígado e pulmão liderando em termos de atividade de pesquisa. Entre as malignidades hematológicas, a leucemia mieloide aguda (LMA) domina, seguida pela leucemia linfocítica crônica (LLC) e mieloma múltiplo (MM). Essa distribuição, baseada em dados de publicação da CAS coleção de conteúdo, está alinhada com as terapias epigenéticas aprovadas pela FDA dos EUA para o tratamento dessas neoplasias, incluindo azacitidina e decitabina, usadas para o tratamento de LMA, e vorinostat , para linfoma cutâneo de células T.
A regulação epigenética no câncer envolve três mecanismos principais:
- Metilação do DNA: A hipermetilação das regiões promotoras frequentemente leva ao silenciamento de genes supressores de tumor, enquanto a hipometilação global pode ativar oncogenes e promover instabilidade genômica.
- Modificações de histonas: As alterações na acetilação, metilação e fosforilação de histonas podem mudar a estrutura da cromatina e a expressão gênica.
- ncRNAs: A desregulação dos miRNAs (por exemplo, superexpressão de miR-21) pode promover a progressão do câncer ao direcionar supressores tumorais ou oncogenes.
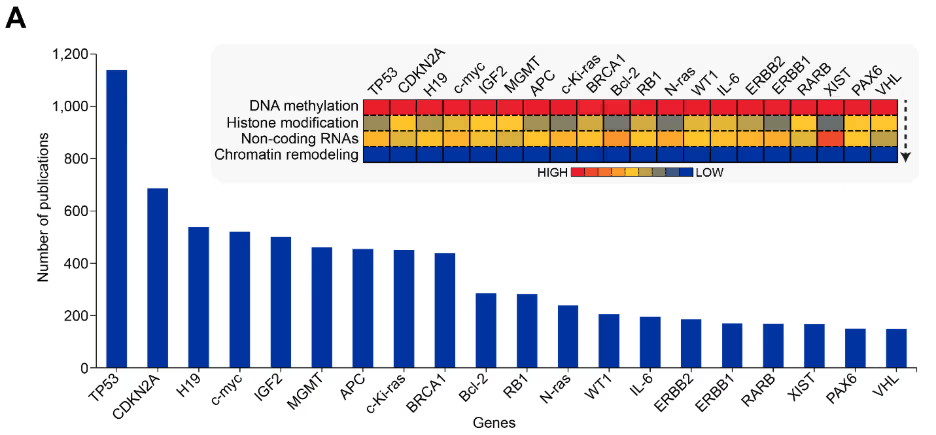
O mapa de calor da coocorrência de mecanismos gene-epigenéticos mostrado na Figura 5 revela padrões distintos. Por exemplo, a predominância da metilação do DNA reflete seu papel como um importante mecanismo epigenético. O remodelamento da cromatina apresenta mínima coocorrência na maioria dos genes, sugerindo seu papel em mudanças arquiteturais mais amplas, em vez de uma regulação específica de genes. As publicações relacionadas com ncRNA e modificações de histonas situam-se entre os dois extremos, metilação do DNA e remodelação da cromatina.
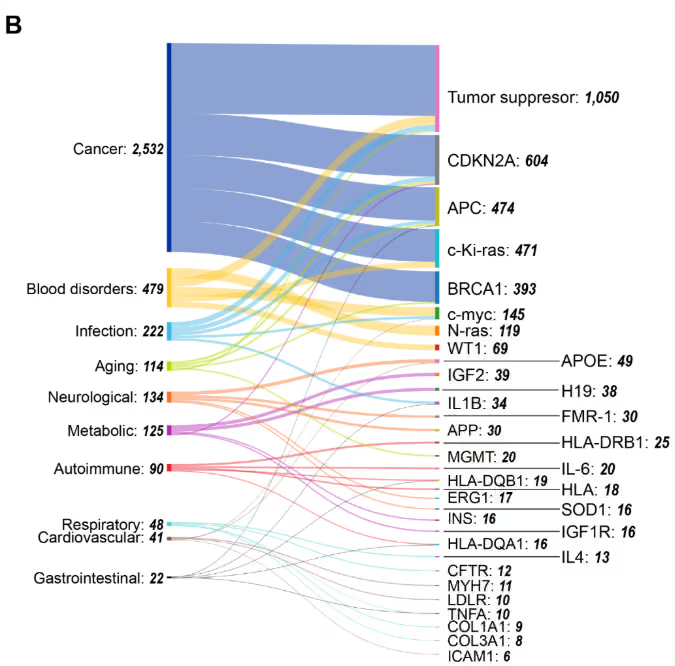
Nossa análise de coocorrências de genes e doenças (Figura 5B) ilustra a posição central do câncer, com os genes supressores de tumor apresentando a maior conectividade. Outros genes com alta coocorrência em vários tipos de câncer incluem CDKN2A, seguido por APC e c-Ki-ras (KRAS325). Esse padrão reflete o papel desses genes como centros epigenéticos sujeitos ao silenciamento mediado por metilação em diversas neoplasias malignas.
Relógios epigenéticos e condições relacionadas ao envelhecimento
Os relógios epigenéticos são um conceito inovador que utiliza modelos computacionais para prever a idade biológica com base em padrões de metilação do DNA. Podem revelar discrepâncias entre a idade biológica e a idade cronológica de um indivíduo, fornecendo insights sobre o processo de envelhecimento e o impacto do estilo de vida e dos fatores ambientais. Esses modelos exploram alterações previsíveis na metilação do DNA relacionadas à idade, onde regiões genômicas específicas tornam-se hipermetiladas ou hipometiladas em padrões reproduzíveis.
O relógio epigenético de primeira geração, o relógio de Horvath, foi desenvolvido por Steve Horvath em 2013 e utiliza dados de metilação do DNA de 353 sítios CpG em múltiplos tecidos e tipos de células para estimar a idade biológica. O relógio de Hannum, desenvolvido no mesmo ano, utiliza 71 sítios CpG, principalmente no sangue. Relógios circadianos mais recentes, como o GrimAge e o PhenoAge, incorporam biomarcadores adicionais (por exemplo, proteínas plasmáticas) para melhorar a precisão e prever a mortalidade e o risco de doenças.
Em pesquisas sobre longevidade, centenários e indivíduos com longevidade excepcional frequentemente exibem um envelhecimento epigenético mais lento, fornecendo pistas sobre os fatores genéticos e ambientais que promovem um envelhecimento saudável. A pesquisa atual explora a reversibilidade por meio de senolíticos e compostos que têm como alvo os reguladores epigenéticos.
As tendências de publicações de pesquisa vistas na Figura 4A demonstram que o envelhecimento representa 9% das pesquisas em epigenética que mencionam explicitamente doença e envelhecimento, um percentual significativamente menor do que o da pesquisa sobre câncer (47%), mas que apresenta crescimento consistente de 2010 a 2024, especialmente perceptível após 2019 (Figura 4B). Essa proporção reflete o papel especializado, porém crescente, da pesquisa sobre envelhecimento dentro do cenário epigenético mais amplo, dominado por aplicações no câncer.
Doenças neurodegenerativas
Modificações epigenéticas foram associadas a doenças neurodegenerativas como Alzheimer, Parkinson e ELA, assim como a transtornos mentais como depressão e esquizofrenia (Figura 6). A produção substancial de pesquisas reflete o crescente reconhecimento dos mecanismos epigenéticos em patologias neuropsiquiátricas e neurodegenerativas (ver Figura 4A).
Alterações epigenéticas afetam genes envolvidos na produção de amiloide-beta (Aβ) e na fosforilação de tau na doença de Alzheimer, com a desregulação de miRNAs como miR-29352 e miR-34354 sendo associada ao declínio cognitivo. A doença de Parkinson apresenta alterações epigenéticas em genes da função mitocondrial (por exemplo, PINK1355) e nas vias de agregação da α-sinucleína. Os padrões de acetilação de histonas e metilação do DNA são alterados em modelos da doença de Parkinson, afetando a sobrevivência neuronal.
Os transtornos do espectro autista apresentam desregulação de genes sinápticos (por exemplo, SHANK3360) por meio de metilação aberrante do DNA e modificações de histonas, sendo que fatores ambientais, como a exposição pré-natal ao ácido valproico, demonstraram induzir alterações epigenéticas em modelos animais. Na epilepsia, os mecanismos epigenéticos regulam genes dos canais iônicos e genes da plasticidade sináptica, contribuindo para a suscetibilidade às convulsões, com modificações de histonas e desregulação dos miRNAs sendo observadas. Distúrbios neurodesenvolvimentais exemplificam regulação epigenética crítica, como evidenciado por mutações no gene MECP2, codificando uma proteína de ligação ao metil-CpG, causando a síndrome de Rett e a hipermetilação de FMR1 na síndrome do X Frágil.
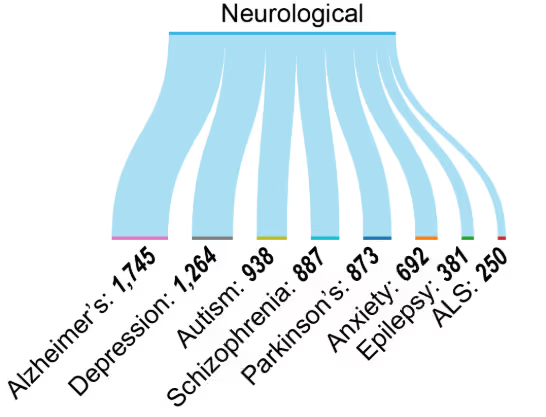
As alterações epigenéticas são cada vez mais reconhecidas como biomarcadores para distúrbios neurológicos. Padrões de metilação de genes como BDNF372 e COMT374 estão associados à função cognitiva e a transtornos psiquiátricos, enquanto marcas específicas de histonas (por exemplo, H3K27me3) estão ligadas a redes regulatórias gênicas na neurodegeneração. miRNAs circulantes, em particular miR-132376 e miR-124378, demonstraram potencial como biomarcadores não invasivos para o diagnóstico da doença de Alzheimer e da doença de Parkinson, respectivamente, oferecendo perspectivas para detecção precoce e monitoramento terapêutico.
Doença cardiovascular
Os mecanismos epigenéticos contribuem para a patogênese de várias doenças cardiovasculares, embora nossa análise dos dados de publicações sugira uma fração menor do interesse em pesquisa quando comparada ao câncer (ver Figura 4A). Por exemplo, na aterosclerose, a metilação do DNA e as modificações das histonas regulam genes envolvidos na inflamação, no metabolismo lipídico e na função endotelial. A hipometilação de genes pró-inflamatórios (ex.: IL-6384) e a hipermetilação de genes anti-inflamatórios (ex.: PPARγ385) promovem a formação de placas.
Alterações epigenéticas nos genes que regulam o tônus vascular e a homeostase do sódio contribuem para a hipertensão, enquanto fatores ambientais, como dieta rica em sal e estresse, podem induzir essas alterações epigenéticas. A regulação epigenética dos genes do canal iônico (por exemplo, SCN5A e KCNQ1392) pode predispor os indivíduos a arritmias. Da mesma forma, as modificações epigenéticas impulsionam a remodelação cardíaca patológica, incluindo hipertrofia e fibrose. A metilação do DNA, as modificações das histonas e os miRNAs são os principais reguladores desses processos. Na doença cardíaca isquêmica e no acidente vascular cerebral, a metilação do DNA e as modificações de histonas alteram a expressão de genes que regulam a sobrevivência celular, as respostas ao estresse e as vias inflamatórias.
Tal como acontece com as doenças neurológicas, estas alterações têm sido cada vez mais documentadas como biomarcadores. Padrões de metilação de genes como F2RL3400 e AHRR401 estão associados ao risco e aos desfechos cardiovasculares. Marcas específicas de histonas estão ligadas a redes regulatórias de genes na insuficiência cardíaca e na aterosclerose. Os miRNAs circulantes são usados como biomarcadores para infarto agudo do miocárdio e insuficiência cardíaca.
Distúrbios metabólicos
As modificações epigenéticas regulam genes que controlam a sensibilidade à insulina, o armazenamento de gordura e a inflamação em doenças metabólicas. Fatores ambientais, incluindo dieta e exercícios físicos, induzem alterações epigenéticas persistentes que contribuem para a resistência à insulina e disfunção metabólica.
As doenças metabólicas representam uma fração considerável da pesquisa epigenética (ver Figura 4A), com estudos sobre obesidade e diabetes tipo 2 dominando este campo. O volume substancial de publicações reflete a epidemia global de doenças metabólicas e uma compreensão crescente das contribuições epigenéticas para a disfunção metabólica. O crescimento constante, porém modesto, na pesquisa de epigenética metabólica é comparável aos distúrbios neurológicos e hematológicos (Figura 4B), mas contrasta com o aumento exponencial nos estudos de câncer, sugerindo um significativo potencial inexplorado nesta área.
Descobriu-se que a epigenética desempenha um papel fundamental em:
- Obesidade: metilação do DNA e modificações nas histonas que regulam genes da adipogênese, controle do apetite e gasto de energia, com miRNAs desregulados associados à obesidade e disfunção do tecido adiposo. Metilação do DNA e modificações de histonas que regulam genes envolvidos na adipogênese, no controle do apetite e no gasto energético, com miRNAs desregulados associados à obesidade e à disfunção do tecido adiposo.
- Diabetes tipo 2 (T2D): Alterações epigenéticas nas células β pancreáticas, no fígado e no músculo esquelético que afetam a produção e a sensibilidade à insulina, incluindo a metilação do DNA dos genes PPARGC1A e IRS1.
- Doença hepática gordurosa não alcoólica (DHGNA): a metilação do DNA e as modificações das histonas regulam o metabolismo lipídico hepático e a inflamação, com os miRNAs contribuindo para a progressão da doença.
- Síndrome metabólica: As alterações epigenéticas afetam os genes do metabolismo da glicose, do metabolismo lipídico e da regulação da pressão arterial.
- Doenças cardiometabólicas: mecanismos epigenéticos conectam desregulação metabólica a complicações cardiovasculares por meio da metilação do DNA de genes, incluindo FTO418 e ABCA1419, associados ao risco de aterosclerose e hipertensão.
Os biomarcadores epigenéticos para doenças metabólicas incluem padrões de metilação dos genes TXNIP e SREBF1 associados a T2D e NAFLD; marcas específicas de histonas ligadas a redes regulatórias de genes metabólicos; e miRNAs circulantes que servem como biomarcadores para T2D e obesidade. Esses biomarcadores possibilitam detecção precoce, estratificação de risco e monitoramento terapêutico em distúrbios metabólicos.
Doenças autoimunes
A metilação aberrante de genes de tolerância imunológica pode ativar células T autorreativas, levando a doenças autoimunes. Apesar de sua importância clínica, as doenças autoimunes representam uma parcela modesta da pesquisa em epigenética (ver Figura 4A), com crescimento constante, porém limitado, entre 2010 e 2024, em comparação com o aumento exponencial dos estudos sobre câncer (Figura 4B). Essa lacuna de pesquisa sugere um potencial significativo para uma investigação expandida sobre epigenética autoimune.
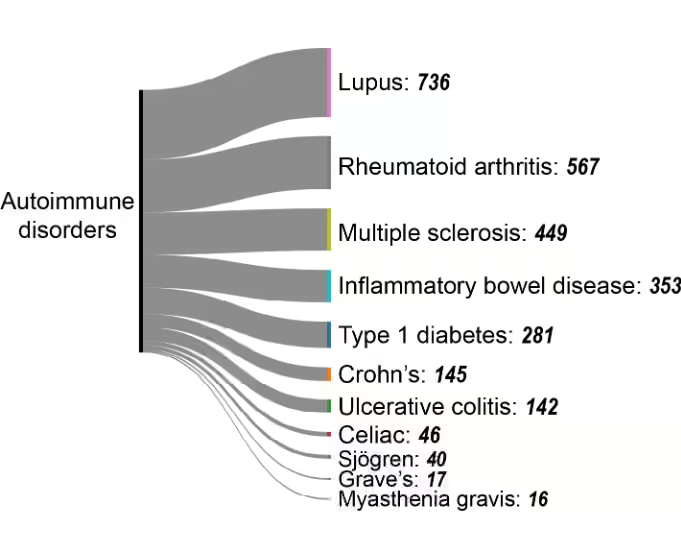
Dentro das doenças autoimunes, certas condições emergiram como áreas primárias de pesquisa (Figura 7):
- Lúpus eritematoso sistêmico (LES) patogênese associada com miRNAs desregulados.
- A artrite reumatoide (AR) envolve alterações de metilação do DNA em fibroblastos sinoviais e células imunes que promovem inflamação articular, enquanto modificações de histonas regulam a produção de citocinas pró-inflamatórias.
- A esclerose múltipla (EM) apresenta alterações epigenéticas em células T e B que afetam a regulação imunológica e os genes de destruição da mielina, sendo a desregulação de microRNAs associada à progressão da doença.
- Diabetes tipo 1 (T1D) envolve metilação do DNA e modificações de histonas em células β pancreáticas e células imunológicas que contribuem para a destruição autoimune das células produtoras de insulina, com miRNAs (por exemplo, miR-21, miR-34a) implicados na patogênese.
- Doenças inflamatórias intestinais (DII), como Crohn e colite ulcerativa, apresentam alterações epigenéticas em células epiteliais intestinais e células imunes, impulsionando inflamação crônica, juntamente com associação a desregulação de miRNA.
Terapêuticas em epigenética: aplicações clínicas de epi-drugs
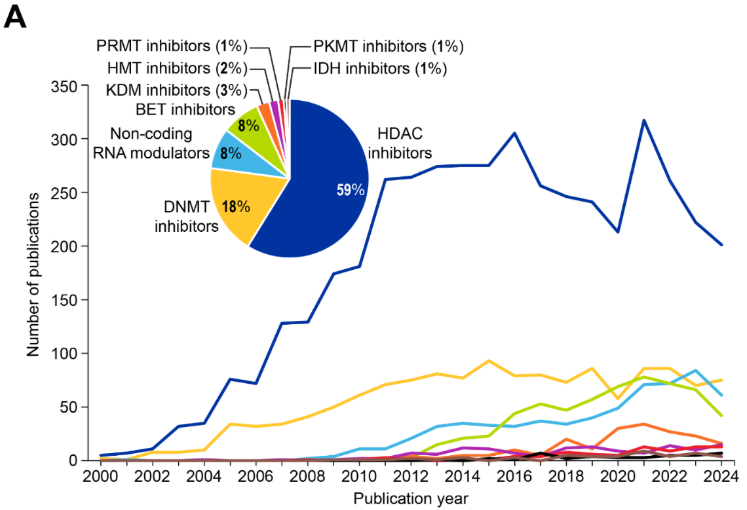
Os fármacos epigenéticos (epi-fármacos) revertem modificações epigenéticas aberrantes para restaurar a expressão gênica normal em doenças caracterizadas por desregulação epigenética. O cenário terapêutico (Ver Figura 8A) revela que os inibidores de HDAC dominam, com 59% das publicações, seguidos pelos inibidores de DNMT (18%) e pelos moduladores de RNA (8% cada para moduladores de ncRNA).
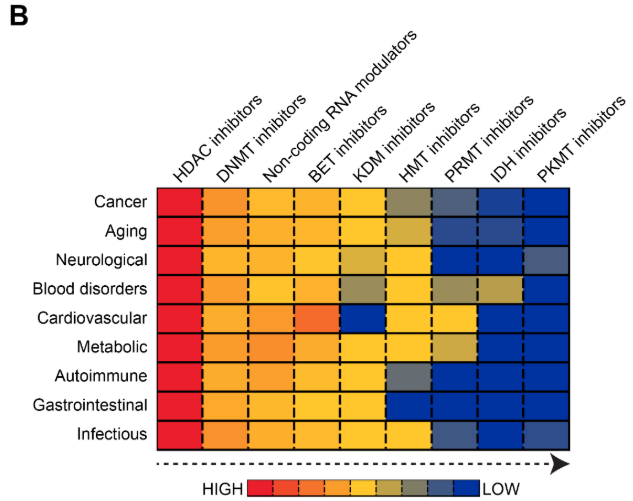
Epi-drugs atuais:
- Os inibidores da histona desacetilase (HDAC) impedem a remoção de grupos acetil das histonas, promovendo estruturas de cromatina mais flexíveis e aumento da expressão gênica, incluindo genes supressores de tumor. Os inibidores de HDAC também afetam proteínas não histonas, como fatores de transcrição e proteínas chaperonas, contribuindo ainda mais para seus efeitos anticancerígenos.
- Os inibidores de DNA metiltransferases (DNMT) representam a segunda maior classe de medicamentos em termos de publicações de pesquisas associadas. Eles bloqueiam os DNMTs, auxiliando assim na reativação de genes supressores de tumor silenciados no câncer. Os inibidores de DNMT atualmente aprovados para uso clínico são a azacitidina (Vidaza®) e a decitabina (Dacogen®), que são análogos de nucleosídeos incorporados ao DNA durante a replicação, ligam-se irreversivelmente às DNMTs e impedem a metilação.
- Os moduladores de ncRNA têm como alvo miRNAs ou lncRNAs para influenciar a regulação gênica. Os moduladores de RNA parecem ser uma categoria de crescimento rápido, especialmente desde 2018 (Figura 8A), refletindo o reconhecimento de miRNAs e lncRNAs como alvos passíveis de fármacos para medicina de precisão.
- Os inibidores do bromodomínio e do domínio extra-terminal (BET) bloqueiam a ligação das proteínas BET às histonas acetiladas, interrompendo a ativação transcricional dos oncogenes. As proteínas BET (por exemplo, BRD2, BRD3, BRD4) estão envolvidas no reconhecimento e na ligação de lisinas acetiladas em histonas e atuam como leitores "" de marcas epigenéticas.
- Os inibidores de histona lisina desmetilases (KDMs) bloqueiam enzimas pertencentes à família das lisina desmetilases (LSDs) ou à família de enzimas N-metil lisina desmetilases contendo o domínio Jumonji (JmjC). Até o momento, não existem inibidores aprovados de KDM, porém, um inibidor de KDM4 está atualmente em um ensaio clínico (zavondemstat) com pesquisas em andamento voltadas para o desenvolvimento de mais.
- Os inibidores da histona metiltransferase (HMT) têm como alvo enzimas que adicionam grupos metil a resíduos específicos de lisina ou arginina em proteínas histonas, as quais podem ativar ou reprimir a expressão gênica, dependendo da histona específica e da localização da metilação.
- Os inibidores da proteína arginina metiltransferase (PRMT) têm como alvo as metiltransferases de proteínas — enzimas responsáveis por adicionar grupos metil às proteínas e impactar a expressão gênica e os processos celulares. Os inibidores de HMT e os inibidores de metiltransferase de proteínas, como os inibidores de PRMT e PKMT, ainda estão em fase inicial de desenvolvimento, enquanto os inibidores de KDM demonstram potencial terapêutico emergente.
- Os inibidores da isocitrato desidrogenase (IDH) têm como alvo as formas mutantes das enzimas IDH, como IDH1 e IDH2, que produzem o oncometabolito 2-hidroxiglutarato. Essas enzimas causam hipermetilação do DNA e bloqueiam a diferenciação celular ao se acumularem nas células e inibirem as enzimas envolvidas na regulação epigenética, como as proteínas TET e as histonas desmetilases.
- Os inibidores da proteína EZH2 (Enhancer of zeste homolog 2) funcionam como inibidores específicos de HMT, reduzindo os níveis de H3K27me3 e reativando genes supressores de tumor silenciados, o que pode restaurar a diferenciação celular normal e inibir o crescimento tumoral, particularmente em cânceres com mutações ou superexpressão de EZH2.
- Os moduladores epigenéticos de dupla ação ou multi-epigenéticos combinam mecanismos que visam múltiplas vias epigenéticas. Esses medicamentos podem aumentar a eficácia terapêutica em doenças complexas.
Análise de coocorrência
O cenário clínico da terapêutica epigenética demonstra sucesso regulatório, com13 medicamentos aprovados pela FDA dos EUA visando os principais reguladores epigenéticos (veja a Figura 9).
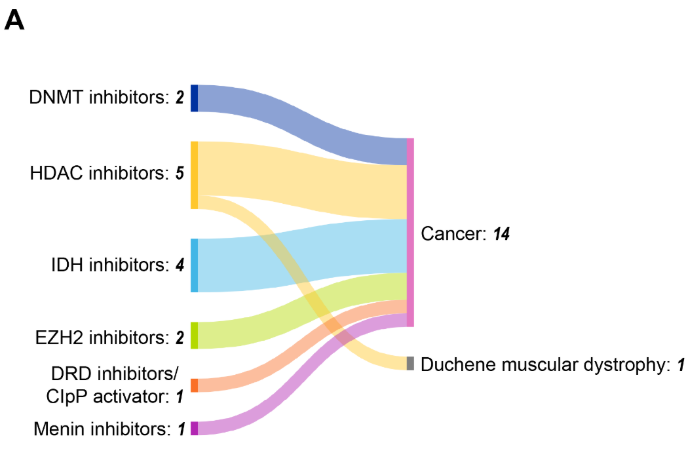
Os inibidores de HDAC lideram com cinco aprovações, e malignidades hematológicas representam a principal aplicação terapêutica, representando 12 das 15 indicações aprovadas. Essa concentração reflete a sensibilidade dos cânceres sanguíneos à desregulação epigenética e a acessibilidade dos alvos hematológicos em comparação com os tumores sólidos.
Os inibidores de DNMT azacitidina (2004) e decitabina (2006) estiveram entre os primeiros medicamentos epigenéticos aprovados, estabelecendo uma prova de conceito para direcionar a metilação do DNA em síndromes mielodisplásicas e LMA. Inibidores de HDAC, incluindo vorinostat, romidepsina e belinostat, demonstraram eficácia em diversas neoplasias hematológicas, validando a modificação de histonas como alvo terapêutico.
Medicamentos epigenéticos em ensaios clínicos
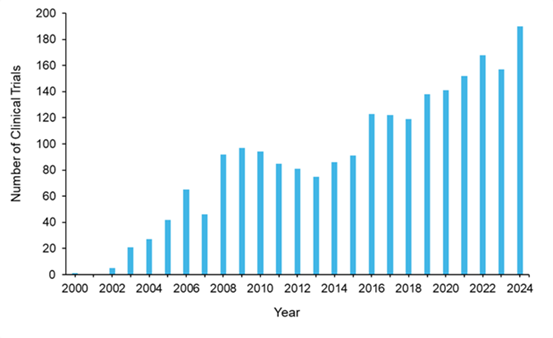
O cenário dos medicamentos epigenéticos em ensaios clínicos se expandiu dramaticamente ao longo de 25 anos, com quase 2.200 ensaios registrados em clinicaltrials.gov (veja a Figura 10). Houve um aumento sustentado de um único ensaio em 2000 para pouco menos de 200 ensaios clínicos por ano em 2024, com oscilações notáveis que refletem marcos regulatórios e dinâmicas de mercado. Após a aprovação da azacitidina pela FDA (Food and Drug Administration) dos EUA em 2004, a atividade dos ensaios clínicos demonstrou padrões de aumento e diminuição, com uma trajetória geral ascendente. Esse padrão de crescimento indica investimento farmacêutico sustentado, apesar das fases periódicas de consolidação.
A análise de ensaios clínicos epigenéticos terapêuticos em relação à distribuição de fases revela que os ensaios de Fase II predominam com 57%, seguidos pelos de Fase I (32%) e Fase III (9%). Essa distribuição é típica do desenvolvimento de medicamentos e reflete a alta taxa de insucesso no desenvolvimento de fármacos epigenéticos, bem como a natureza exploratória de muitas estratégias de combinação. Notavelmente, 62% dos ensaios clínicos envolvem medicamentos aprovados pela FDA (Food and Drug Administration) dos EUA, o que sugere esforços extensivos de expansão da bula e exploração de terapias combinadas além das indicações iniciais. Os restantes 38% dos ensaios clínicos são para medicamentos mais recentes/inovadores e ainda não aprovados.
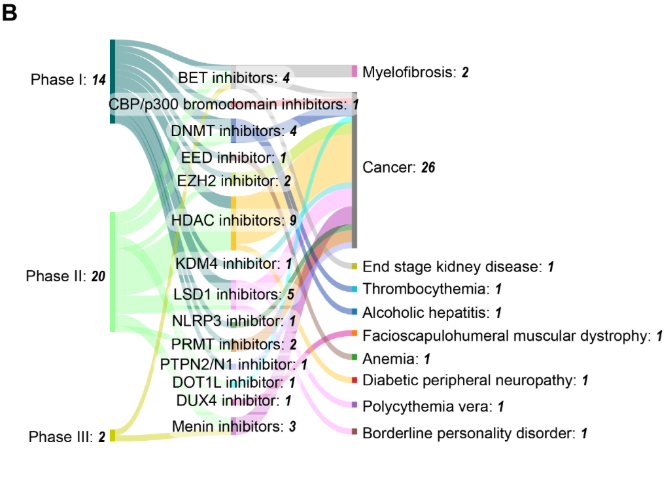
O pipeline de desenvolvimento clínico revela uma atividade robusta, com 36 ensaios em andamento em três fases. Os ensaios de fase II predominam (23 ensaios), com inibidores de DNMT e HDAC mantendo uma forte presença clínica, com 4 e 11 ensaios, respectivamente. Há também diversificação além dos inibidores de DNMT e HDAC, com inibidores de LSD1, BET e menina sendo cada vez mais explorados (ver Figura 9B). Essa distribuição demonstra tanto a otimização contínua de alvos já estabelecidos quanto a expansão para novos reguladores epigenéticos. As aplicações em câncer continuam a predominar com 26 dos 36 ensaios, embora os dados sugiram incentivar a diversificação para condições não oncoológicas, incluindo trombocitemia, hepatite alcoólica, mielofibrose e neuropatia periférica diabética.
Agentes promissores em desenvolvimento clínico
Dentre os vários medicamentos em desenvolvimento, alguns se destacam como promissores para o câncer e outras doenças:
- Agentes oncológicos:
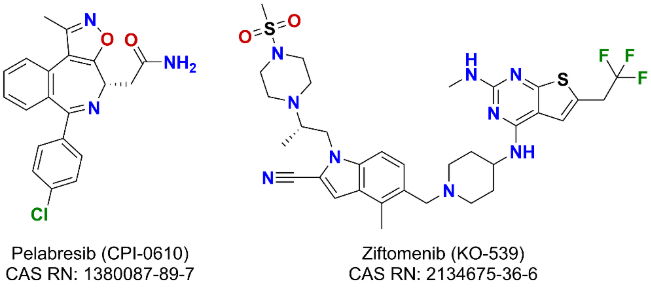
- O Pelabresib (CPI-0610), um inibidor avançado de BET, chegou aos testes de Fase III para mielofibrose.
- O ziftomenib (KO-539), um inibidor seletivo de pequenas moléculas da interação proteína-proteína menina-KMT2A, recebeu a designação de Terapia Inovadora (Breakthrough Therapy) da FDA dos EUA em março de 2024 para LMA com mutação NPM1 recidivante ou refratária.
- Agentes não oncológicos:
- Apabetalone (RVX-208), um inibidor seletivo de BET que tem como alvo domínios BD2, está atualmente em Fase I/II para doença renal em estágio terminal.
- O larsucosterol (DUR-928), um oxisterol sulfatado endógeno e regulador epigenético pioneiro, está em ensaios clínicos de Fase II para hepatite alcoólica.
- O vafidemstat (ORY-2001) é um inibidor seletivo da LSD1 que está atualmente sendo avaliado em ensaios clínicos de Fase II para o transtorno de personalidade borderline.
- Agentes aprovados recentemente:
- Modeyso (Dordaviprone) recebeu aprovação acelerada da FDA dos EUA em agosto de 2025 para gliomas difusos de linha média com mutação H3K27M em pacientes com mais de um ano de idade.
- O Revuforj (Revumenibe) obteve a aprovação do FDA dos EUA em novembro de 2024 para LMA rearranjada com KMT2A recidivante/refratária em adultos e pacientes pediátricos.
Epigenética na medicina personalizada
A integração de dados epigenéticos auxilia no desenvolvimento de ferramentas de diagnóstico altamente precisas, marcadores prognósticos e abordagens terapêuticas, particularmente para doenças complexas. Como observado, os epifármacos, incluindo inibidores de DNMT e inibidores de HDAC, já estão estabelecidos clinicamente e continuam a ser desenvolvidos. Terapias combinadas que integram medicamentos epigenéticos com quimioterapia e imunoterapia também estão aprimorando a eficácia do tratamento, representando um avanço fundamental em abordagens terapêuticas personalizadas.
Outra descoberta importante na epigenética é a utilização dessas modificações como biomarcadores específicos de tecido. Exemplos desses padrões específicos de doenças incluem a hipermetilação de genes supressores de tumor no câncer e a metilação aberrante e modificações de histonas em pacientes com doença de Alzheimer ou doença de Parkinson.
A identificação desses biomarcadores epigenéticos permite a detecção e o diagnóstico precoces de doenças. Por exemplo, poderia fazer isso por meio de biópsias líquidas usadas para detectar padrões de metilação de DNA específicos do câncer no sangue ou em outros fluidos corporais para diagnóstico e monitoramento não invasivos e testes pré-natais por meio de marcadores epigenéticos no sangue materno para avaliar a saúde fetal. Marcadores epigenéticos prognósticos podem prever os resultados da doença e a resposta à terapia. Por exemplo, o estado de metilação prediz resultados e probabilidade de metástase em alguns tipos de câncer, enquanto alterações epigenéticas em transtornos psiquiátricos podem predizer a resposta à medicação.
Aplicações clínicas de biomarcadores epigenéticos
Biomarcadores epigenéticos são importantes para diagnóstico de doença, prognóstico e tomada de decisão terapêutica. Analisamos publicações na CAS Content Collection específicas para biomarcadores epigenéticos e encontramos um aumento acentuado a partir de 2008-2009, marcado por alguns períodos de estabilização (2015-2017 e 2023-2024) (ver Figura 11).
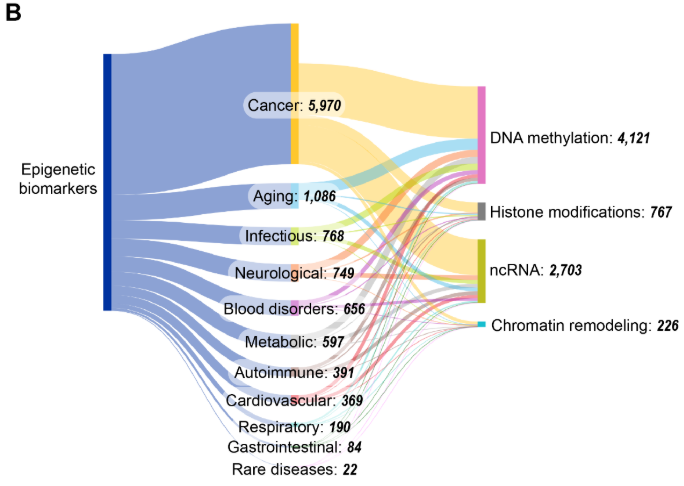
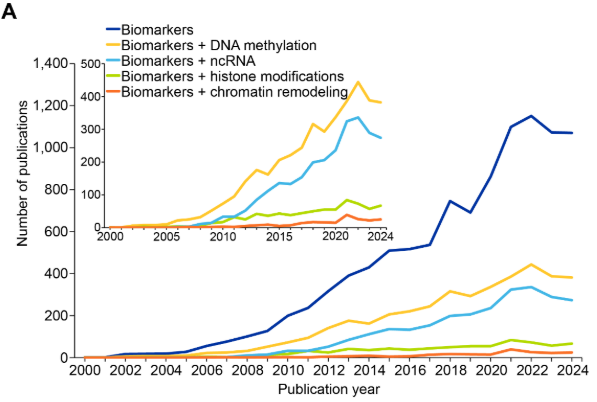
Entre os quatro principais mecanismos epigenéticos, a metilação do DNA e o ncRNA parecem ser os mais bem estudados, com as publicações relacionadas a biomarcadores de metilação do DNA e ncRNA dobrando entre 2015 e 2022, enquanto as modificações de histonas e o remodelamento da cromatina permanecem comparativamente pouco explorados nesse contexto. Como observado na Figura 11B, o câncer parece coocorrer com maior frequência em publicações relacionadas a biomarcadores epigenéticos, refletindo o papel bem estabelecido da desregulação epigenética na oncogênese e a utilidade clínica de marcadores de metilação como MGMT516 e VIM517 para diagnóstico e prognóstico. A expressiva representação da pesquisa sobre envelhecimento está alinhada com os recentes avanços no desenvolvimento do relógio epigenético e suas aplicações na avaliação da idade biológica.
biomarcadores de metilação do DNA
Padrões aberrantes de metilação do DNA servem como marcadores de doenças, sendo a hipermetilação de supressores tumorais um biomarcador comum de vários tipos de câncer. Por exemplo, a metilação de SEPT9 possibilita a triagem não invasiva do câncer colorretal por meio da detecção em sangue, como alternativa à colonoscopia. A metilação MGMT prevê a resposta da temozolomida no glioblastoma, com a hipermetilação associada a melhores desfechos. A metilação do gene BRCA1 serve como marcador diagnóstico e prognóstico associado ao aumento do risco de câncer de mama e de ovário. Notavelmente, a metilação do DNA ocorre predominantemente em conjunto com a pesquisa de biomarcadores epigenéticos, provavelmente devido à sua estabilidade química, metodologias estabelecidas de detecção e tradução clínica direta por meio de testes aprovados pela FDA.
Biomarcadores de modificação de histonas
As modificações das histonas influenciam a estrutura da cromatina e a expressão gênica, e marcas específicas de histonas estão associadas a estados patológicos. A coocorrência relativamente modesta de modificações histonas que vemos na Figura 11B sugere potencial não explorado, especialmente dada sua natureza dinâmica e resposta a intervenções terapêuticas.
A perda da acetilação da histona H4 prevê um prognóstico ruim em certos cânceres, enquanto a trimetilação da lisina 27 da histona H3 (H3K27me3) reflete desregulação da PRC2 e se correlaciona com um prognóstico ruim em cânceres de próstata e bexiga. A citrulinação das histonas H3/H4 está ligada à produção de anticorpos anti-proteínas citrulinadas (ACPA), uma característica da artrite reumatoide que permite o diagnóstico e o monitoramento.
Apesar desses achados promissores, permanecem desafios como a natureza altamente lábil das modificações de histonas e sua suscetibilidade à degradação enzimática, causando perda rápida de sinal em minutos após a coleta da amostra. Protocolos atuais exigem tampões de preservação especializados contendo inibidores de proteases, desacetilases e desmetilases, o que complica a implementação clínica de rotina.
biomarcadores de ncRNA
Os ncRNAs, incluindo miRNAs como miR-21529 e miR-155530, são superexpressos em vários tipos de câncer e servem como biomarcadores diagnósticos e prognósticos através de fluidos corporais. A coocorrência substancial de ncRNA com a pesquisa de biomarcadores epigenéticos reflete o interesse crescente em miRNAs e lncRNAs circulantes como biomarcadores minimamente invasivos.
Por exemplo, a superexpressão de miR-21 está associada a crescimento tumoral, invasão, metástase e resistência à quimioterapia em câncer de mama, pulmão e colorretal. Níveis elevados de miR-208a servem como biomarcador para infarto agudo do miocárdio (ataque cardíaco). A superexpressão do lncRNA HOTAIR também está associada a metástase e prognóstico ruim em cânceres de mama, colorretal e pancreático.
Biomarcadores de remodelação da cromatina
Os padrões de remodelação da cromatina preveem a resistência terapêutica, com regiões de cromatina abertas em células cancerígenas resistentes a medicamentos sendo usadas para prever a falha do tratamento. Assim como as modificações de histonas, a relativa baixa coocorrência de remodelação da cromatina sugere um potencial inexplorado.
De modo geral, o futuro dos biomarcadores epigenéticos reside no desenvolvimento de tecnologias robustas e de alto rendimento, bem como em abordagens integrativas. A integração multiômica combinando dados epigenéticos, genômicos, transcriptômicos e proteômicos aprimorará a descoberta e validação de biomarcadores. A detecção não invasiva de biomarcadores epigenéticos em fluidos corporais revolucionará o diagnóstico precoce e o monitoramento.
Espera-se que ferramentas computacionais avançadas ajudem a identificar assinaturas epigenéticas complexas para estratificação de pacientes. Por exemplo, a edição do epigenoma baseada em CRISPR pode permitir a manipulação de marcas epigenéticas associadas a doenças para fins terapêuticos, potencialmente fazendo com que biomarcadores passem de ferramentas diagnósticas a ferramentas terapêuticas.
Implicações éticas, legais e sociais da epigenética na medicina
A epigenética tem o potencial de transformar nossa compreensão da saúde e da doença, mas também levanta desafios éticos, legais e sociais significativos. Enfrentar esses desafios requer uma abordagem proativa e colaborativa que equilibre os benefícios da pesquisa epigenética com a necessidade de proteger os direitos individuais e promover a justiça social. Ao desenvolver diretrizes éticas robustas, proteções legais e estratégias de engajamento público, podemos aproveitar o poder da epigenética para melhorar a saúde e o bem-estar, minimizando ao mesmo tempo possíveis danos.
Considerações éticas
- Privacidade e discriminação: as informações epigenéticas, assim como dados genéticos, são altamente pessoais e podem revelar informações sensíveis sobre a saúde de um indivíduo, suas escolhas de estilo de vida e exposições ambientais, exigindo, portanto, proteções robustas de privacidade. Por exemplo, marcadores epigenéticos que preveem o risco de doenças poderiam permitir a discriminação por parte das seguradoras de saúde através do aumento dos prêmios ou da recusa de cobertura. Da mesma forma, a capacidade de detectar modificações epigenéticas decorrentes de comportamentos passados levanta preocupações sobre avaliações de saúde retroativas e discriminação no emprego.
- Responsabilidade individual e impactos transgeracionais: Correlatamente, informações epigenéticas podem resultar na atribuição de culpa aos indivíduos por suas condições de saúde, desconsiderando determinantes sociais e ambientais mais amplos da saúde. Alterações epigenéticas induzidas por fatores ambientais podem, por vezes, ser transmitidas às gerações futuras. Isso levanta preocupações éticas sobre as consequências a longo prazo de intervenções que alteram marcadores epigenéticos.
Requisitos legais
- Fiscalização regulatória: A proliferação de kits de teste epigenético vendidos diretamente ao consumidor levanta preocupações sobre precisão, interpretação e regulamentação. Os marcos legais devem garantir que essas aplicações sejam baseadas em evidências e eticamente sólidas, ao mesmo tempo que impedem a comercialização prematura de tecnologias não comprovadas.
- Responsabilidade e propriedade intelectual: Modificações epigenéticas ligadas à exposição ambiental levantam questões complexas de responsabilidade. Por exemplo, os danos causados por toxinas devem ser da responsabilidade dos empregadores, dos fabricantes ou dos governos? A possível responsabilização legal por danos epigenéticos em fetos devido à negligência dos pais ou de terceiros, ou por exposições ambientais, exigiria uma análise cuidadosa. A comercialização da pesquisa epigenética, como biomarcadores ou terapias, levanta questões sobre patenteamento e titularidade, exigindo um equilíbrio entre a inovação e a manutenção do acesso público às tecnologias epigenéticas.
Implicações sociais
- Compreensão pública e equidade: a compreensão limitada do público sobre epigenética favorece equívocos e a exploração por meio de terapias não comprovadas (por exemplo, “dietas epigenéticas”). Uma educação abrangente e uma comunicação científica robusta são essenciais para abordar esse problema e melhorar a tomada de decisões informadas. A pesquisa epigenética que relaciona a exposição ambiental a doenças também pode contribuir para a estigmatização de certas comunidades ou populações, particularmente aquelas expostas a altos níveis de poluição ou toxinas. Para garantir o acesso equitativo às terapias epigenéticas e evitar a exacerbação das disparidades de saúde, são necessárias intervenções políticas deliberadas que abordem as barreiras socioeconômicas.
- Estratégias de implementação: Uma governança eficaz exige diretrizes éticas claras para a coleta, o uso e o compartilhamento de dados epigenéticos; marcos legais atualizados que abordem os desafios específicos das informações epigenéticas; o engajamento do público para promover confiança e consentimento informado; e a cooperação internacional para garantir padrões consistentes entre jurisdições. Ao desenvolver proteções robustas e, ao mesmo tempo, promover a inovação responsável, a sociedade pode aproveitar o potencial transformador da epigenética, salvaguardando os direitos individuais e promovendo a equidade em saúde.
Direções futuras para a epigenética
O cenário da pesquisa em epigenética passou por uma transformação notável na última década, evoluindo de uma área especializada da biologia molecular para uma disciplina biomédica dominante, com profundas implicações para a saúde humana e a intervenção terapêutica. A transposição clínica da pesquisa epigenética alcançou um sucesso notável, com 15 medicamentos aprovados pelo FDA validando alvos epigenéticos como terapeuticamente viáveis. Os 36 ensaios clínicos em andamento em várias fases de desenvolvimento indicam investimento sustentado e confiança na terapêutica epigenética, incentivando a diversificação além da oncologia, os ensaios agora abrangem doenças metabólicas, neurológicas, inflamatórias e raras.
Essa mudança reflete o reconhecimento crescente de que fatores ambientais, como dieta, estresse, toxinas e escolhas de estilo de vida, induzem alterações epigenéticas hereditárias com implicações transgeracionais. A integração de dados de exposição ambiental com perfis epigenéticos individuais possibilita avaliações de risco personalizadas e estratégias de intervenção, representando uma mudança fundamental em direção a abordagens de medicina preventiva e de precisão.
O futuro da epigenética é brilhante, com imenso potencial para aprimorar nossa compreensão da biologia e melhorar a saúde humana. No entanto, a realização desse potencial exigirá a superação de desafios significativos, incluindo limitações tecnológicas, questões éticas e a complexidade da regulação epigenética. Ao fomentar a colaboração interdisciplinar, investir em tecnologias inovadoras e enfrentar as implicações éticas e sociais, o campo da epigenética pode continuar a realizar descobertas revolucionárias e traduzi-las em benefícios clínicos e sociais significativos.