表观遗传学是研究不涉及 DNA 序列改变的可遗传基因表达变化的学科,已成为生物学和医学中具有变革性的领域,揭示了基因表达如何响应内外部信号进行调控。表观遗传调控是发育生物学、疾病发病机制、基因-环境相互作用、跨代遗传以及治疗开发的基础。通过阐明基因在静态基因组之外的动态调控机制,表观遗传学将遗传学与环境影响联系起来,为疾病机制研究和创新疗法提供了重要洞察。
我们分析了 CAS 内容合集™,全球最大的人工收录科学信息库,以概述表观遗传学研究的进展,并识别关键的新兴概念和挑战。这一综合分析考察了影响现代生命科学和医疗的科学基础、临床应用及技术创新。
我们的分析发现,在过去二十年中,相关出版物数量呈陡峭且持续的增长,目前 CAS 内容合集中已有超过 12 万篇与表观遗传学相关的出版物(见图 1)。该领域以期刊文章为主(占 97%),专利仅占出版物的 3%(见图 1A),表明表观遗传学仍处于发现和验证阶段。
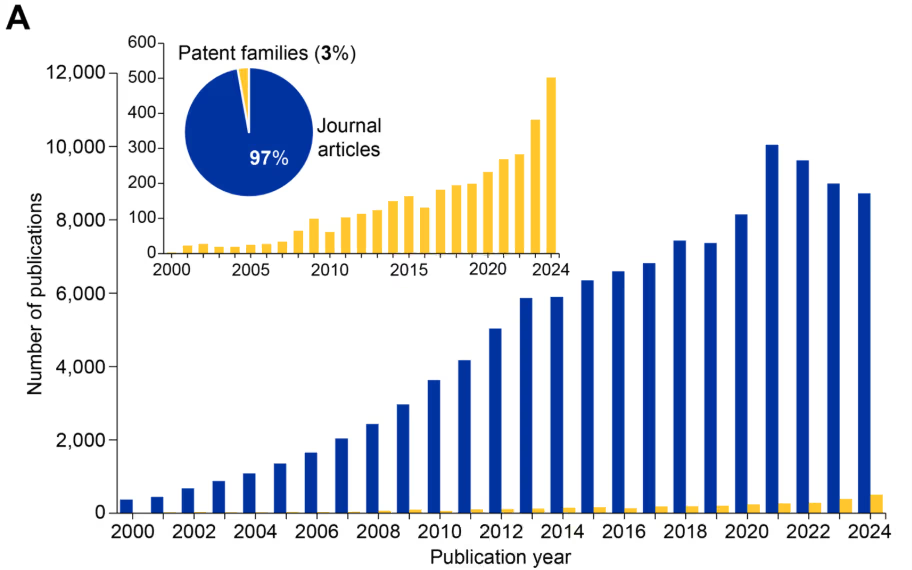


然而,专利出版物的急剧增加(见图 1A 的插图)表明这一快速发展的领域中商业兴趣和转化潜力正在增长。值得注意的是,自 2014 年以来,表观遗传学的出版物数量已超过遗传学(图 1B)。表观转录组学作为一个独立领域的出现,在 2020 年之后开始显现(图 1B)。
这一增长趋势与资金大幅增加相一致,总研究经费从 2004 年的 2 亿美元增长到 2024 年的超过 45 亿美元,每年支持约 2,700 个项目(见图 1C)。项目数量和资助水平的持续上升,以及平均项目经费从 120 万美元增加到 170 万美元,凸显了政府和私营部门在推进表观遗传学研究及其临床转化方面的持续投入与承诺。
表观遗传学的商业价值显著提升,2023 年全球表观遗传学市场价值为 18.4 亿美元,预计到 2033 年将达到 67.7 亿美元。这一增长得益于十余种 FDA 批准的表观遗传学药物,包括用于癌症治疗的阿扎胞苷 (Vidaza®) 和沃利诺昔特 (Zolinza®)。此外,还有 35 种以上表观遗传疗法正在进行临床试验。这些候选药物主要针对各类恶性肿瘤,但已开始显示出向癌症之外领域的多样化发展趋势。
让我们更深入地探讨表观遗传学,以了解其发展动态及其对未来医学的意义:
表观遗传调控的核心机制
表观遗传机制通过对 DNA 和染色质结构的化学修饰来调控基因表达,而不改变 DNA 序列。这些机制主要包括四类:DNA 甲基化、组蛋白修饰、非编码 RNA (ncRNA) 调控以及染色质重塑。在我们审视与表观遗传学相关的出版物时,最初涉及这些机制的出版物数量很少,这是可以理解的,因为该领域在 2000 年代初尚处于建立阶段(见图 2)。
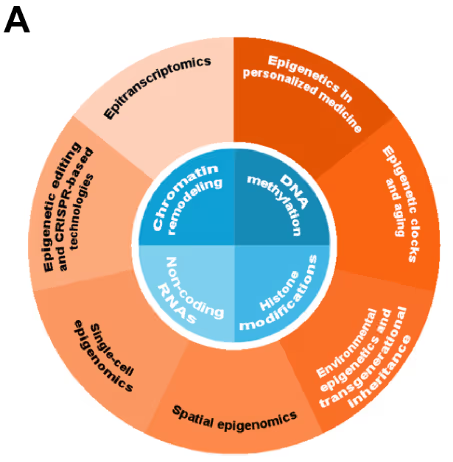

随后,四种机制均显示出加速增长,其中 DNA 甲基化增长最为迅猛,无论在期刊还是专利出版物中,都成为研究领域的主导。其他机制也都有所增长,这表明表观遗传学靶点在药物开发中的重要性正逐渐得到认可。
DNA甲基化
DNA 甲基化是一种基础的表观遗传机制,涉及将甲基 (–CH₃) 添加到 DNA 中 CpG 二核苷酸的胞嘧啶环上,从而导致转录抑制。这种修饰在 X 染色体失活、基因组印记以及转座子抑制中起着关键作用。
DNA 甲基化是由 DNA 甲基转移酶 (DNMT) 催化的。DNMT1 在复制过程中维持已有的甲基化模式,而 DNMT3a/3b 则在发育过程中或响应环境信号时建立新的甲基化模式。DNMT3L 缺乏催化活性,主要在早期发育中表达,成年后仅限于生殖细胞和胸腺中。DNMTs 靶向 CpG 岛,即 CpG 二核苷酸频率较高的区域,这些区域通常位于基因启动子附近。
在包括癌症、心血管疾病、心理健康障碍、阿尔茨海默病、自闭症以及代谢综合征等多种疾病中,已发现异常的甲基化模式被识别。肿瘤抑制基因启动子的高甲基化会使其表达沉默,从而促进肿瘤发生;而全基因组低甲基化则可能激活癌基因并导致基因组不稳定。DNA 甲基化模式会随年龄变化,包括错误的累积和甲基化维持的准确性下降。
组蛋白修饰
组蛋白修饰可以通过细胞分裂遗传,并可能受到环境因素的影响,从而对发育和疾病状态产生作用。组蛋白的翻译后修饰,如乙酰化、甲基化、磷酸化和泛素化,会改变染色质结构及基因的可及性。组蛋白乙酰转移酶 (HAT) 和去乙酰酶 (HDAC) 通过催化组蛋白乙酰基的添加和去除来调控乙酰化,而甲基转移酶 (HMT) 和去甲基酶 (HDM) 则负责调控甲基化。这些修饰主要发生在组蛋白尾部的赖氨酸、精氨酸、丝氨酸和苏氨酸残基上,组蛋白尾部是从核小体核心伸出的区域,可及性较高。
组蛋白修饰会影响染色质的结构。染色质是 DNA 围绕组蛋白蛋白质包装形成的复合体,它在基因表达、DNA 修复以及有丝分裂期间的染色体凝缩中起调控作用。异常的组蛋白修饰会破坏基因表达模式,促进肿瘤发生和转移,并且与其他疾病和障碍相关,如阿尔茨海默病、亨廷顿病、自闭症、与衰老相关的染色质变化以及免疫功能失调。
这些变化通常形成“组蛋白密码”,不同残基上的修饰组合通过协同或拮抗作用微调染色质状态。它们是调控染色质结构和基因表达的动态且多功能的系统,其可逆性使其成为具有潜力的治疗干预靶点。
非编码 RNA (ncRNA)
非编码 RNA (ncRNA) 是一类多样化的调控分子,在基因表达和染色质动态调控中发挥关键作用,但不编码蛋白质。这些 RNA 通过靶向信使 RNA (mRNA) 进行降解或调节转录机制,从而微调基因表达过程。
三类 RNA 已成为主要的表观遗传调控因子:微小 RNA (miRNA)、长非编码 RNA (lncRNA) 以及 PIWI 互作 RNA (piRNA)。这些非编码 RNA 通过五种主要机制协调表观遗传调控:
- 染色质重塑:lncRNA 将染色质修饰复合物招募到特定基因组位点,从而影响染色质结构和基因表达。例如,X 染色体失活特异性转录本 (XIST) 通过招募多梳抑制复合物 2 (PRC2) 介导 X 染色体失活。
- 转录调控:miRNA 和 lncRNA 通过与转录因子或 RNA 聚合酶相互作用来调节转录。例如,lncRNA HOX 转录本反义间隔 RNA (HOTAIR) 招募 PRC2,以抑制另一条染色体上的基因表达。
- 转录后调控:miRNA 结合靶信使 RNA (mRNA) 的 3′ 非翻译区 (UTR),导致其降解或翻译抑制。lncRNA 可以充当分子“海绵”吸附 miRNA,从而阻止它们靶向 mRNA。
- RNA 修饰:一些非编码 RNA 指导 RNA 甲基化(例如 N6-甲基腺苷,m6A)或编辑,从而影响 RNA 的稳定性和翻译。
- 基因组防御:piRNA 和 siRNA 抑制转座子,从而保护基因组完整性。siRNAs 可以在含有重复序列的区域引导异染色质的形成。
染色质重塑
染色质重塑动态地改变染色质结构,使其在常染色质(开放、转录活跃)与异染色质(致密、转录沉默)状态之间转换。染色质的基本单位是核小体,由 DNA 围绕一组八聚体组蛋白包装而成。染色质重塑由依赖 ATP 的复合物完成,例如 switch/sucrose nonfermentable (SWI/SNF)、imitation switch (ISWI)、chromodomain helicase DNA (CHD) 结合蛋白以及 INO80 家族,它们利用 ATP 水解为核小体的重新定位、驱逐或重构提供能量。
重塑机制包括核小体滑动、组蛋白驱逐/交换以及染色质压缩/解压缩。这些过程与 DNA 甲基化和组蛋白修饰协同作用,以调控基因表达、细胞分化和身份维持。
染色质重塑失调与癌症、神经系统疾病以及发育性疾病相关。例如,染色质重塑因子如富 AT 区相互作用结构域 1A(ARID1A)(SWI/SNF 复合物的组成部分)的突变,在恶性肿瘤中常被观察到。染色质重塑因子是逆转异常基因表达的有前景的治疗靶点。因此,染色质重塑被认为是环境因素(饮食、压力、毒素等)对基因表达和健康影响的中介。
表观遗传学的最新进展
近期的研究进展显示,表观遗传修饰,包括 DNA 甲基化、组蛋白修饰、非编码 RNA 调控和染色质重塑,在疾病发生机制中发挥作用,尤其是在癌症中。关于 miRNA 及其他非编码 RNA 作为表观遗传调控因子的最新研究,已发现新的治疗靶点;同时,个体表观遗传谱分析的进展正在推动个性化医疗方法的发展。出版趋势显示了主要的研究兴趣领域(见图 3)。

环境表观遗传学
饮食、压力、毒素和生活方式等环境因素可以通过前文讨论的各种机制诱导表观遗传变化。这些修饰可能通过改变细胞功能和组织稳态,促成癌症、代谢紊乱和神经系统疾病等疾病的发展。具体影响因素包括:
- 营养物质的可用性(如叶酸、维生素 B12)会影响 DNA 甲基化模式。
- 化学物质暴露(如双酚 A、农药、空气污染物)可改变表观遗传标记,进而导致长期健康影响。
- 心理和生理压力可诱导应激反应基因的表观遗传变化,并调节心理健康。
- 生活方式因素(如吸烟、饮酒、身体活动水平)通过调节表观遗传状态影响疾病风险。
表观转录组学
表观转录组学关注 RNA 分子的化学修饰及其在调控基因表达和细胞功能中的作用。正如表观遗传学研究对 DNA 和组蛋白的修饰如何在不改变 DNA 序列的情况下影响基因活性,表观转录组学则探讨 RNA 修饰如何影响 RNA 的稳定性、翻译、剪接及其他过程。
已在 mRNA、tRNA、rRNA 和 ncRNA 中鉴定出 170 多种不同的 RNA 修饰,其中 N6-甲基腺苷 (m6A) 是最丰富且在真核生物 mRNA 中研究最广泛的修饰。主要修饰包括:m6A 甲基化,发生在腺苷的 N6 位,影响 mRNA 的稳定性、剪接、转运和翻译;m5C 甲基化,发生在 mRNA 和 tRNA 的胞嘧啶 N5 位,影响 RNA 的稳定性和翻译;Ψ(假尿苷),尿苷的异构体,可增强 RNA 的稳定性和翻译效率;以及腺苷向次黄嘌呤脱氨,改变碱基配对特性,影响剪接和蛋白编码。
表观转录组学机制由三类主要蛋白组成:
- “写入者 (Writers)”:添加修饰的酶(例如用于 m6A 甲基化的 METTL3/METTL14 复合物)。
- “擦除者 (Erasers)”:去除修饰的酶(例如用于 m6A 去甲基化的脂肪质量与肥胖相关蛋白 FTO 以及 ALKBH5 RNA 去甲基酶)。
- “读取者 (Readers)”:识别并结合修饰 RNA 的蛋白(例如用于 m6A 识别的 YTH 结构域蛋白),它们共同调控 RNA 修饰的动态变化。
RNA 修饰调控多种细胞过程,这些修饰的失调会导致各种疾病。在癌症中,m6A 修饰常在肿瘤中发生改变,并与肿瘤进展、转移及药物耐受相关。异常的 RNA 编辑和修饰还与包括阿尔茨海默病、帕金森病及渐冻症 (ALS) 在内的神经退行性疾病相关。此外,包括 HIV 和 SARS-CoV-2 在内的 RNA 病毒利用宿主的 RNA 修饰机制调控病毒复制和免疫逃逸,其中也涉及表观遗传修饰。
高通量测序技术使得 RNA 修饰的全基因组绘图成为可能,同时结合质谱和化学标记技术,可用于修饰的检测和定量。这些进展为以 RNA 修饰酶为靶点的治疗开发提供了便利。
针对 RNA 修饰机制的各类组分(写入者、擦除者和读取者)被探索作为疾病治疗策略。例如,FTO(m6A 去甲基化酶)抑制剂在癌症治疗中显示出潜力,而 mRNA 疫苗中的修饰核苷则可增强稳定性和翻译效率。
总体而言,当前研究重点包括破解“表观转录组密码”、开发用于精确体内操作 RNA 修饰的工具,以及探索非编码 RNA 中的修饰。单细胞表观转录组学揭示了细胞类型特异性的 RNA 修饰模式及其功能后果。一项新兴技术多组学整合,将表观基因组数据与转录组学、蛋白质组学和代谢组学结合,利用 CUT&RUN 和 Hi-C 整合等技术,提供对细胞功能的整体视角。这些方法使得在复杂疾病中进行全面的通路分析和生物标志物发现成为可能。
跨代遗传
跨代遗传是指环境诱导的表观遗传变化在多代之间传递,而不依赖于 DNA 序列的改变。这一现象已在植物和动物中被观察到,表明一代经历的环境暴露可能影响后代的健康和发育。然而,在人类中验证这一过程的范围和意义仍具有挑战性。
跨代表观遗传的例子包括荷兰饥荒(1944-1945 年),在经历饥荒暴露的个体后代中观察到 DNA 甲基化模式的改变以及代谢风险增加。动物研究也提供了内分泌干扰物(如维氯佐林)对生殖、行为和疾病易感性的跨代影响示例,而在人类中,父亲吸烟和母亲压力已被发现与后代的表观遗传变化相关。
虽然跨代表观遗传的具体机制尚未完全明了,但它对后代疾病风险的提升(如肥胖、糖尿病和心血管疾病),表明这一领域仍然是活跃的研究方向。理解跨代效应还有助于制定政策,以减少有害环境因素的暴露,尤其是在关键发育阶段(如妊娠期)。
表观遗传编辑与基于 CRISPR 的技术
CRISPR-Cas9 技术的出现彻底改变了基因工程,其在表观遗传学中的应用也不例外。表观遗传编辑是指在不改变 DNA 序列的情况下,有针对性地修饰表观遗传标记,为研究基因调控和开发新型疗法提供了强大的工具。
CRISPR-Cas9 系统利用向导 RNA (gRNA) 将催化失活的 Cas9 (dCas9) 与表观遗传效应器结构域融合,引导至特定的基因组位点。主要效应器结构域包括 DNMT(如 DNMT3A)、DNA 去甲基酶(如 TET1)、组蛋白修饰酶(如 p300、HDAC)以及染色质重塑因子,从而实现对表观遗传修饰的精确添加或去除。
CRISPR-Cas9 技术通过靶向包括增强子和启动子在内的调控元件,实现基因表达的选择性激活或抑制,使研究人员能够直接检验特定表观遗传标记在基因调控、细胞分化和疾病中的因果作用。此外,它还可用于研究表观遗传在细胞分裂、发育过程中的遗传情况,以及由表观遗传失调驱动的疾病模型的构建。
治疗应用包括沉默致病基因(如癌基因、病毒基因)以及重新激活有益的沉默基因(如肿瘤抑制基因),适用于癌症、高胆固醇血症等疾病。这种方法有望实现高度个性化的治疗,具有最小的脱靶效应,并可应用于再生医学的细胞重编程。基于 CRISPR 的表观基因组编辑的主要优势包括高靶向精度、通过可互换效应器结构域实现的多功能性,以及与基因编辑相比更低的诱变风险。
推动该技术的发展需要研发高保真 Cas 变体并优化 gRNA 设计,以将脱靶效应降到最低。此外,多重靶向将使研究复杂的调控网络成为可能,而改进的递送方法(如病毒载体、纳米颗粒)将促进其临床转化。该领域的新兴技术包括表观基因组编辑工具,尤其是与表观遗传效应器(如 DNMT、TET、HDAC)融合的 CRISPR/dCas9 系统。其他平台包括用于特定位点靶向的 TALE549 和锌指蛋白。
单细胞表观基因组学
单细胞表观基因组技术使得可以在单个细胞水平上分析表观遗传修饰。这为揭示细胞的多样性和功能提供了前所未有的洞察,并克服了传统整体测序方法的局限,传统方法仅观察数百万细胞的平均表观遗传标记。
包括单细胞 ATAC-seq(转座酶可及染色质测序)和单细胞 ChIP-seq(染色质免疫沉淀测序)在内的技术,可在单个细胞中分析染色质可及性和组蛋白修饰,处于该趋势的前沿。应用包括绘制胚胎发育过程中的表观遗传图谱、细胞和组织分化、细胞命运决定以及免疫系统异质性。
在癌症研究中,单细胞表观基因组学可以揭示肿瘤内部的表观遗传异质性,这与克隆进化、药物耐受性和转移密切相关。该技术还用于阐明神经发育、神经退行性疾病及免疫细胞分化中的表观遗传变化,从而加深我们对自身免疫疾病和免疫疗法反应的理解。
未来方向包括与空间转录组学的整合、对细胞过程或环境刺激下表观遗传标记的时间动态分析,以及在生物标志物识别和个性化医疗方面的临床应用。
空间表观基因组学
空间表观基因组学是一项前沿技术,它将表观遗传修饰的研究与组织内的空间环境结合起来。这种方法将单细胞表观基因组学与组织学相结合,揭示表观遗传调控在组织不同区域的差异,以及其如何影响细胞的组织结构、功能和健康与疾病状态下的相互交流。
应用包括:绘制器官发生过程中由表观遗传变化指导的组织格局;识别肿瘤中空间上不同的表观遗传特征(核心区与侵袭边缘),这些特征可能驱动转移或药物耐受性;表征脑组织或特定细胞类型的区域性表观遗传变化,从而深入理解神经发育、可塑性及神经退行性疾病;解析免疫细胞微环境中的表观遗传调控;以及研究组织微环境中表观遗传状态的影响。
健康与疾病中的表观遗传学
表观遗传修饰通过激活或沉默特定基因集合,指导胚胎发育和细胞命运的决定。这些过程的失调会影响多种疾病,虽然癌症一直是研究的重点领域,但表观遗传在其他疾病中的作用也正在被探索。
癌症
遗传突变长期以来被认为是癌症的驱动因素,而如今人们也认识到,表观遗传改变在肿瘤发生中同样起着关键作用。研究布局显示癌症领域占主导地位,占出版物的 47%,这既反映了该领域的成熟度,也体现了其临床转化的成功(见图 4)。
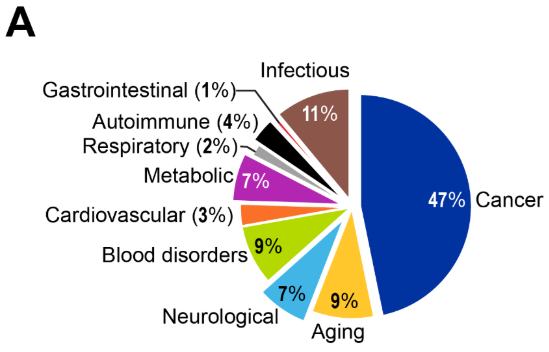

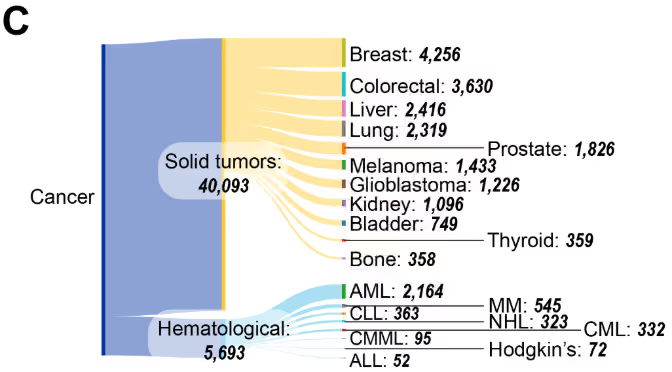
实体瘤占据了绝大多数出版物(见图 4C),其中乳腺癌、结直肠癌、肝癌和肺癌在研究活跃度方面处于领先地位。在血液系统恶性肿瘤中,急性髓系白血病 (AML) 占主导,其次是慢性淋巴细胞白血病 (CLL) 和多发性骨髓瘤 (MM)。基于 CAS 内容合集出版数据的这种分布,与美国 FDA 已批准、靶向这些恶性肿瘤的表观遗传治疗药物相一致,包括用于治疗 AML 的 azacitidine 和 decitabine,以及用于治疗皮肤 T 细胞淋巴瘤的 vorinostat。
癌症中的表观遗传调控主要涉及三种机制:
- DNA 甲基化:启动子区域的高甲基化通常会导致肿瘤抑制基因沉默,而全局性低甲基化则可能激活癌基因并促进基因组不稳定性。
- 组蛋白修饰:组蛋白乙酰化、甲基化和磷酸化的改变可以改变染色质结构和基因表达。
- 非编码 RNA (ncRNA):miRNA(如 miR-21 过表达)的失调可通过靶向肿瘤抑制基因或癌基因,促进癌症进展。
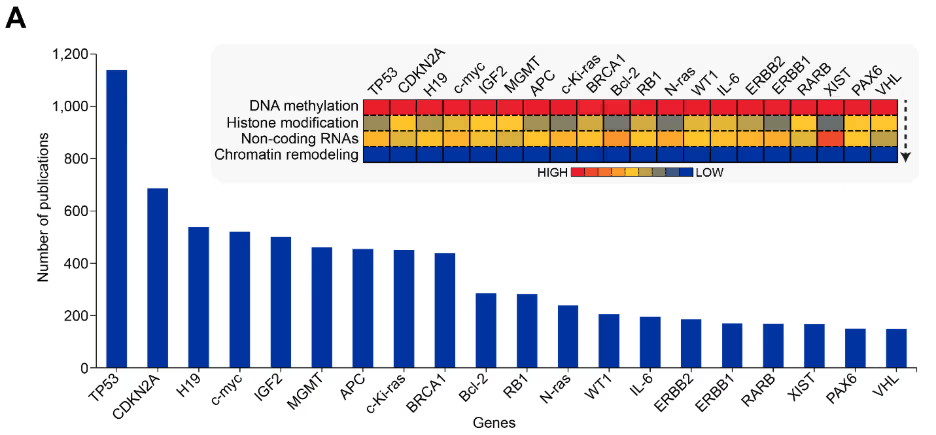
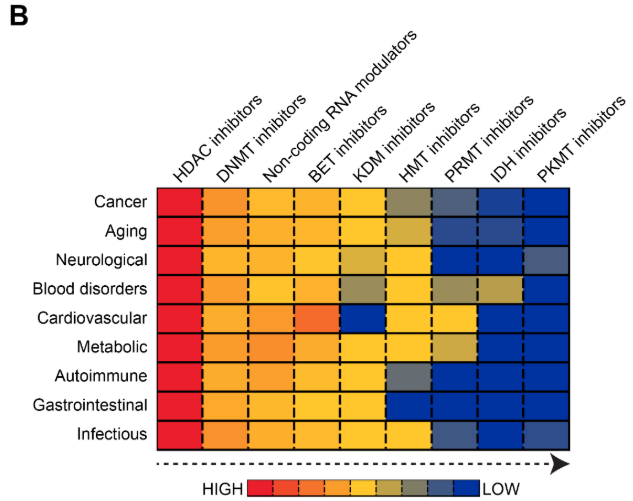
图 5 所示的基因-表观遗传机制共现热图显示了不同的模式。例如,DNA 甲基化的主导地位反映了其作为重要表观遗传机制的作用。染色质重塑在大多数基因中显示出最小的共现,表明其作用更多体现在整体结构改变,而非基因特异性调控。与 ncRNA 和组蛋白修饰相关的出版物介于两个极端,DNA 甲基化和染色质重塑之间。
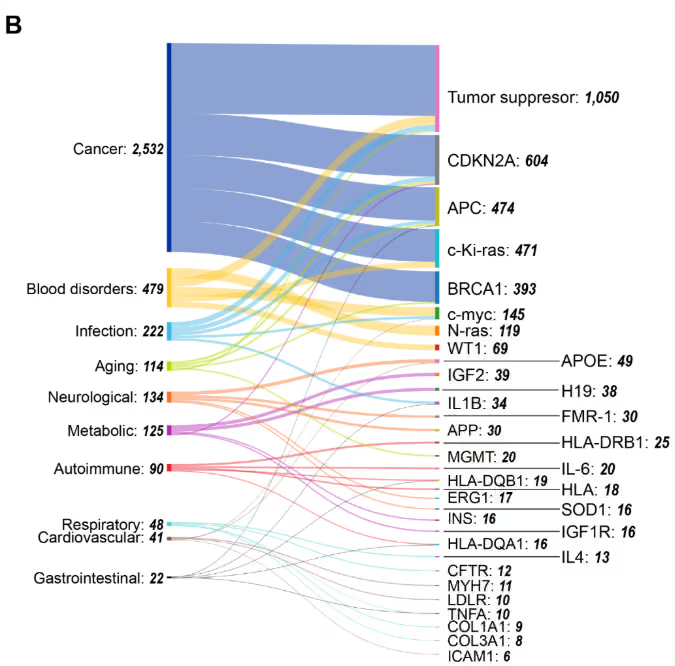
我们对基因与疾病共现关系的分析(见图 5B)表明癌症处于核心位置,其中肿瘤抑制基因显示出最高的关联度。在多种癌症中具有较高共现度的其他基因还包括 CDKN2A,其次是 APC 和 c-Ki-ras (KRAS)。这种模式反映了这些基因作为表观遗传“枢纽”的作用,它们在多种恶性肿瘤中常受到甲基化介导的沉默。
表观遗传时钟与衰老相关疾病
表观遗传时钟是一项突破性的概念,它利用计算模型根据 DNA 甲基化模式来预测生物学年龄。它们可以揭示个体生物学年龄与实际年龄之间的差异,从而为理解衰老过程以及生活方式和环境因素的影响提供线索。这些模型利用 DNA 甲基化中可预测的年龄相关变化,即特定基因组区域会以可重复的模式发生高甲基化或低甲基化。
第一代表观遗传时钟 Horvath 时钟,由 Steve Horvath 于 2013 年开发,利用来自多种组织和细胞类型的 353 个 CpG 位点的 DNA 甲基化数据来估计生物学年龄。同年开发的 Hannum 时钟主要基于血液中的 71 个 CpG 位点。更新的表观遗传时钟如 GrimAge 和 PhenoAge 融入了更多生物标志物(如血浆蛋白),以提高预测精度,并预测死亡率和疾病风险。
在长寿研究中,百岁老人和极端长寿个体通常表现出较慢的表观遗传衰老,为揭示促进健康衰老的遗传和环境因素提供了线索。当前研究正在探索通过清除衰老细胞和靶向表观遗传调控因子的化合物实现的可逆性。
图 4A 中的研究出版趋势显示,衰老在明确提及疾病与衰老的表观遗传研究中占 9%,明显低于癌症研究(47%),但从 2010 年至 2024 年呈现持续增长,尤其在 2019 年之后更为显著(见图 4B)。这一比例反映了衰老研究在以癌症应用为主导的更广泛表观遗传领域中,虽然专业化但正不断扩展的角色。
神经退行性疾病
表观遗传修饰已被发现与阿尔茨海默病、帕金森病和渐冻症 (ALS) 等神经退行性疾病,以及抑郁症和精神分裂症等心理健康障碍相关(见图 6)。大量的研究产出反映了人们对表观遗传机制在神经精神疾病和神经退行性疾病中的作用日益重视(见图 4A)。
表观遗传改变影响阿尔茨海默病中参与 β-淀粉样蛋白 (Aβ) 生成和 tau 蛋白磷酸化的基因,其中 miR-29352 和 miR-34354 等 miRNA 的失调与认知下降相关。帕金森病在参与线粒体功能的基因(如 PINK1355)以及 α-突触核蛋白聚集通路中表现出表观遗传改变。帕金森病模型中组蛋白乙酰化和 DNA 甲基化模式受到破坏,从而影响神经元的存活。
自闭症谱系障碍通过异常的 DNA 甲基化和组蛋白修饰表现出突触基因(如 SHANK3360)的失调,而环境因素如产前暴露于丙戊酸已在动物模型中显示可诱导表观遗传变化。在癫痫中,表观遗传机制调控离子通道基因和突触可塑性基因,影响癫痫发作易感性,同时观察到组蛋白修饰异常和 miRNA 失调。神经发育障碍体现了关键的表观遗传调控,例如 MECP2 基因突变(编码甲基-CpG 结合蛋白)导致 Rett 综合征,以及 Fragile X 综合征中 FMR1 基因的高甲基化。
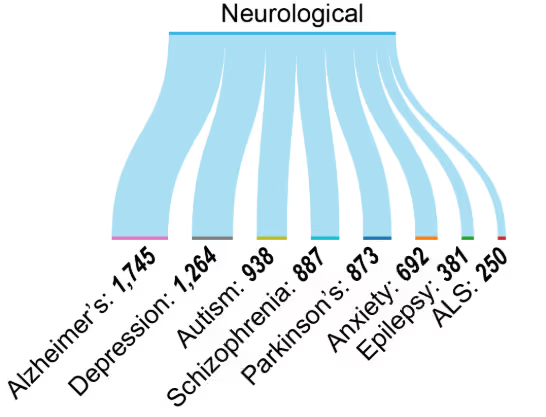
表观遗传改变越来越被认为是神经系统疾病的生物标志物。BDNF372 和 COMT374 等基因的甲基化模式与认知功能和精神疾病相关,而特定的组蛋白标记(如 H3K27me3)则与神经退行性疾病中的基因调控网络相关联。循环 miRNA,特别是 miR-132376 和 miR-124378,已显示出作为阿尔茨海默病和帕金森病诊断的无创生物标志物的潜力,为早期检测和治疗监测提供了可能。
心血管疾病
表观遗传机制在多种心血管疾病的发病中起作用,但我们对出版数据的分析显示,与癌症相比,该领域的研究兴趣占比相对较小(见图 4A)。例如,在动脉粥样硬化中,DNA 甲基化和组蛋白修饰调控参与炎症、脂质代谢和内皮功能的基因。促炎基因(如 IL-6384)的低甲基化以及抗炎基因(如 PPARγ385)的高甲基化会促进斑块形成。
调控血管张力和钠稳态的基因的表观遗传改变会促成高血压,而高盐饮食和压力等环境因素可诱导这些表观遗传变化。离子通道基因(如 SCN5A 和 KCNQ1392)的表观遗传调控可使个体易患心律失常。同样,表观遗传修饰推动病理性心脏重构,包括心肌肥厚和纤维化。DNA 甲基化、组蛋白修饰和 miRNA 是这些过程的关键调控因子。在缺血性心脏病和中风中,DNA 甲基化和组蛋白修饰改变了调控细胞存活、应激反应和炎症通路的基因表达。
与神经系统疾病类似,这些表观遗传改变也越来越多地被记录为生物标志物。F2RL3400 和 AHRR401 等基因的甲基化模式与心血管风险及预后相关。特定的组蛋白标记与心力衰竭和动脉粥样硬化中的基因调控网络相关。循环 miRNA 被用作急性心肌梗死和心力衰竭的生物标志物。
代谢紊乱
表观遗传修饰调控代谢性疾病中控制胰岛素敏感性、脂肪储存和炎症的基因。包括饮食和运动在内的环境因素会诱导持续的表观遗传改变,从而促成胰岛素抵抗和代谢功能障碍。
代谢性疾病在表观遗传学研究中占据相当比例(见图 4A),其中以肥胖研究和 2 型糖尿病研究为主。大量出版物反映了代谢性疾病的全球流行,以及人们对表观遗传对代谢功能障碍作用的日益理解。代谢表观遗传学研究虽呈稳定但温和的增长,这与神经系统疾病和血液疾病相当(见图 4B),但与癌症研究的指数级增长形成对比,表明该领域仍有巨大的潜在发展空间。
研究发现,表观遗传在以下方面发挥关键作用:
- 肥胖:DNA 甲基化和组蛋白修饰调控脂肪生成、食欲控制和能量消耗相关基因,同时 miRNA 失调与肥胖及脂肪组织功能障碍相关。DNA 甲基化和组蛋白修饰调控脂肪生成、食欲控制和能量消耗相关基因,同时 miRNA 失调与肥胖及脂肪组织功能障碍相关。
- 2 型糖尿病 (T2D):胰腺 β 细胞、肝脏和骨骼肌中的表观遗传变化影响胰岛素的产生和敏感性,包括 PPARGC1A 和 IRS1 基因的 DNA 甲基化。
- 非酒精性脂肪肝病(NAFLD): DNA甲基化和组蛋白修饰调节肝脏脂质代谢和炎症,miRNA促进疾病进展。
- 代谢综合征: 表观遗传变化影响葡萄糖代谢、脂质代谢和血压调节基因。
- 心脏代谢性疾病:表观遗传机制通过 DNA 甲基化将代谢功能失调与心血管并发症联系起来,其中包括与动脉粥样硬化和高血压风险相关的 FTO418 和 ABCA1419 基因。
代谢性疾病的表观遗传生物标志物包括与 2 型糖尿病 (T2D) 和非酒精性脂肪肝病 (NAFLD) 相关的 TXNIP 和 SREBF1 基因的甲基化模式;与代谢基因调控网络相关的特定组蛋白标记;以及作为 T2D 和肥胖生物标志物的循环 miRNA。这些生物标志物可用于代谢性疾病的早期检测、风险分层和治疗监测。
自身免疫性疾病
免疫耐受基因的异常甲基化可激活自反应性 T 细胞,导致自身免疫性疾病。尽管自身免疫性疾病具有临床重要性,但在表观遗传学研究中所占比例较小(见图 4A),从 2010 年到 2024 年的增长虽稳定但有限,相较于癌症研究的指数级增长(见图 4B)。这一研究空白表明自身免疫表观遗传学领域存在显著的扩展研究潜力。
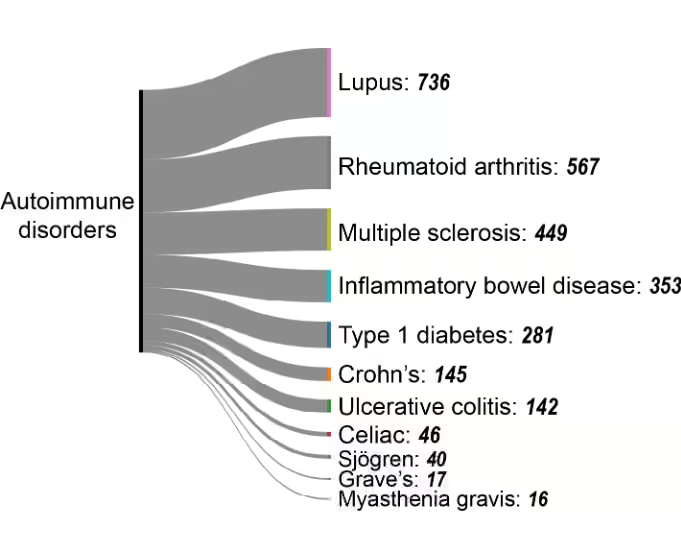
在自身免疫性疾病中,某些疾病已成为主要研究领域(见图 7):
- 系统性红斑狼疮 (SLE) 的发病机制与 miRNA 失调相关。
- 类风湿关节炎 (RA) 涉及滑膜成纤维细胞和免疫细胞中的 DNA 甲基化变化,促进关节炎症,同时组蛋白修饰调控促炎细胞因子的产生。
- 多发性硬化症 (MS)在 T 细胞和 B 细胞中表现出表观遗传变化,影响免疫调控和髓鞘破坏相关基因,同时 miRNA 失调与疾病进展相关。
- 1 型糖尿病 (T1D) 涉及胰腺 β 细胞和免疫细胞中的 DNA 甲基化和组蛋白修饰,促成胰岛素生成细胞的自身免疫性破坏,同时 miRNA(如 miR-21、miR-34a)参与其发病机制。
- 炎症性肠病 (IBD),如克罗恩病和溃疡性结肠炎,在肠上皮细胞和免疫细胞中表现出表观遗传变化,推动慢性炎症,同时与 miRNA 失调相关。
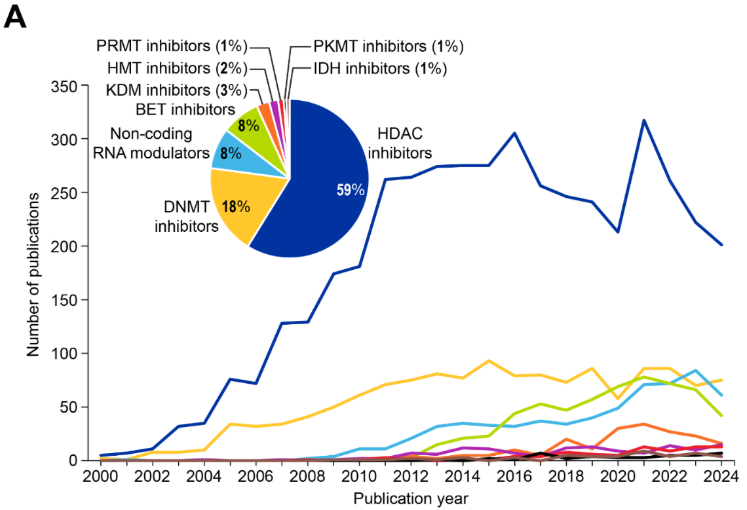
表观遗传治疗:表观遗传药物的临床应用
表观遗传药物 (epi-drugs) 可逆转异常的表观遗传修饰,从而在以表观遗传失调为特征的疾病中恢复正常的基因表达。治疗研究格局(见图 8A)显示,HDAC 抑制剂占主导地位,占出版物的 59%,其次是 DNMT 抑制剂(18%),以及 RNA 调控剂(非编码 RNA 调控剂各占 8%)。
现有表观遗传药物:
- 组蛋白去乙酰化酶 (HDAC) 抑制剂阻止组蛋白上乙酰基的去除,促进染色质结构松弛并增强基因表达,包括肿瘤抑制基因。HDAC 抑制剂还影响非组蛋白蛋白质,如转录因子和分子伴侣蛋白,进一步增强其抗癌作用。
- DNA 甲基转移酶 (DNMT) 抑制剂是相关研究出版物数量第二多的药物类别。它们通过抑制 DNMT,从而帮助重新激活在癌症中被沉默的肿瘤抑制基因。目前获批用于临床的 DNMT 抑制剂是阿扎胞苷 (Vidaza®) 和地西他滨 (Dacogen®),它们是核苷类似物,在 DNA 复制过程中掺入 DNA,不可逆地结合 DNMT,从而阻止甲基化。
- 非编码 RNA (ncRNA) 调控剂靶向 miRNA 或 lncRNA,以影响基因调控。RNA 调控剂似乎是一个快速增长的类别,尤其自 2018 年以来(见图 8A),这反映出 miRNA 和 lncRNA 被认为是精准医疗中可药物化的靶点。
- 溴结构域及附加结构域 (BET) 抑制剂阻止 BET 蛋白与乙酰化组蛋白的结合,从而干扰癌基因的转录激活。BET 蛋白(如 BRD2、BRD3、BRD4)参与识别和结合组蛋白上的乙酰化赖氨酸,并作为表观遗传标记的“读取者”。
- 组蛋白赖氨酸去甲基化酶 (KDM) 抑制剂抑制属于赖氨酸去甲基化酶 (LSD) 或含 Jumonji 结构域 (JmjC) 的 N-甲基赖氨酸去甲基化酶家族的酶。目前尚无获批的 KDM 抑制剂,但 KDM4 抑制剂 (zavondemstat) 正在进行临床试验,同时相关研究正致力于开发更多此类药物。
- 组蛋白甲基转移酶 (HMT) 抑制剂靶向在组蛋白特定赖氨酸或精氨酸残基上添加甲基的酶,这些甲基化可以根据具体的组蛋白类型和甲基化位置,激活或抑制基因表达。
- 蛋白精氨酸甲基转移酶 (PRMT) 抑制剂靶向蛋白甲基转移酶,这些酶负责向蛋白质添加甲基,并影响基因表达及细胞过程。HMT 抑制剂以及蛋白甲基转移酶抑制剂(如 PRMT 和 PKMT 抑制剂)仍处于早期开发阶段,而 KDM 抑制剂显示出新兴的治疗潜力。
- 异柠檬酸脱氢酶 (IDH) 抑制剂靶向 IDH 酶的突变形式,如 IDH1 和 IDH2,这些突变酶会产生致癌代谢物 2-羟基戊二酸。这些酶通过在细胞中积累并抑制参与表观遗传调控的酶(如 TET 蛋白和组蛋白去甲基化酶),导致 DNA 高甲基化并阻碍细胞分化。
- EZH2(Enhancer of zeste 同源物 2)抑制剂作为特定的 HMT 抑制剂,通过降低 H3K27me3 水平并重新激活沉默的肿瘤抑制基因,从而恢复正常的细胞分化并抑制肿瘤生长,尤其适用于 EZH2 突变或过表达的癌症。
- 双重作用或多表观遗传调控剂结合了作用于多条表观遗传通路的机制。这些药物可能在复杂疾病中提高治疗效果。
共现分析
表观遗传治疗的临床布局显示了监管上的成功,目前已有 13 种美国 FDA 批准的药物靶向关键表观遗传调控因子(见图 9)。
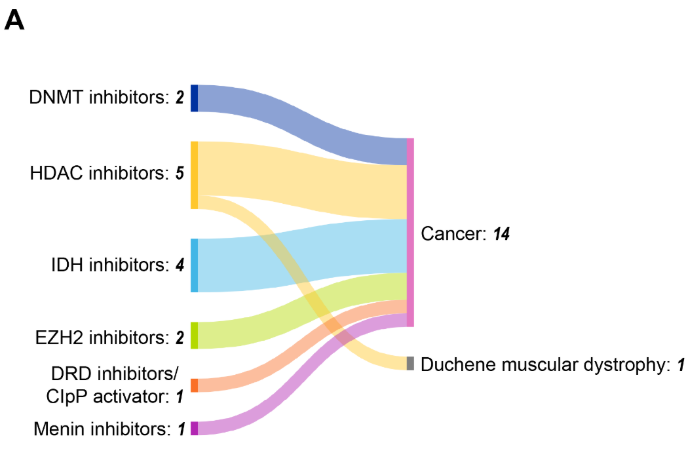
HDAC 抑制剂以五项获批位居首位,血液系统恶性肿瘤是主要治疗应用,占 15 项获批适应症中的 12 项。这种集中趋势反映了血液癌症对表观遗传失调的敏感性,以及与实体瘤相比,血液靶点更易获得。
DNA 甲基转移酶抑制剂氮杂胞苷(2004 年)与地西他滨(2006 年)是最早获批的表观遗传药物,为治疗骨髓增生异常综合征和急性髓系白血病中靶向 DNA 甲基化的理念提供了关键性概念验证。组蛋白去乙酰化酶抑制剂如伏立诺他、罗米地辛及贝利司他已在多种血液系统恶性肿瘤中展现疗效,证实了组蛋白修饰可作为有效的治疗靶点。
临床试验中的表观遗传药物
表观遗传药物的临床试验格局在过去 25 年中显著扩展,目前在 clinicaltrials.gov 上注册的试验接近 2,200 项(见图 10)。自 2000 年的单项试验起,表观遗传药物临床试验数量持续增加,到 2024 年接近每年 200 项,其中显著的波动反映了监管里程碑和市场动态。继阿扎胞苷于 2004 年获美国FDA批准后,临床试验活动呈现出起伏波动的模式,但总体保持上升趋势。这一增长模式表明,尽管存在周期性的整合阶段,制药公司仍保持持续投资。
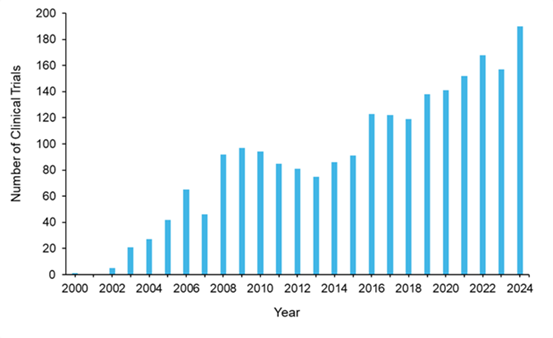
对表观遗传治疗临床试验按阶段分布的分析显示,II 期试验占主导地位,为 57%,其次是 I 期 (32%) 和 III 期 (9%)。这种分布是药物开发的典型特征,反映了表观遗传药物开发中较高的淘汰率以及许多联合用药策略的探索性特征。值得注意的是,62% 的试验涉及美国 FDA 已批准的药物,这表明在初始适应症之外,存在广泛的适应症扩展尝试和联合治疗探索。其余 38% 的临床试验针对的是更新/新型未获批准的药物。
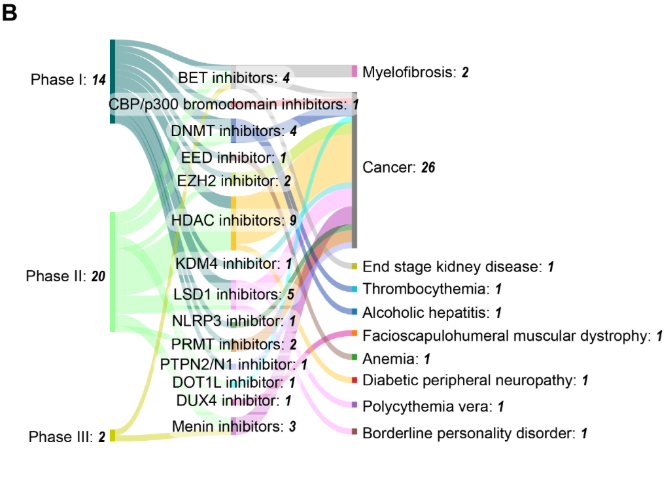
临床开发管线显示活跃态势,目前在三个阶段共有 36 项正在进行的试验。II 期试验占主导(23 项),DNMT 抑制剂和 HDAC 抑制剂在临床中保持强势地位,分别有 4 项和 11 项试验。除了 DNMT 和 HDAC 抑制剂之外,研究也在不断多样化,LSD1、BET 和 menin 抑制剂的探索日益增加(见图 9B)。这种分布既显示了对既有靶点的持续优化,也反映了向新型表观遗传调控因子的拓展。癌症应用仍占主导地位,在 36 项试验中有 26 项,但数据显示,研究正向非肿瘤性疾病拓展,包括血小板增多症、酒精性肝炎、骨髓纤维化和糖尿病周围神经病变。
临床开发中的潜力药物
在各类正在开发的药物中,有几种在癌症及其他疾病中显示出潜力:
- 肿瘤学药物:
- Pelabresib (CPI-0610)是一种先进的 BET 抑制剂,已进入骨髓纤维化的 III 期临床试验。
- Ziftomenib (KO-539) 是一种选择性小分子抑制剂,作用于 menin-KMT2A 蛋白–蛋白相互作用,于 2024 年 3 月因复发或难治性 NPM1 突变型急性髓系白血病 (AML) 获得美国 FDA 突破性疗法认定。
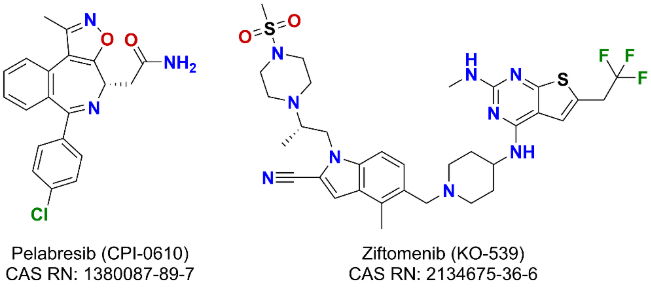
- 非肿瘤药物:
- Apabetalone (RVX-208) 是一种选择性 BET 抑制剂,靶向 BD2 结构域,目前正处于终末期肾病的 I/II 期临床试验中。
- Larsucosterol (DUR-928) 是一种内源性硫酸化氧甾醇,也是首创的表观遗传调控剂,正在进行酒精性肝炎的 II 期临床试验。
- Vafidemstat (ORY-2001) 是一种选择性 LSD1 抑制剂,目前正在进行边缘性人格障碍的 II 期临床试验。
- 近期获批药物:
- Modeyso (Dordaviprone) 于 2025 年 8 月获得美国 FDA 加速批准,用于一岁以上患者的 H3K27M 突变弥漫性中线胶质瘤。
- Revuforj (Revumenib) 于 2024 年 11 月获得美国 FDA 批准,用于成人及儿童复发/难治性 KMT2A 重排型急性髓系白血病 (AML)。
表观遗传学在个性化医疗中的应用
表观遗传数据的整合有助于开发高度精准的诊断工具、预后标志物和治疗方法,尤其针对复杂疾病。如前所述,包括 DNMT 抑制剂和 HDAC 抑制剂在内的表观遗传药物已在临床上得到应用,并仍在持续开发中。将表观遗传药物与化疗和免疫疗法相结合的联合治疗也在提高治疗效果,代表了个性化治疗方法的重要进展。
表观遗传学的另一个重要突破是将这些修饰用作组织特异性的生物标志物。这些疾病特异性模式的例子包括在癌症中肿瘤抑制基因的高甲基化,以及在阿尔茨海默病或帕金森病患者中异常的甲基化和组蛋白修饰。
识别这些表观遗传生物标志物可实现疾病的早期检测和诊断。例如,可通过液体活检检测血液或其他体液中的癌症特异性 DNA 甲基化模式,以进行无创诊断和监测;在产前检测中,通过母体血液中的表观遗传标志物评估胎儿健康。在预后方面,表观遗传标志物可预测疾病结局和治疗反应。例如,某些癌症中甲基化状态可预测疾病结局及转移可能性,而精神障碍中的表观遗传变化则可预测药物反应。
表观遗传生物标志物的临床应用
表观遗传生物标志物在疾病诊断、预后及治疗决策中具有重要作用。我们分析了 CAS 内容合集中关于表观遗传生物标志物的出版物,发现自 2008–2009 年起出现快速增长,其间经历了几个平台期(2015–2017 年和 2023–2024 年)(见图 11)。
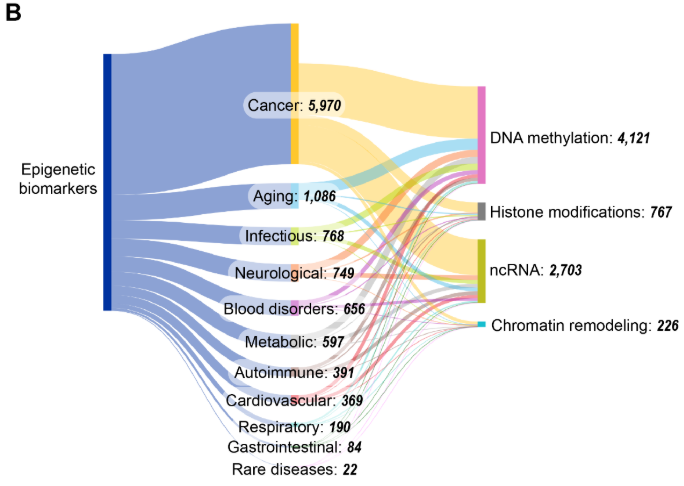
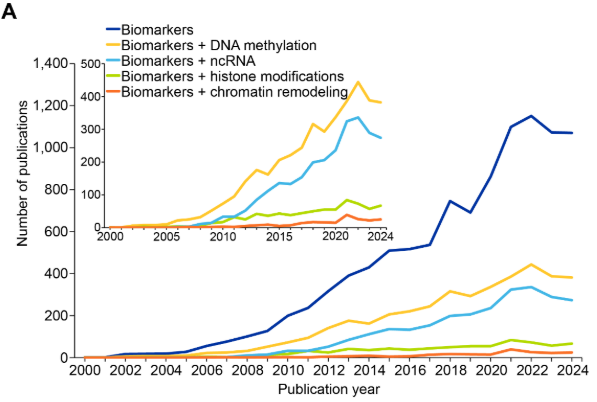
在四大表观遗传机制中,DNA 甲基化和 ncRNA 研究最为充分,与 DNA 甲基化和 ncRNA 生物标志物相关的出版物在 2015–2022 年间翻了一番,而组蛋白修饰和染色质重塑在这一领域中仍相对研究不足。如图 11B 所示,癌症与表观遗传生物标志物相关的出版物共现最多,这反映了表观遗传失调在肿瘤发生中的公认作用,以及甲基化标志物(如 MGMT516 和 VIM517)在诊断和预后中的临床价值。衰老研究的高比例与近期表观遗传时钟发展的进展及其在生物学年龄评估中的应用相一致。
DNA 甲基化生物标志物
异常的 DNA 甲基化模式可作为疾病标志,尤其是肿瘤抑制基因的高甲基化,是多种癌症的常见生物标志物。例如,SEPT9 甲基化可通过血液检测实现非侵入性结直肠癌筛查,作为结肠镜检查的替代方法。MGMT 甲基化可预测胶质母细胞瘤对替莫唑胺的反应,其中高甲基化与更好的预后相关。BRCA1 甲基化可作为诊断和预后标志物,与乳腺癌和卵巢癌的风险增加相关。值得注意的是,DNA 甲基化在表观遗传生物标志物研究中最为常见,这可能归因于其化学稳定性、成熟的检测方法以及通过 FDA 批准的检测实现的直接临床转化。
组蛋白修饰生物标志物
组蛋白修饰会影响染色质结构和基因表达,特定的组蛋白标记与疾病状态相关。如图 11B 所示,组蛋白修饰的共现情况相对较少,这表明其潜力尚未充分开发,尤其考虑到其动态特性及对治疗干预的响应能力。
组蛋白 H4 乙酰化丧失可预测某些癌症的不良预后,而组蛋白 H3 赖氨酸 27 三甲基化 (H3K27me3) 反映 PRC2 功能失调,并与前列腺癌和膀胱癌的不良预后相关。组蛋白 H3/H4 的瓜氨酸化与抗瓜氨酸化蛋白抗体 (ACPA) 的产生相关,这是类风湿关节炎的标志,可用于诊断和监测。
尽管这些发现令人鼓舞,但仍存在挑战,例如组蛋白修饰高度不稳定,易受酶促降解影响,导致样品采集后几分钟内信号迅速丧失。目前的实验方案需要含有蛋白酶、去乙酰化酶和去甲基化酶抑制剂的专用保存缓冲液,这增加了常规临床应用的复杂性。
ncRNA 生物标志物
非编码 RNA (ncRNA),包括 miRNA 如 miR-21529 和 miR-155530,在多种癌症中呈高表达,并可通过体液作为诊断和预后生物标志物。ncRNA 与表观遗传生物标志物研究的高度共现,反映了对循环 miRNA 和 lncRNA 作为微创标志物的日益关注。
例如,miR-21 高表达与乳腺癌、肺癌和结直肠癌的肿瘤生长、侵袭、转移及化疗耐药相关。miR-208a 水平升高可作为急性心肌梗死(心脏病发作)的生物标志物。HOTAIR lncRNA 高表达同样与乳腺癌、结直肠癌和胰腺癌的转移及不良预后相关。
染色质重塑生物标志物
染色质重塑模式可预测治疗耐药性,耐药癌细胞中的开放染色质区域可用于预测治疗失败。与组蛋白修饰类似,染色质重塑的共现率相对较低,这表明其潜力尚未充分开发。
总体而言,表观遗传生物标志物的未来在于开发稳健的高通量技术和综合方法。多组学整合将表观遗传组学、基因组学、转录组学和蛋白质组学数据结合起来,这将有助于生物标志物的发现与验证。在体液中对表观遗传生物标志物进行无创检测,将彻底改变早期诊断和监测方式。
先进的计算工具有望帮助识别复杂的表观遗传特征,用于患者分层。例如,基于 CRISPR 的表观基因组编辑可能实现对疾病相关表观遗传标记的干预,用于治疗目的,有可能将生物标志物从诊断工具转变为治疗工具。
表观遗传学在医学中的伦理、法律和社会影响
表观遗传学有潜力改变我们对健康与疾病的理解,但它也带来了重大的伦理、法律和社会层面的挑战。应对这些挑战需要采取一种积极且协作的方式,在发挥表观遗传学研究益处的同时,兼顾保护个人权利并促进社会公正。通过制定健全的伦理准则、法律保护措施以及公众参与策略,我们可以在最大化利用表观遗传学力量以改善健康与福祉的同时,将潜在危害降到最低。
伦理考量
- 隐私与歧视:表观遗传信息与基因数据一样,具有高度个人属性,可能揭示个体的健康状况、生活方式选择以及环境暴露等敏感信息,因此需要健全而有力的隐私保护措施。例如,用于预测疾病风险的表观遗传标志物可能会使健康保险机构提高保费或拒绝承保,从而造成歧视。同样,检测过去行为所导致的表观遗传修饰的能力,也引发了对追溯性健康评估以及就业歧视的担忧。
- 个体责任与跨代影响:相关地,表观遗传信息可能导致将健康问题归咎于个人,而忽视健康背后的更广泛社会与环境决定因素。由环境因素引起的表观遗传变化有时可能传递给后代。这引发了关于干预措施改变表观遗传标志物的长期后果的伦理担忧。
法律要求
- 监管监督:直接面向消费者的表观遗传检测套件的普及,引发了关于其准确性、结果解读以及监管的担忧。法律框架必须确保这些应用具有证据支持且符合伦理,同时防止未经验证技术的过早商业化。
- 责任与知识产权:与环境暴露相关的表观遗传修饰提出了复杂的责任问题。例如,由毒素引起的损害应由雇主、制造商还是政府负责?对于由于父母或第三方的疏忽或环境暴露而导致胎儿表观遗传损害的潜在法律责任,需要进行谨慎考虑。表观遗传学研究的商业化,例如生物标志物或疗法,也引发了关于专利与所有权的问题,需要在鼓励创新与保持公众对表观遗传技术的可及性之间取得平衡。
社会影响
- 公众理解与公平:公众对表观遗传学的有限理解容易导致误解,并可能被未经验证的疗法(如“表观遗传饮食”)所利用。全面的教育和稳健的科学传播对于解决这一问题、提升知情决策能力至关重要。将环境暴露与疾病联系起来的表观遗传研究,也可能导致对特定社区或人群的污名化,尤其是那些暴露于高污染或毒素环境中的群体。确保表观遗传疗法的公平可及性,并防止加剧健康差距,需要通过有针对性的政策干预来解决社会经济障碍。
- 实施策略:有效的治理需要为表观遗传数据的收集、使用和共享制定明确的伦理准则;更新法律框架以应对表观遗传信息的独特挑战;通过公众参与建立信任并确保知情同意;以及通过国际合作在各司法辖区之间确保标准一致。通过在推动负责任创新的同时建立健全的保护措施,社会可以利用表观遗传学的变革潜力,同时保障个人权利并促进健康公平。
表观遗传学的未来方向
表观遗传学研究的格局在过去十年中经历了显著变化,从分子生物学的一个专业领域发展为具有深远影响的人类健康和治疗干预的主流生物医学学科。表观遗传学研究的临床转化取得了显著成果,已有 15 种获得 FDA 批准的药物验证了表观遗传靶点在治疗上的可行性。目前正在进行的 36 项跨多个开发阶段的临床试验显示了对表观遗传疗法持续的投资与信心,并且研究领域正从肿瘤学扩展到代谢、神经、炎症及罕见疾病等多方面,呈现出令人鼓舞的多样化趋势。
这一转变反映出人们日益认识到,饮食、压力、毒素及生活方式选择等环境因素会引发具有跨代影响的可遗传表观遗传变化。将环境暴露数据与个体表观遗传特征整合,可实现个性化风险评估和干预策略,这标志着向预防性精准医学方法的根本性转变。
表观遗传学的未来光明,具有推动我们对生物学理解和改善人类健康的巨大潜力。然而,要实现这一潜力,需要克服诸多重大挑战,包括技术限制、伦理问题以及表观遗传调控的复杂性。通过促进跨学科合作、投资创新技术,并应对伦理与社会影响,表观遗传学领域能够持续取得突破性发现,并将其转化为有意义的临床和社会效益。