후성유전학은 DNA 염기서열의 변화 없이 유전자 발현에 나타나는 유전 가능한 변화를 연구하는 학문으로, 생물학과 의학 전반에서 중요한 전환점을 마련한 분야로 부상하며 내부 및 외부 자극에 따라 유전자 발현이 어떻게 조절되는지를 밝혀내고 있습니다. 후성유전적 조절은 발달 생물학, 질병 발생 기전, 유전자-환경 상호작용, 세대 간 유전, 치료제 개발 등 다양한 영역에서 핵심적인 역할을 합니다. 고정된 유전체를 넘어 유전자가 동적으로 조절되는 방식을 규명함으로써, 후성유전학은 유전학과 환경 요인을 연결하고 질병 메커니즘에 대한 이해와 혁신적인 치료 전략에 대한 통찰력을 제공합니다.
CAS는 사람이 직접 큐레이션한 최대 규모의 과학 정보 저장소인 CAS Content CollectionTM을 분석하여 후성유전학 연구의 진전을 정리하고 주요 신흥 개념과 과제를 도출했습니다. 이번 종합 분석은 현대 생명과학과 헬스케어에 영향을 미치는 과학적 기반, 임상 응용, 기술적 혁신을 폭넓게 살펴봅니다.
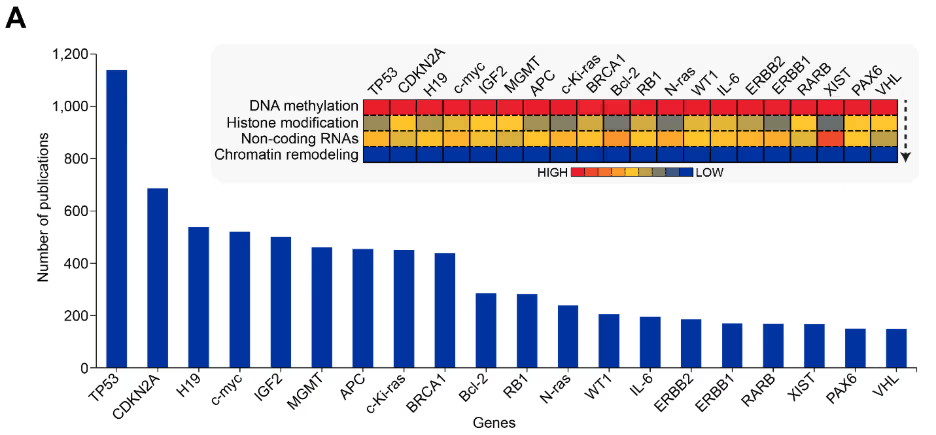
분석 결과, 지난 20년간 후성유전학 관련 간행물 수는 가파르고 지속적으로 증가했으며, 현재 CAS Content Collection에는 12만 건이 넘는 후성유전학 관련 간행물이 수록되어 있는 것으로 나타났습니다(그림 1 참조). 이 분야는 학술지 논문이 97%를 차지하고 특허는 3%에 불과해(그림 1A 참조), 후성유전학이 여전히 발견과 검증 단계에 머물러 있음을 보여줍니다.
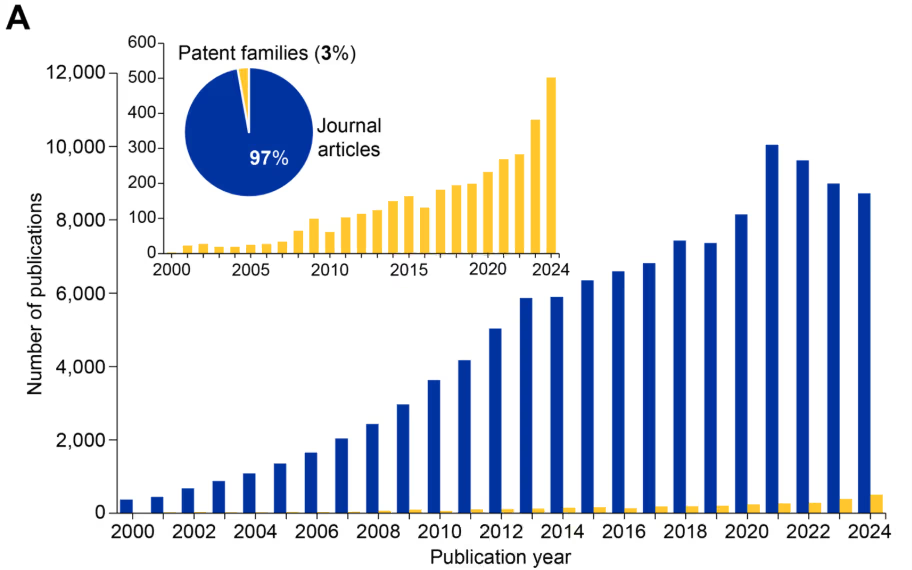


그러나 특허 간행물 수의 급격한 증가는(그림 1A 삽입 그래프 참조) 이 빠르게 발전하는 분야에서 상업적 관심과 전환 가능성이 확대되고 있음을 보여줍니다. 특히 후성유전학 관련 간행물은 2014년 이후 유전학 관련 간행물 수를 앞지르기 시작했으며(그림 1B), 에피트랜스크립토믹스는 2020년 이후 독립적인 연구 분야로 부상한 흐름이 뚜렷하게 나타납니다(그림 1B).
이러한 성장 추이는 연구비 증가와도 궤를 같이합니다. 총 연구 지원 규모는 2004년 2억 달러에서 2024년에는 45억 달러를 넘어섰으며, 연간 약 2,700개의 프로젝트를 지원하고 있습니다(그림 1C 참조). 프로젝트 수와 연구비 규모가 꾸준히 증가하고, 평균 프로젝트당 연구비가 120만 달러에서 170만 달러로 확대된 점은, 후성유전학 연구와 그 임상적 전환을 발전시키기 위한 정부 및 민간 부문의 지속적인 투자를 보여줍니다.
후성유전학의 상업적 중요성 역시 크게 확대되었습니다. 글로벌 후성유전학 시장은 2023년 기준 18억 4천만 달러 규모로 평가되었으며, 2033년에는 67억 7천만 달러에 이를 것으로 전망됩니다. 이러한 성장은 암 치료에 사용되는 아자시티딘(Vidaza®), 보리노스타트(Zolinza®)를 포함해 10종이 넘는 FDA 승인 후성유전학 치료제가 출시된 데 힘입은 결과입니다. 또한 현재 35종 이상의 후성유전학 치료제가 임상시험 단계에 있으며, 이들 후보물질은 주로 다양한 암을 표적으로 하고 있으나, 점차 암을 넘어 다른 질환 영역으로도 적용 범위를 넓혀가고 있습니다.
이제 후성유전학이 어떻게 진화하고 있으며, 이것이 미래 의학에 어떤 의미를 갖는지 보다 구체적으로 살펴보겠습니다.
후성유전 조절의 핵심 메커니즘
후성유전학적 메커니즘은 DNA 염기서열을 변경하지 않고 DNA와 염색질 구조의 화학적 변형을 통해 유전자 발현을 조절합니다. 이러한 메커니즘은 크게 네 가지 범주로 구분됩니다. DNA 메틸화, 히스톤 변형, 비암호화 RNA(ncRNA)에 의한 조절, 그리고 염색질 재구성이 이에 해당합니다. 후성유전학 관련 간행물을 분석한 결과, 초기에는 이러한 메커니즘을 직접적으로 다룬 연구가 많지 않았는데, 이는 2000년대 초반 해당 분야가 형성 단계에 있었던 점을 고려하면 자연스러운 결과입니다(그림 2 참조).
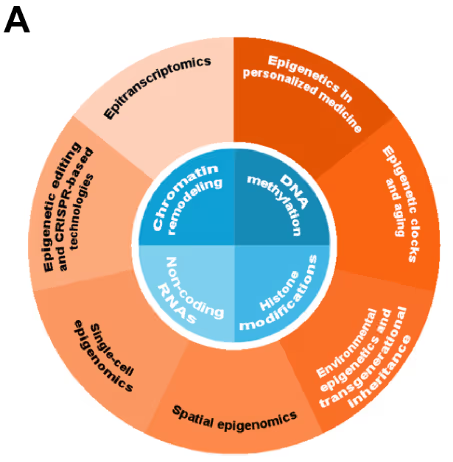

이후 네 가지 메커니즘 모두에서 연구가 가속화되었으며, 특히 DNA 메틸화는 증가 폭이 가장 커 학술지 및 특허 간행물 모두에서 연구 환경을 주도하는 영역으로 자리 잡았습니다. 다른 메커니즘들 역시 전반적으로 증가세를 보였는데, 이는 약물 개발을 위한 후성유전 표적에 대한 인식이 확대되고 있음을 시사합니다.
DNA 메틸화
DNA 메틸화는 DNA 내 CpG 이뉴클레오타이드의 시토신 고리에 메틸기(–CH₃)가 추가되는 기본적인 후성유전학적 메커니즘으로, 전사 억제를 유발합니다. 이 변형은 X 염색체 불활성화, 유전체 각인, 전이인자 억제 등에서 중요한 역할을 합니다.
DNA 메틸화는 DNA 메틸전달효소(DNMTs)에 의해 촉매됩니다. DNMT1은 복제 과정에서 기존의 메틸화 패턴을 유지하는 반면, DNMT3a/3b는 발달 과정이나 환경적 자극에 반응하여 새로운 메틸화 패턴을 형성합니다. 촉매 활성이 없는 DNMT3L은 주로 초기 발달 단계에서 발현되며, 성체에서는 생식세포와 흉선에 한정되어 발현됩니다. DNMT는 CpG 이뉴클레오타이드가 고빈도로 존재하는 CpG 섬을 표적으로 하며, 이러한 영역은 대개 유전자 프로모터 인근에 위치합니다.
비정상적인 메틸화 패턴은 암, 심혈관 질환, 정신 건강 장애, 알츠하이머병, 자폐증, 대사 증후군 등 다양한 질환에서 확인되고 있습니다. 종양 억제 유전자 프로모터의 과도한 메틸화는 해당 유전자의 발현을 억제하여 종양 형성을 촉진하는 반면, 전반적인 저메틸화는 종양 유전자의 활성화와 유전체 불안정을 유발할 수 있습니다. DNA 메틸화 패턴은 노화와 함께 변화하며, 메틸화 유지 과정에서의 오류 축적과 정확성 저하가 관찰됩니다.
히스톤 변형
히스톤 변형은 세포 분열을 통해 유전될 수 있으며, 환경적 요인의 영향을 받아 발달 과정과 질병 상태에 영향을 미칠 수 있습니다. 아세틸화, 메틸화, 인산화, 유비퀴틴화와 같은 번역 후 히스톤 변형은 염색질 구조와 유전자 접근성을 변화시킵니다. 히스톤 아세틸전달효소(HAT)와 히스톤 탈아세틸화효소(HDAC)는 히스톤에 아세틸기를 부가하거나 제거함으로써 아세틸화를 조절하며, 히스톤 메틸전달효소(HMT)와 히스톤 탈메틸화효소(HDM)는 메틸화를 조절합니다. 이러한 변형은 주로 히스톤 꼬리 부위의 라이신, 아르기닌, 세린, 트레오닌 잔기에서 일어나며, 히스톤 꼬리는 뉴클레오솜 핵심부에서 돌출되어 있어 접근성이 높은 영역입니다.
히스톤 변형은 히스톤 단백질 주위에 DNA가 포장된 구조인 염색질의 구조에 영향을 미치며, 이는 유전자 발현, DNA 복구, 유사분열 동안의 염색체 응축을 조절하는 데 관여합니다. 비정상적인 히스톤 변형은 유전자 발현 패턴을 교란하고 종양 발생과 전이에 기여할 수 있으며, 알츠하이머병, 헌팅턴병, 자폐증, 노화와 연관된 크로마틴 변화, 면역 조절 이상 등 다양한 질환과도 연관되어 있습니다.
이러한 변화는 흔히 ‘히스톤 코드’를 형성하는데, 이는 서로 다른 잔기에서의 변형 조합이 상호 상승적이거나 길항적으로 작용하여 염색질 상태를 미세하게 조절함을 의미합니다. 히스톤 변형은 염색질 구조와 유전자 발현을 조절하는 데 있어 역동적이고 유연한 시스템이며, 가역적 특성을 지니고 있어 치료적 개입의 유망한 표적으로 주목받고 있습니다.
비암호화 RNA(ncRNA)
비암호화 RNA(ncRNA)는 단백질을 암호화하지 않으면서도 유전자 발현과 염색질 역학을 조절하는 데 핵심적인 역할을 수행하는 다양한 조절 분자군으로 구성됩니다. 이러한 RNA는 메신저 RNA(mRNA)를 분해 대상으로 지정하거나 전사 체계를 조절함으로써 유전자 처리 과정을 정교하게 조율합니다.
현재 주요한 후성유전적 조절 인자로는 마이크로 RNA(miRNA), 긴 비암호화 RNA(lncRNA), 그리고 PIWI 상호작용 RNA(piRNA)의 세 가지 계열이 주목받고 있습니다. 이들 ncRNA는 다음의 다섯 가지 주요 메커니즘을 통해 후성유전적 조절을 수행합니다.
- 염색질 재구성: lncRNA는 특정 유전체 위치로 염색질 변형 복합체를 유도하여 염색질 구조와 유전자 발현에 영향을 미칩니다. 예를 들어, X 비활성화 특이 전사체(XIST)는 폴리콤 억제 복합체 2(PRC2)를 모집함으로써 X 염색체 비활성화를 매개합니다.
- 전사 조절: miRNA와 lncRNA는 전사 인자 또는 RNA 중합효소와 상호작용하여 전사 과정을 조절합니다. 예를 들어, lncRNA인 HOX 전사체 안티센스 인터젠릭 RNA(HOTAIR)는 PRC2를 모집하여 다른 염색체에 위치한 유전자의 발현을 억제합니다.
- 전사 후 조절: miRNA는 표적 메신저 RNA(mRNA)의 3′ 비번역 영역(UTR)에 결합하여 분해 또는 번역 억제를 유도합니다. lncRNA는 miRNA를 흡착하는 분자 스펀지로 작용해, miRNA가 mRNA를 표적화하는 것을 방지할 수 있습니다.
- RNA 변형: 일부 ncRNA는 RNA 메틸화(예: N6-메틸아데노신, m6A) 또는 RNA 편집을 유도하여 RNA의 안정성과 번역에 영향을 미칩니다.
- 유전체 방어: piRNA와 siRNA는 전이성 요소를 억제하여 유전체 무결성을 보호합니다. siRNA는 반복 서열이 존재하는 영역에서 이질염색질 형성을 유도할 수 있습니다.
염색질 재구성
염색질 재구성은 진정염색질(열린 구조로 전사 활성이 높은 염색질)과 이질염색질(응축되어 전사 활성이 낮은 염색질) 상태 사이에서 염색질 구조를 동적으로 조절하는 과정입니다. 염색질의 기본 단위는 DNA가 히스톤 단백질 8량체를 감싸 형성된 뉴클레오솜입니다. 염색질 재구성은 ATP 가수분해 에너지를 이용해 뉴클레오솜의 위치 이동, 제거, 또는 구조 변화를 유도하는 ATP 의존적 복합체에 의해 수행되며, 대표적으로 SWI/SNF(switch/sucrose nonfermentable), ISWI(imitation switch), CHD(chromodomain helicase DNA 결합) 계열 단백질, 그리고 INO80 계열이 이에 해당합니다.
재구성 메커니즘에는 뉴클레오솜 이동, 히스톤 제거/교환, 염색질의 응축/이완이 포함됩니다. 이러한 과정은 DNA 메틸화 및 히스톤 변형과 함께 작용하여 유전자 발현, 세포 분화, 그리고 세포 정체성 유지에 관여합니다.
염색질 재구성의 조절 이상은 암, 신경계 질환, 발달성 질환과 연관되어 있습니다. 예를 들어, SWI/SNF 복합체의 구성 요소인 ARID1A(AT-rich interaction domain 1A)와 같은 염색질 재구성 인자의 돌연변이는 다양한 악성 종양에서 빈번하게 관찰됩니다. 염색질 재구성 인자는 비정상적인 유전자 발현을 되돌릴 수 있는 유망한 치료 표적으로 주목받고 있습니다. 이러한 맥락에서 염색질 재구성은 식이, 스트레스, 독소 등 환경 요인이 유전자 발현과 건강에 미치는 영향을 매개하는 기전으로 인식되고 있습니다.
후성유전학의 최근 발전
최근 연구를 통해 DNA 메틸화, 히스톤 변형, ncRNA 조절, 염색질 재구성과 같은 후성유전학적 변형이 질병의 병인, 특히 암 발생에 어떻게 기여하는지가 점차 규명되고 있습니다. miRNA를 비롯한 다양한 ncRNA가 후성유전학적 조절자로 작용한다는 연구가 확대되면서 새로운 치료 표적이 확인되고 있으며, 개인별 후성유전학 프로파일링 기술의 발전은 맞춤형 의료 접근법의 진전을 가능하게 하고 있습니다. 출판 동향은 최근 후성유전학 연구에서 주목받는 주요 관심 분야를 보여줍니다(그림 3 참조).

환경 후성유전학
식이, 스트레스, 독소, 생활 습관과 같은 환경 요인은 앞서 논의한 다양한 기전을 통해 후성유전학적 변화를 유도할 수 있습니다. 이러한 변화는 세포 기능과 조직 항상성을 변화시켜 암, 대사 질환, 신경계 질환과 같은 질병의 발생에 기여할 수 있습니다. 주요 환경 요인의 영향은 다음과 같습니다.
- 영양소 가용성(예: 엽산, 비타민 B12)이 DNA 메틸화 패턴에 영향을 미침
- 화학 물질 노출(예: 비스페놀 A, 농약, 대기 오염 물질)이 후성유전학적 표지를 변화시켜 장기적인 건강 영향을 초래함
- 심리적·생리적 스트레스가 스트레스 반응 유전자에서 후성유전학적 변화를 유도하고 정신 건강을 조절함
- 생활 습관 요인(예: 흡연, 음주, 신체 활동 수준)이 후성유전학적 상태 조절을 통해 질병 위험에 영향을 미침
에피트랜스크립토믹스
에피트랜스크립토믹스는 RNA 분자에 일어나는 화학적 변형과, 이러한 변형이 유전자 발현 및 세포 기능을 어떻게 조절하는지를 집중해서 다루는 연구 분야입니다. 후성유전학이 DNA 염기서열 자체를 변화시키지 않으면서 DNA와 히스톤의 변형을 통해 유전자 활성이 조절되는 과정을 다루는 것처럼, 에피트랜스크립토믹스는 RNA 변형이 RNA의 안정성, 번역, 스플라이싱 등 다양한 과정에 미치는 영향을 규명합니다.
현재까지 mRNA, tRNA, rRNA, ncRNA에 걸쳐 170종 이상의 서로 다른 RNA 변형이 확인되었으며, 이 가운데 N6-메틸아데노신(m6A)은 진핵생물 mRNA에서 가장 풍부하고 가장 광범위하게 연구된 변형입니다. 주요 RNA 변형에는 다음과 같은 것들이 포함됩니다. m6A는 아데노신의 N6 위치에서 일어나는 메틸화로, mRNA의 안정성, 스플라이싱, 핵외 수송 및 번역 조절에 영향을 미칩니다. 또한 mRNA와 tRNA에서 시토신의 N5 위치에 발생하는 m5C 메틸화는 RNA 안정성과 번역에 관여하며, 유리딘의 이성질체인 슈도유리딘(Ψ)은 RNA의 구조적 안정성과 번역 효율을 향상시킵니다. 이와 함께 아데노신에서 이노신으로의 탈아미노화는 염기쌍 형성 특성을 변화시켜 스플라이싱 과정과 단백질 암호화에 영향을 미칩니다.
에피트랜스크립토믹스 조절 체계는 크게 세 가지 단백질 군으로 구성됩니다.
- Writer: 변형을 추가하는 효소(예: m6A 메틸화를 위한 METTL3/METTL14 복합체)
- Erasers: 변형을 제거하는 효소(예: m6A 탈메틸화를 위한 fat mass- and obesity-associated protein(FTO) 및 alkB homolog 5, RNA demethylase(ALKBH5)).
- Readers: 변형된 RNA를 인식하고 결합하는 단백질(예: m6A 인식을 위한 YTH 도메인 단백질). 이들은 함께 RNA 변형의 동적 조절을 담당합니다.
RNA 변형은 다양한 세포 과정 조절에 관여하며, 이러한 조절이 교란될 경우 여러 질병을 유발합니다. 암에서는 m6A 변형은 종종 변화하며 이는 종양 진행, 전이, 약물 내성과 관련이 있습니다. 비정상적인 RNA 편집 및 변형은 알츠하이머병, 파킨슨병, ALS와 같은 신경퇴행성 질환과도 관련이 있습니다. 또한, HIV와 SARS-CoV-2를 포함한 RNA 바이러스는 숙주의 RNA 변형 조절 체계를 활용해 바이러스 복제와 면역 회피를 조절하는 것으로 알려져 있으며, 이 과정에는 후성유전학적 조절 기전도 관여합니다.
고처리량 시퀀싱 기술은 RNA 변형을 전장 수준에서 매핑할 수 있게 해 주며, 여기에 질량분석법과 화학적 표지 기법이 결합되어 RNA 변형의 검출과 정량을 가능하게 합니다. 이러한 발전은 RNA 변형 효소를 표적으로 하는 치료제 개발을 촉진하고 있습니다.
RNA 변형 조절 체계의 구성 요소(writer, eraser, reader)를 표적으로 하는 치료 전략도 질환 치료를 위한 접근법으로 검토되고 있습니다. 예를 들어, m6A 탈메틸효소인 FTO 억제제는 항암 치료에서 가능성을 보여주고 있으며, mRNA 백신에 사용되는 변형 뉴클레오타이드는 RNA 안정성과 번역 효율을 향상시키는 역할을 합니다.
전반적으로 현재 연구는 ‘에피트랜스크립톰 코드’를 해독하고, RNA 변형을 생체 내에서 정밀하게 조절할 수 있는 도구를 개발하며, ncRNA에서의 변형을 탐구하는 데 초점을 맞추고 있습니다. 단일 세포 에피트랜스크립토믹스는 세포 유형별 RNA 변형 패턴과 그에 따른 기능적 결과를 밝혀내고 있습니다. 또한 새롭게 부상하는 기술인 멀티오믹스 통합은 CUT&RUN, Hi-C 통합과 같은 기술을 활용해 후성유전체 데이터와 전사체학, 단백질체학, 대사체학 데이터를 결합함으로써 세포 기능을 보다 총체적으로 이해할 수 있게 합니다. 이러한 접근법은 복잡한 질환에서 포괄적인 경로 분석과 바이오마커 발굴을 가능하게 합니다.
세대 간 유전
세대 간 유전이란 DNA 염기서열 변화와는 무관하게 환경적 요인에 의해 유도된 후성유전학적 변화가 여러 세대에 걸쳐 전달되는 현상을 의미합니다. 이러한 현상은 식물과 동물에서 관찰되어 왔으며, 한 세대가 경험한 환경적 노출이 후대의 건강과 발달에 영향을 미칠 수 있음을 시사합니다. 다만, 인간에서 이 과정의 범위와 중요성을 명확히 입증하는 것은 여전히 어려운 과제로 남아 있습니다.
세대 간 후성유전학적 유전의 대표적인 사례로는 네덜란드 기근(Dutch Hunger Winter, 1944~1945)이 있습니다. 당시 네덜란드에서 기아를 경험한 개인들의 후손에서 DNA 메틸화 패턴의 변화와 대사 질환 위험 증가가 관찰되었습니다. 동물 연구에서도 내분비계 교란 물질(예: 빈클로졸린)에 노출된 경우, 생식, 행동, 질병 감수성에 이르는 세대 간 영향이 보고되었습니다. 인간의 경우에는 부계 흡연이나 모계 스트레스가 자손의 후성유전학적 변화와 관련이 있는 것으로 나타났습니다.
세대 간 후성유전학적 유전의 기전은 아직 완전히 규명되지 않았습니다. 그러나 이러한 변화가 비만, 당뇨병, 심혈관 질환과 같은 질환의 위험을 노출된 개인의 후손에서 높일 수 있다는 점에서, 이 분야는 현재 활발한 연구가 이루어지고 있습니다. 세대 간 유전의 영향에 대한 이해는 특히 임신과 같은 중요한 발달 기간 동안 유해한 환경 요인에 대한 노출을 줄이기 위한 정책 수립에도 중요한 근거를 제공할 수 있습니다.
후성유전학적 편집과 CRISPR 기반 기술
CRISPR-Cas9 기술의 등장은 유전공학 분야에 혁신을 가져왔으며, 후성유전학에의 적용 역시 예외가 아닙니다. 후성유전학적 편집은 DNA 염기서열을 변경하지 않고 특정 후성유전학적 표지를 표적화해 수정하는 접근법으로, 유전자 발현 조절을 연구하고 새로운 치료법을 개발하는 데 강력한 도구를 제공합니다.
CRISPR-Cas9 시스템은 가이드 RNA(gRNA)를 이용해 촉매 활성이 없는 Cas9(dCas9)을 특정 유전체 위치로 유도하며, 이 dCas9에는 후성유전학적 이펙터 도메인이 결합됩니다. 주요 이펙터 도메인에는 DNMT(예: DNMT3A), DNA 탈메틸화 효소(예: TET1), 히스톤 변형 효소(예: p300, HDACs), 염색질 재구성 인자가 포함되며, 이를 통해 후성유전학적 변형을 정밀하게 추가하거나 제거할 수 있습니다.
CRISPR-Cas9 기술은 인핸서와 프로모터를 포함한 조절 요소를 표적화함으로써 유전자 발현을 선택적으로 활성화하거나 억제할 수 있게 합니다. 이를 통해 연구자들은 특정 후성유전학적 표지가 유전자 조절, 세포 분화, 질환 발생에서 수행하는 인과적 역할을 직접 검증할 수 있습니다. 또한 이러한 기술은 세포 분열과 발달 과정은 물론, 후성유전학적 조절 이상에 의해 유도되는 질환 모델의 생성에 이르기까지 전반적인 후성유전학적 유전 양상을 분석하는 데에도 활용할 수 있습니다.
치료적 응용으로는 암이나 고콜레스테롤혈증 등에서 질병 유발 유전자(온코진, 바이러스 유전자)를 침묵시키거나 유익하지만 억제된 유전자(종양 억제 유전자)를 다시 활성화하는 접근이 포함됩니다. 이러한 방식은 비의도적 표적 효과를 최소화한 고도로 개인화된 치료 가능성을 제공하며, 재생의학을 위한 세포 재프로그래밍에도 적용될 수 있습니다. CRISPR 기반 후성유전체 편집의 주요 장점으로는 높은 표적 정확성, 이펙터 도메인을 교체할 수 있는 유연성, 그리고 유전자 편집에 비해 낮은 돌연변이 위험이 포함됩니다.
이 기술을 더욱 발전시키기 위해서는 비의도적 표적 효과를 최소화할 수 있는 고정밀 Cas 변이체와 최적화된 gRNA 설계가 필요합니다. 또한 다중 표적화는 복잡한 조절 네트워크를 규명하는 데 기여할 수 있으며, 바이러스 벡터나 나노입자와 같은 전달 기술의 개선은 임상 적용을 촉진할 것입니다. 이 분야의 새로운 기술로는 DNMT, TET, HDAC와 같은 후성유전학적 이펙터를 결합한 CRISPR/dCas9 기반 후성유전체 편집 도구가 있습니다. 대안 플랫폼으로는 특정 유전체 위치를 표적화할 수 있는 TALE549 및 아연 핑거 단백질이 포함됩니다.
단일 세포 후성유전체학
단일 세포 후성유전체학 기술은 개별 세포 수준에서 후성유전적 변화를 분석할 수 있게 해줍니다. 이는 세포의 다양성과 기능에 대한 전례 없는 통찰력을 제공하고, 수백만 개의 세포에서 평균적인 후성 유전 표지를 분석하는 기존의 벌크 시퀀싱 방식이 갖는 한계를 극복할 수 있게 합니다.
단일 세포 ATAC-seq(시퀀싱을 이용한 전이효소 접근 염색질 분석)와 단일 세포 ChIP-seq(염색질 면역침강 시퀀싱)와 같은 기법은 개별 세포에서의 염색질 접근성 및 히스톤 변형을 분석할 수 있어, 이 분야를 이끄는 핵심 기술로 자리 잡고 있습니다. 이러한 기술은 배아 발생 과정에서의 후성유전적 지형을 매핑하고, 세포 및 조직 분화, 세포 운명 결정, 면역계 이질성을 규명하는 데 활용되고 있습니다.
암 연구 분야에서는 단일 세포 후성유전체학을 통해 종양 내 후성유전적 이질성을 규명할 수 있으며, 이는 클론 진화, 약물 내성, 전이와 같은 현상과 밀접하게 연관되어 있습니다. 또한 이 기술은 신경 발달, 신경 퇴행, 면역 세포 분화에서의 후성유전적 변화를 규명하는 데에도 활용되어 자가면역 질환과 면역치료 반응에 대한 이해를 넓히는 데 기여하고 있습니다.
향후 연구 방향으로는 공간 전사체학과의 통합, 세포 과정이나 환경 자극에 따른 후성유전 표지의 시간적 변화 분석, 그리고 바이오마커 식별과 개인 맞춤형 의료를 위한 임상 적용 등이 포함됩니다.
공간 후성유전체학
공간 후성유전체학은 조직 내 후성유전적 변형의 연구를 공간적 맥락과 결합하는 최첨단 기술입니다. 이 접근 방식은 단일 세포 후성유전체학과 조직학을 연결하여 건강 및 질병 상태에서 후성유전적 조절이 조직의 서로 다른 영역에서 어떻게 달라지고, 그 결과가 세포 조직화, 기능, 세포 간 상호작용에 어떤 영향을 미치는지를 규명합니다.
이 기술의 활용 사례로는 후성유전적 변화에 의해 유도되는 기관 형성 과정에서의 조직 패턴 매핑, 종양 내에서 공간적으로 구분되는 후성유전적 서명(예: 종양 중심부와 침윤 경계부)의 규명과 이를 통한 전이 또는 약물 내성 기전 이해, 뇌 조직이나 특정 세포 유형에서의 영역 특이적 후성유전 변화 분석을 통한 신경 발달, 가소성, 신경 퇴행성 질환에 대한 통찰 확보가 있습니다. 또한 면역 세포 니치 전반에서의 후성유전 조절 양상과 조직 미세환경 내에서 후성유전 상태가 미치는 영향에 대한 이해에도 활용되고 있습니다.
건강과 질병에서의 후성유전학
후성유전적 변형은 특정 유전자 집합을 활성화하거나 억제함으로써 배아 발달과 세포 운명 결정 과정을 조절합니다. 이러한 조절 과정이 교란되면 다양한 병리적 상태로 이어질 수 있으며, 지금까지는 암이 가장 활발히 연구된 질환 영역이었지만 최근에는 다른 질환에서의 후성유전학적 역할에 대한 연구도 확대되고 있습니다.
암
유전적 돌연변이가 암의 주요 원인으로 오랫동안 인식되어 왔지만, 최근에는 후성유전적 변화 역시 종양 형성 과정에서 그에 못지않게 중요한 역할을 한다는 점이 밝혀지고 있습니다. 연구 동향을 살펴보면, 전체 후성유전학 관련 간행물의 47%가 암을 대상으로 하고 있어(그림 4 참조), 해당 분야의 성숙도와 임상 적용 성과를 반영하고 있습니다.
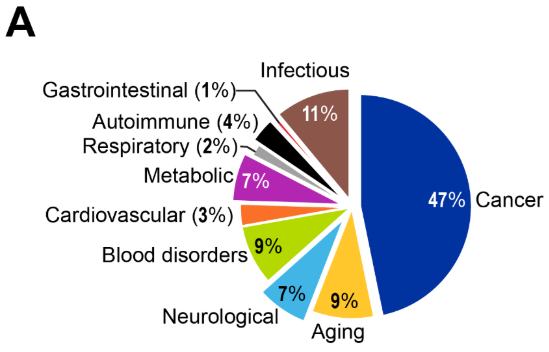

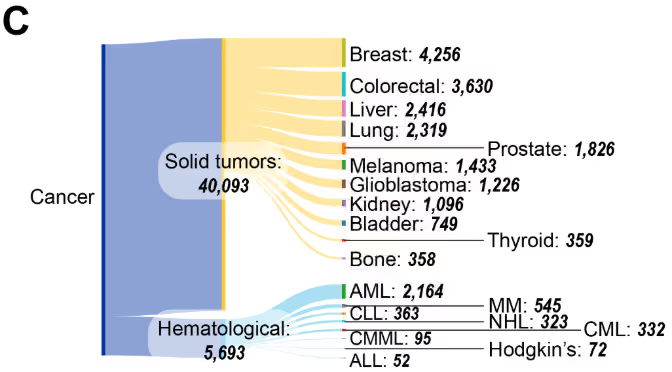
고형종양은 간행물의 압도적 다수를 차지하며(그림 4C), 유방암, 대장암, 간암, 폐암이 연구 활동 측면에서 두드러집니다. 혈액암 중에서는 급성 골수성 백혈병(AML)이 가장 많은 비중을 차지하고, 그 뒤를 만성 림프구성 백혈병(CLL)과 다발성 골수종(MM)이 잇고 있습니다. 이러한 분포는 CAS Content Collection의 출판 데이터를 기반으로 한 결과이며, AML 치료에 사용되는 아자시티딘과 데시타빈, 피부 T세포 림프종 치료에 사용되는 보리노스타트 등 미국 FDA 승인 후성유전 치료제의 적용 대상과도 일치합니다.
암에서의 후성유전적 조절은 주로 세 가지 기전을 통해 이루어집니다.
- DNA 메틸화: 프로모터 영역의 과도한 메틸화는 종양 억제 유전자의 발현을 억제하는 반면, 전반적인 저메틸화는 종양유전자를 활성화하고 유전체 불안정성을 촉진할 수 있습니다.
- 히스톤 변형: 히스톤의 아세틸화, 메틸화, 인산화 변화는 염색질 구조와 유전자 발현을 변화시킵니다.
- ncRNA: miRNA의 발현 이상(예: miR-21 과발현)은 종양 억제 유전자 또는 종양유전자를 표적으로 삼아 암 진행을 촉진할 수 있습니다.
그림 5에 제시된 유전자-후성유전 기전 동시 언급 히트맵은 뚜렷한 패턴을 보여줍니다. 예를 들어, DNA 메틸화가 가장 두드러지게 나타나는 것은 이 기전이 중요한 후성유전 조절 메커니즘임을 반영합니다. 반면 염색질 재구성은 대부분의 유전자에서 동시 언급 빈도가 낮아, 개별 유전자 조절보다는 보다 광범위한 구조적 변화에 관여함을 시사합니다. ncRNA와 히스톤 변형과 관련된 간행물은 DNA 메틸화와 염색질 재구성의 중간 수준에 위치합니다.
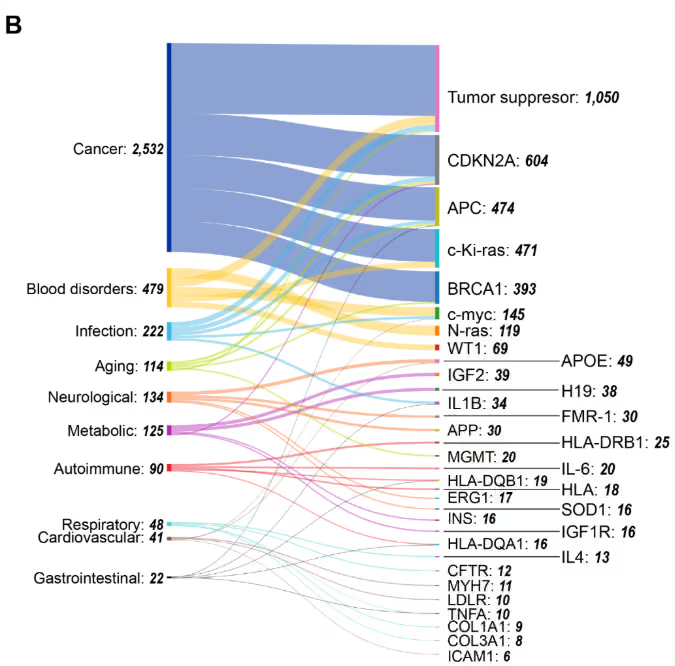
유전자와 질환 간 동시 언급 분석 결과(그림 5B), 암이 중심적인 위치를 차지하며 종양 억제 유전자들이 가장 높은 연결성을 보였습니다. 여러 암 유형에서 높은 동시 언급을 보이는 다른 유전자로는 CDKN2A가 있으며, 그 뒤를 APC와 c-Ki-ras(KRAS)325가 잇고 있습니다. 이러한 패턴은 해당 유전자들이 다양한 악성 종양에서 메틸화에 의해 발현이 억제되는 후성유전적 허브로 작용함을 반영합니다.
후성유전학적 시계와 노화 관련 질환
후성유전학적 시계는 DNA 메틸화 패턴을 기반으로 생물학적 나이를 예측하는 계산 모델을 활용한 획기적인 개념입니다. 이 시계는 개인의 생물학적 나이와 연대기적 나이 사이의 차이를 드러내며, 노화 과정과 생활 습관 및 환경 요인이 미치는 영향을 이해하는 데 중요한 통찰을 제공합니다. 이러한 모델은 특정 유전체 영역이 재현 가능한 방식으로 과메틸화되거나 저메틸화되는, 나이에 따른 예측 가능한 DNA 메틸화 변화를 활용합니다.
1세대 후성유전학적 시계인 Horvath 시계는 2013년 Steve Horvath에 의해 개발되었으며, 여러 조직과 세포 유형에 걸친 353개의 CpG 부위 DNA 메틸화 데이터를 사용해 생물학적 나이를 추정합니다. 같은 해 개발된 Hannum 시계는 주로 혈액에서 측정한 71개의 CpG 부위를 활용합니다. 보다 최근에 제안된 GrimAge와 PhenoAge와 같은 시계는 추가적인 생체표지자(예: 혈장 단백질)를 통합해 예측 정확도를 높이고, 사망 위험과 질병 위험을 예측하는 데까지 확장되었습니다.
장수 연구에서는 100세 이상 장수하는 사람들과 예외적으로 긴 수명을 보이는 개인들이 대체로 후성유전학적 노화 속도가 더 느리게 진행되는 특징을 보이며, 이는 건강한 노화를 촉진하는 유전적·환경적 요인에 대한 단서를 제공합니다 현재 연구에서는 세놀리틱이나 후성유전 조절 인자를 표적으로 하는 화합물을 통해 이러한 변화가 가역적인지 여부도 탐구하고 있습니다.
그림 4A에 제시된 연구 간행물 동향에 따르면, 노화는 질환과 노화를 명시적으로 언급한 후성유전학 연구의 약 9%를 차지하며, 이는 암 연구(47%)에 비해 비중은 작지만 2010년부터 2024년까지 꾸준한 증가세를 보이고 있으며, 특히 2019년 이후 그 증가가 두드러집니다(그림 4B). 이러한 비율은 암 중심의 응용이 주를 이루는 후성유전학 연구 전반 속에서 노화 연구가 전문화되어 있으면서도 점차 확대되고 있는 영역임을 보여줍니다.
신경퇴행성 질환
후성유전학적 변형은 알츠하이머병, 파킨슨병, ALS와 같은 신경퇴행성 질환뿐 아니라, 우울증과 조현병과 같은 정신질환과도 연관되어 있습니다(그림 6). 방대한 연구 성과는 신경정신질환 및 신경퇴행성 병태에서 후성유전학적 기전에 대한 인식이 점차 확대되고 있음을 보여줍니다(그림 4A 참조).
알츠하이머병에서는 아밀로이드 베타(Aβ) 생성과 타우 단백질 인산화에 관여하는 유전자들이 후성유전학적 변형의 영향을 받으며, miR-29352 및 miR-34354와 같은 miRNA의 조절 이상은 인지 기능 저하와 연관이 있습니다. 파킨슨병의 경우, 미토콘드리아 기능 관련 유전자(예: PINK1355)와 α-시누클레인 응집 경로에서 후성유전학적 변화가 관찰됩니다. 또한 파킨슨병 모델에서는 히스톤 아세틸화와 DNA 메틸화 패턴이 교란되어 신경세포 생존에 영향을 미칩니다.
자폐 스펙트럼 장애에서는 비정상적인 DNA 메틸화와 히스톤 변형을 통해 시냅스 관련 유전자(예: SHANK3360)의 조절 이상이 관찰되며, 동물 모델에서는 임신 중 발프로산 노출과 같은 환경 요인이 후성유전학적 변화를 유도하는 것으로 나타났습니다. 간질에서는 후성유전학적 기전이 이온 채널 유전자와 시냅스 가소성 관련 유전자를 조절함으로써 발작 감수성에 기여하며, 히스톤 변형과 miRNA 조절 이상이 함께 관찰됩니다. 이러한 신경발달 장애는 후성유전학적 조절의 중요성을 잘 보여주는데, 예를 들어 메틸-CpG 결합 단백질을 암호화하는 MECP2 유전자의 돌연변이는 레트 증후군을 유발하며 FMR1 유전자의 과메틸화는 취약 X 증후군과 연관되어 있습니다.
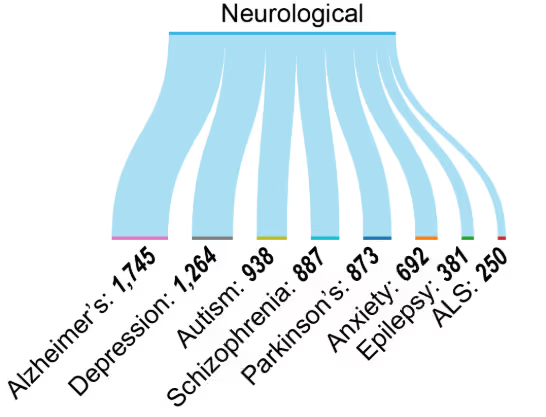
후성유전학적 변형은 신경계 질환의 바이오마커로서도 점차 주목받고 있습니다. BDNF372 및 COMT374와 같은 유전자의 메틸화 패턴은 인지 기능 및 정신질환과 연관되어 있으며, 특정 히스톤 표지(예: H3K27me3)는 신경퇴행 과정에서 유전자 조절 네트워크와 연결되어 있습니다. 순환 miRNA, 특히 miR-132376과 miR-124378은 각각 알츠하이머병과 파킨슨병의 비침습적 진단 바이오마커로서 잠재력을 보여주고 있어, 조기 진단 및 치료 모니터링에 활용될 가능성을 시사합니다.
심혈관 질환
후성유전학적 기전은 다양한 심혈관 질환의 병태생리에 기여하지만, 간행물 데이터 분석에 따르면 해당 분야에 대한 연구 관심도는 암에 비해 상대적으로 낮은 것으로 나타납니다(그림 4A 참조). 예를 들어, 죽상동맥경화증에서는 DNA 메틸화와 히스톤 변형이 염증, 지질 대사, 내피 기능에 관여하는 유전자들을 조절합니다. 친염증성 유전자(예: IL-6384)의 저메틸화와 항염증성 유전자(예: PPARγ385)의 고메틸화는 플라크 형성을 촉진합니다.
혈관 긴장도와 나트륨 항상성을 조절하는 유전자에서 발생하는 후성유전학적 변화는 고혈압 발생에 기여하며, 고염식이나 스트레스와 같은 환경 요인은 이러한 후성유전학적 변화를 유도할 수 있습니다. 이온 채널 유전자(예: SCN5A, KCNQ1392)에 대한 후성유전학적 조절은 부정맥 발생 소인을 높일 수 있습니다. 이와 유사하게, 후성유전학적 변형은 심근 비대와 섬유화를 포함한 병리적 심장 리모델링을 유도합니다. 이러한 과정에서 DNA 메틸화, 히스톤 변형, miRNA는 핵심적인 조절 인자로 작용합니다. 허혈성 심장 질환과 뇌졸중에서는 DNA 메틸화와 히스톤 변형이 세포 생존, 스트레스 반응, 염증 경로를 조절하는 유전자 발현을 변화시킵니다.
신경계 질환의 경우와 마찬가지로, 이러한 변화는 점차 바이오마커로 활용되고 있습니다. F2RL3400 및 AHRR401과 같은 유전자의 메틸화 패턴은 심혈관 위험도와 임상 결과와 연관되어 있으며, 특정 히스톤 표지는 심부전과 죽상동맥경화증에서의 유전자 조절 네트워크와 연결됩니다. 또한 순환 miRNA는 급성 심근경색과 심부전에 대한 바이오마커로 활용되고 있습니다.
대사 장애
후성유전학적 변형은 대사 질환에서 인슐린 감수성, 지방 저장, 염증을 조절하는 유전자의 발현을 조절합니다. 식이와 운동을 포함한 환경적 요인은 지속적인 후성유전학적 변화를 유도하며, 이는 인슐린 저항성과 대사 기능 장애에 기여합니다.
대사 질환은 후성유전학 연구에서 상당한 비중을 차지하고 있으며(그림 4A 참조), 이 가운데 비만과 제2형 당뇨병 연구가 주를 이룹니다. 간행물 규모가 큰 것은 전 세계적인 대사 질환 유행과 대사 기능 장애에 대한 후성유전학적 기여에 대한 이해가 확대되고 있음을 반영합니다. 대사 후성유전학 연구는 꾸준하지만 완만한 증가세를 보이며, 이는 신경계 질환 및 혈액 질환 분야와 유사한 수준입니다(그림 4B). 반면 암 연구에서 나타나는 기하급수적인 증가와는 대비되며, 이 영역에 아직 상당한 미개척 잠재력이 있음을 시사합니다.
후성유전학은 다음과 같은 질환에서 핵심적인 역할을 하는 것으로 확인되었습니다.
- 비만: DNA 메틸화와 히스톤 변형이 지방세포 분화, 식욕 조절, 에너지 소비 관련 유전자를 조절하며, 조절 이상 miRNA가 비만 및 지방 조직 기능 장애와 연관됩니다. DNA 메틸화와 히스톤 변형이 지방세포 분화, 식욕 조절, 에너지 소비 관련 유전자를 조절하며, 조절 이상 miRNA가 비만 및 지방 조직 기능 장애와 연관됩니다.
- 제2형 당뇨병 (T2D): 췌장 β 세포, 간, 골격근에서의 후성유전학적 변화가 인슐린 생성과 감수성에 영향을 미치며, PPARGC1A 및 IRS1 유전자의 DNA 메틸화가 포함됩니다.
- 비알코올성 지방간 질환(NAFLD): DNA 메틸화와 히스톤 변형이 간 지질 대사와 염증을 조절하고, miRNA가 질환 진행에 기여합니다.
- 대사 증후군: 후성유전학적 변화가 포도당 대사, 지질 대사, 혈압 조절 관련 유전자에 영향을 미칩니다.
- 심대사 질환: 후성유전학적 기전이 대사 이상과 심혈관 합병증을 연결하며, FTO418 및 ABCA1419 등 동맥경화와 고혈압 위험과 연관된 유전자의 DNA 메틸화가 포함됩니다.
대사 질환을 위한 후성유전학적 바이오마커로는 제2형 당뇨병과 NAFLD와 연관된 TXNIP 및 SREBF1 유전자의 메틸화 패턴, 대사 유전자 조절 네트워크와 연관된 특정 히스톤 표지, 그리고 제2형 당뇨병과 비만의 바이오마커로 활용되는 순환 miRNA가 포함됩니다. 이러한 바이오마커는 대사 질환에서 조기 진단, 위험도 층화, 치료 모니터링을 가능하게 합니다.
자가면역 질환
면역 관용 관련 유전자의 비정상적인 메틸화는 자가 반응성 T 세포를 활성화시켜 자가면역 질환을 유발할 수 있습니다. 임상적 중요성에도 불구하고, 자가면역 질환은 후성유전학 연구에서 차지하는 비중이 비교적 낮으며(그림 4A 참조) 2010년부터 2024년까지 완만하지만 제한적인 증가세를 보였습니다. 이는 암 연구에서 나타나는 기하급수적인 증가와 대비됩니다(그림 4B). 이러한 연구 격차는 자가면역 후성유전학 분야에서 추가적인 연구 확장의 잠재력이 크다는 것을 시사합니다.
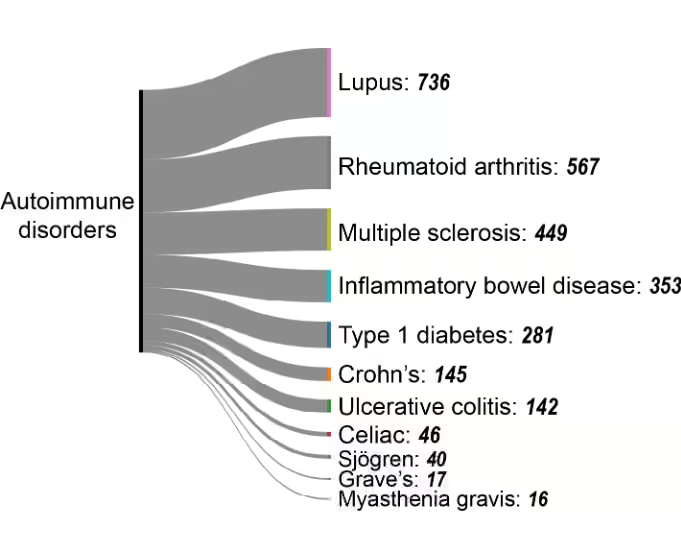
자가면역 질환 가운데에서는 다음과 같은 질환들이 주요 연구 대상으로 부상하고 있습니다(그림 7).
- 전신홍반루푸스(SLE): miRNA 조절 이상과 연관된 병태생리.
- 류마티스 관절염(RA): 활막 섬유아세포와 면역 세포에서의 DNA 메틸화 변화가 관절 염증을 촉진하며, 히스톤 변형이 염증성 사이토카인 생성 조절에 관여합니다.
- 다발성 경화증(MS): T 세포와 B 세포에서의 후성유전학적 변화가 면역 조절 및 수초 파괴 관련 유전자에 영향을 미치며, miRNA 조절 이상이 질환 진행과 관련이 있습니다.
- 제1형 당뇨병(T1D): 췌장 β 세포와 면역 세포에서의 DNA 메틸화 및 히스톤 변형이 인슐린 생성 세포의 자가면역적 파괴에 기여하며, miR-21, miR-34a 등의 miRNA가 병인에 관여합니다.
- 염증성 장질환(IBD): 크론병과 궤양성 대장염을 포함하며, 장 상피 세포와 면역 세포에서의 후생유전학적 변화가 miRNA 조절 이상과 함께 만성 염증을 유도합니다.
후성유전 치료제: 에피드러그의 임상 적용
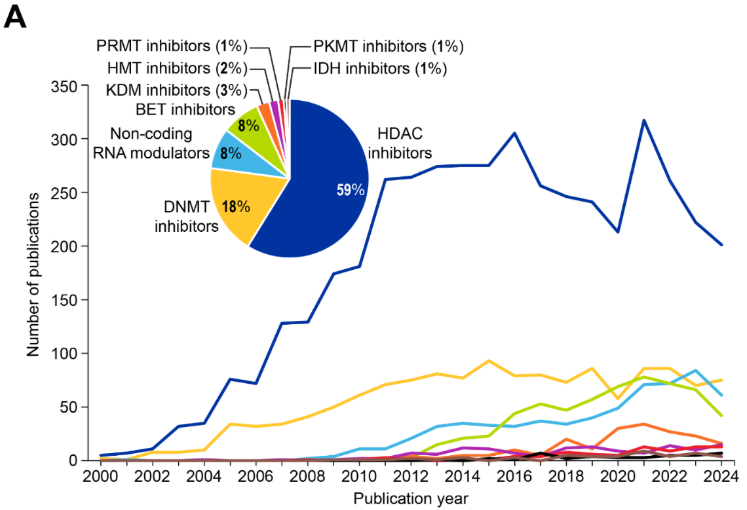
후성유전 치료제(epi-drugs)는 후성유전 조절 이상이 특징인 질환에서 비정상적인 후성유전 변형을 되돌려 정상적인 유전자 발현을 회복하는 것을 목표로 합니다. 치료제 동향을 살펴보면(그림 8A 참조) HDAC 억제제가 전체 간행물의 59%를 차지하며 가장 큰 비중을 보이고 있습니다. 그다음으로는 DNMT 억제제가 18%를 차지하며 뒤를 이었으며, RNA 조절제 중 ncRNA 조절제가 8%의 비중을 차지했습니다.
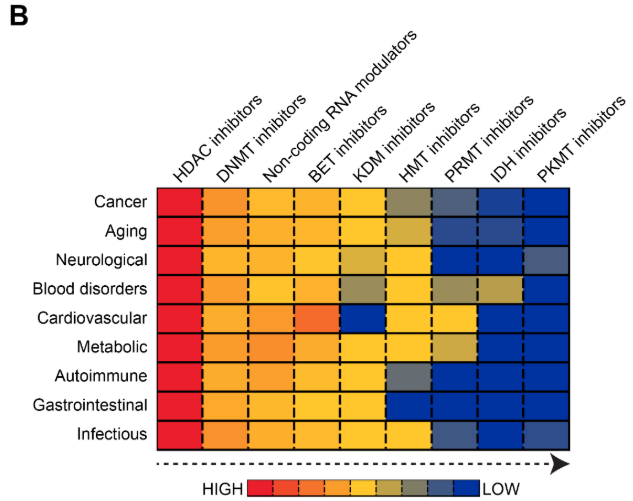
현재 사용 중인 에피드러그
- 히스톤 탈아세틸화효소(HDAC) 억제제는 히스톤에서 아세틸기가 제거되는 것을 차단하여, 염색질 구조를 이완된 상태로 유지하고 종양 억제 유전자를 포함한 유전자 발현을 증가시킵니다. HDAC 억제제는 전사 인자 및 샤페론 단백질과 같은 비히스톤 단백질에도 영향을 미쳐 항암 효과에 더욱 기여합니다.
- DNA 메틸전달효소(DNMT) 억제제는 관련 연구 간행물 수 기준으로 두 번째로 큰 에피드러그 계열입니다. 이들 약물은 DNMT의 활성을 차단함으로써 암에서 침묵된 종양 억제 유전자의 재활성을 돕습니다. 현재 임상에서 승인된 DNMT 억제제로는 아자시티딘(Vidaza®)과 데시타빈(Dacogen®)이 있으며, 이들은 DNA 복제 과정에서 DNA에 삽입되는 뉴클레오사이드 유사체로서 DNMT에 비가역적으로 결합해 메틸화를 억제합니다.
- ncRNA 조절제는 miRNA 또는 lncRNA를 표적으로 하여 유전자 조절에 영향을 미칩니다. RNA 조절제는 특히 2018년 이후 빠르게 성장한 범주로 나타나며(그림 8A), 이는 miRNA와 lncRNA가 정밀의학에서 약물 표적이 될 수 있다는 인식이 확산되고 있음을 반영합니다.
- 브로모도메인 및 엑스트라 터미널 도메인(BET) 억제제는 BET 단백질이 아세틸화된 히스톤에 결합하는 것을 차단하여 종양 유전자의 전사 활성화를 방해합니다. BET 단백질(BRD2, BRD3, BRD4 등)은 히스톤의 아세틸화된 라이신을 인식·결합하며, 후성유전 표지의 ‘리더(reader)’ 역할을 합니다.
- 히스톤 라이신 탈메틸화효소(KDM) 억제제는 라이신 탈메틸화효소(LSD) 계열 또는 Jumonji 도메인을 포함하는(JmjC) N-메틸 라이신 탈메틸화효소를 억제합니다. 현재까지 승인된 KDM 억제제는 없지만, KDM4 억제제인 자본뎀스타트(zavondemstat)가 임상 시험 단계에 있으며, 추가적인 약물 개발 연구가 진행 중입니다.
- 히스톤 메틸전달효소(HMT) 억제제는 히스톤 단백질의 특정 라이신 또는 아르기닌 잔기에 메틸기를 추가하는 효소를 표적으로 합니다. 이러한 메틸화는 히스톤의 종류와 위치에 따라 유전자 발현을 활성화하거나 억제할 수 있습니다.
- 단백질 아르기닌 메틸전달효소(PRMT) 억제제는 단백질에 메틸기를 추가하는 단백질 메틸전달효소를 표적으로 하며, 유전자 발현과 세포 과정에 영향을 미칩니다 HMT 억제제와 PRMT·PKMT 억제제와 같은 단백질 메틸전달효소 억제제는 아직 초기 개발 단계에 있는 반면, KDM 억제제는 점차 치료 가능성이 부각되고 있습니다.
- 아이소시트르산 탈수소효소(IDH) 억제제는 IDH1 및 IDH2와 같은 변이형 IDH 효소를 표적으로 하며, 이들 효소는 종양대사산물인 2-하이드록시글루타레이트를 생성합니다. 이러한 효소는 세포 내에 축적되어 TET 단백질과 히스톤 탈메틸화효소 등 후성유전 조절에 관여하는 효소를 억제함으로써 DNA 과메틸화를 유도하고 세포 분화를 차단합니다.
- Enhancer of zeste homolog 2(EZH2) 억제제는 특정 HMT 억제제로 작용하여 H3K27me3 수준을 감소시키고 침묵된 종양 억제 유전자를 재활성화합니다. 이를 통해 정상적인 세포 분화를 회복하고 종양 성장을 억제할 수 있으며, 특히 EZH2 변이 또는 과발현이 관찰되는 암에서 효과가 기대됩니다.
- 이중 작용 또는 다중 후성유전 조절제는 여러 후성유전 경로를 동시에 표적으로 하는 기전을 결합한 약물입니다. 이러한 에피드러그는 복잡한 질환에서 치료 효과를 강화할 수 있는 가능성을 제시합니다.
동시 언급 분석
후성유전 치료제의 임상 환경은 규제 측면에서의 성과를 보여주고 있으며, 현재 미국 FDA의 승인을 받은 후성유전 조절 인자를 표적으로 하는 치료제는 총 13종에 이릅니다(그림 9 참조).
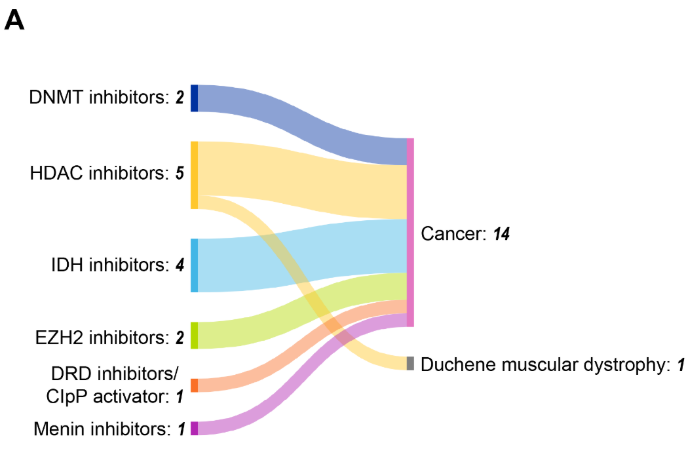
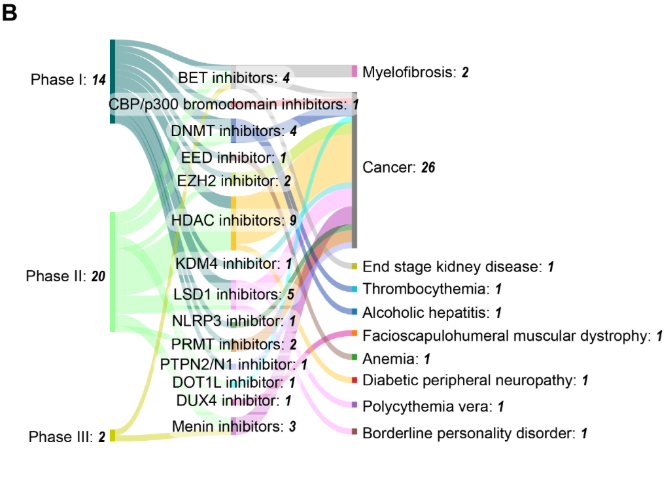
HDAC 억제제는 승인된 치료제 가운데 5종으로 가장 큰 비중을 차지하며, 혈액학적 악성 종양이 주요 치료 적용 분야로 나타납니다. 실제로 승인된 15개 적응증 중 12개가 혈액암에 해당합니다. 이러한 집중 양상은 혈액암이 후성유전적 조절 이상에 민감하며, 고형종양에 비해 혈액계 표적이 상대적으로 접근하기 용이하다는 점을 반영합니다.
DNMT 억제제인 아자시티딘(2004년)과 데시타빈(2006년)은 최초로 승인된 후성유전 치료제에 속하며, 골수이형성증후군과 급성 골수성 백혈병(AML)에서 DNA 메틸화를 표적으로 하는 치료 전략의 개념을 확립했습니다. 또한 보리노스타트, 로미뎁신, 벨리노스타트를 포함한 HDAC 억제제들은 다양한 혈액학적 악성 종양에서 치료 효과를 보여주며, 히스톤 변형을 치료 표적으로 삼는 접근의 유효성을 입증했습니다.
임상 시험 단계의 후성유전 치료제
임상 시험 단계에 있는 후성유전 치료제의 환경은 지난 25년간 크게 확대되었으며, 현재 clinicaltrials.gov에 등록된 임상 시험은 약 2,200건에 달합니다(그림 10 참조). 2000년 단 1건의 임상 시험에서 출발해, 2024년에는 연간 약 200건에 가까운 임상 시험이 수행될 정도로 지속적인 증가세를 보이고 있으며, 규제 환경의 변화와 시장 역학을 반영하는 뚜렷한 변동 양상도 함께 나타납니다. 2004년 아자시티딘이 미국 FDA 승인을 받은 이후, 임상 시험 활동은 증감이 반복되는 흐름을 보였지만 전반적으로는 상승 추세를 유지했습니다. 이러한 성장 패턴은 간헐적인 통합 국면에도 불구하고 지속적인 제약 투자가 이어지고 있음을 나타냅니다.
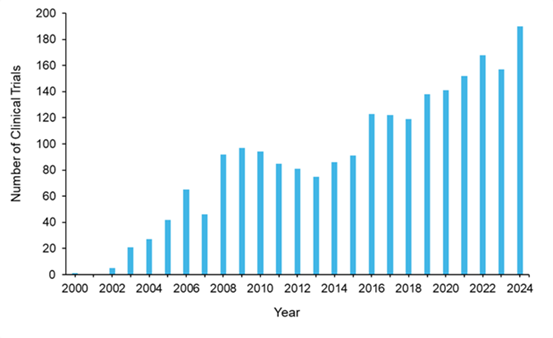
후성유전 치료제 임상 시험을 단계별로 분석한 결과, 2상 시험이 57%로 가장 큰 비중을 차지하며, 1상(32%)과 3상(9%)이 그 뒤를 이었습니다. 이러한 분포는 일반적인 신약 개발 과정의 특성을 반영하는 동시에, 후성유전 치료제 개발에서의 높은 탈락률과 다수의 병용 요법이 탐색 단계에 있음을 보여줍니다. 특히 전체 임상 시험의 62%가 이미 미국 FDA 승인을 받은 약물을 포함하고 있어, 초기 적응증을 넘어선 적응증 확장과 병용 치료 전략에 대한 활발한 탐색이 이루어지고 있음을 시사합니다. 나머지 38%의 임상 시험은 아직 승인되지 않은 신규 또는 신개념 치료제를 대상으로 합니다.
임상 개발 파이프라인을 살펴보면, 총 36건의 진행 중인 임상 시험이 3개 단계에 걸쳐 분포하며 활발한 연구 활동이 이어지고 있습니다. 이 가운데 2상 시험이 23건으로 가장 많고, DNMT 억제제와 HDAC 억제제가 각각 4건과 11건의 임상 시험으로 강한 존재감을 유지하고 있습니다. DNMT 및 HDAC 억제제 외에도 LSD1, BET, menin 억제제에 대한 연구도 점차 확대되고 있습니다(그림 9B 참조). 이러한 분포는 기존 표적에 대한 지속적인 최적화와 더불어 새로운 후성유전 조절 인자로의 연구 확장이 병행되고 있음을 보여줍니다. 임상 적용 분야는 여전히 암이 주를 이루며 전체 36건 중 26건이 암 관련 임상 시험이지만, 혈소판증가증, 알코올성 간염, 골수섬유증, 당뇨병성 말초신경병증 등 비종양성 질환으로의 점진적인 확산도 관찰됩니다.
임상 개발 단계에서 유망한 후보 물질
개발 중인 다양한 약물 가운데, 암 및 기타 질환에서 유망성이 두드러지는 후보 물질들이 있습니다.
- 종양학 치료제:
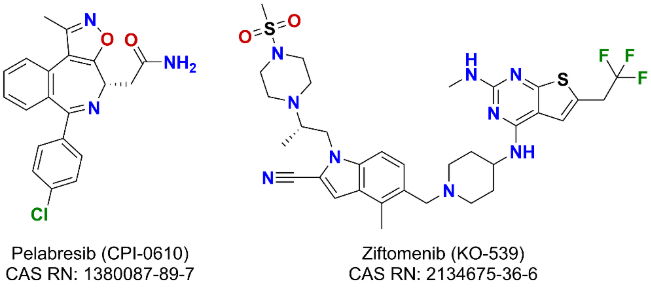
- Pelabresib(CPI-0610)는 차세대 BET 억제제로, 골수섬유증 치료를 대상으로 임상 3상 단계에 도달했습니다.
- Ziftomeni(KO-539)는 menin-KMT2A 단백질-단백질 상호작용을 선택적으로 억제하는 저분자 억제제로, 재발성 또는 불응성 NPM1 변이 급성 골수성 백혈병(AML) 치료제로서 2024년 3월 미국 FDA 혁신 치료제로 지정되었습니다.
- 비종양학 치료제:
- Apabetalone(RVX-208)은 BD2 도메인을 표적으로 하는 선택적 BET 억제제로, 말기 신장 질환을 대상으로 현재 임상 1/2상이 진행 중입니다.
- Larsucosterol(DUR-928)은 내인성 황산화 옥시스테롤 기반의 최초 계열 후성유전 조절제로, 알코올성 간염 치료를 위한 임상 2상에 있습니다.
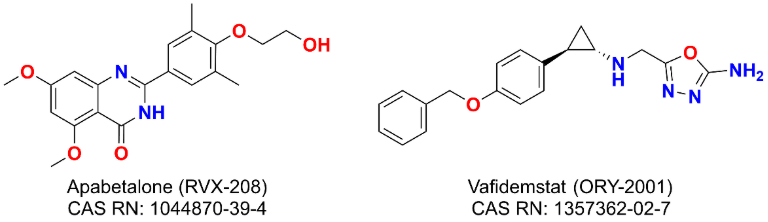
- Vafidemstat(ORY-2001)는 선택적 LSD1 억제제로, 경계선 성격장애를 대상으로 현재 임상 2상에서 평가되고 있습니다.
- 최근 승인된 약제:
- Modeyso(Dordaviprone)는 H3K27M 변이 미만성 정중선 교종 환자(만 1세 이상)를 대상으로 2025년 8월 미국 FDA 가속 승인을 받았습니다.
- Revuforj(Revumenib)는 KMT2A 재배열 급성 골수성 백혈병(AML) 성인 및 소아 환자의 재발성/불응성 질환 치료제로 2024년 11월 미국 FDA 승인을 획득했습니다.
개인 맞춤 의학에서의 후성유전학
후성유전 데이터의 통합은 특히 복합 질환을 대상으로 정밀한 진단 도구, 예후 지표, 그리고 치료 접근법의 개발을 가능하게 합니다. 앞서 언급한 바와 같이 DNMT 억제제와 HDAC 억제제를 포함한 에피드러그는 이미 임상적으로 확립되어 있으며, 현재도 지속적으로 개발되고 있습니다. 또한 후성유전 약물을 화학요법이나 면역치료와 병용하는 복합 치료 전략은 치료 효과를 향상시키고 있으며, 이는 개인맞춤 치료 접근법에서 중요한 진전을 의미합니다.
후성유전학에서 또 다른 핵심적 돌파구는 이러한 변형을 조직별 바이오마커로 사용하는 것입니다. 이러한 질병별 패턴의 예로는 암에서의 종양 억제 유전자 과메틸화, 그리고 알츠하이머병이나 파킨슨병 환자에서 관찰되는 비정상적인 DNA 메틸화 및 히스톤 변형이 있습니다.
이러한 후성유전 바이오마커를 규명하면 질환의 조기 발견과 진단이 가능해집니다. 예를 들어, 혈액이나 기타 체액에서 암 특이적 DNA 메틸화 패턴을 검출하는 액체 생검을 통해 비침습적 진단 및 모니터링을 수행할 수 있으며, 모체 혈액 내 후성유전 마커를 활용한 산전 검사를 통해 태아의 건강 상태를 평가할 수도 있습니다. 예후 측면에서 후성유전 마커는 질병의 경과와 치료 반응을 예측하는 데 활용됩니다. 예를 들어, 일부 암에서는 메틸화 상태가 예후와 전이 가능성을 예측하며, 정신질환에서는 후성유전적 변화가 약물 반응을 예측하는 지표가 될 수 있습니다.
후성유전 바이오마커의 임상 적용
후성유전 바이오마커는 질병 진단, 예후 평가, 그리고 치료 의사결정에서 중요한 역할을 합니다. 본 분석에서는 CAS Content Collection에 수록된 후성유전 바이오마커 관련 간행물을 분석하였으며, 그 결과 2008~2009년경부터 급격한 증가가 나타났고, 일부 정체 구간(2015~2017년, 2023~2024년)도 관찰되었습니다(그림 11 참조).
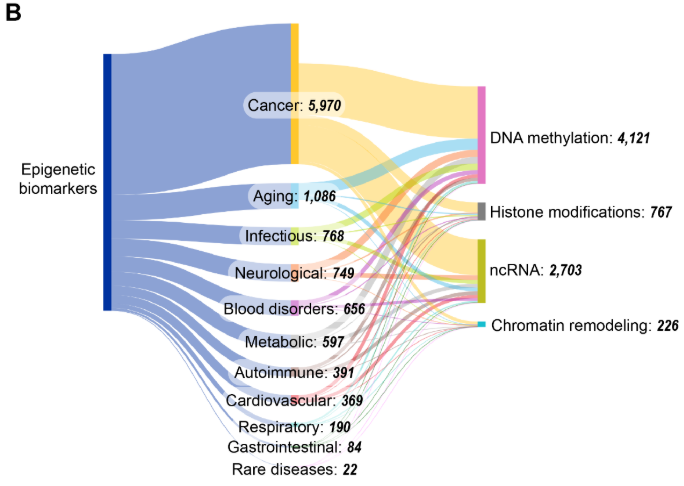
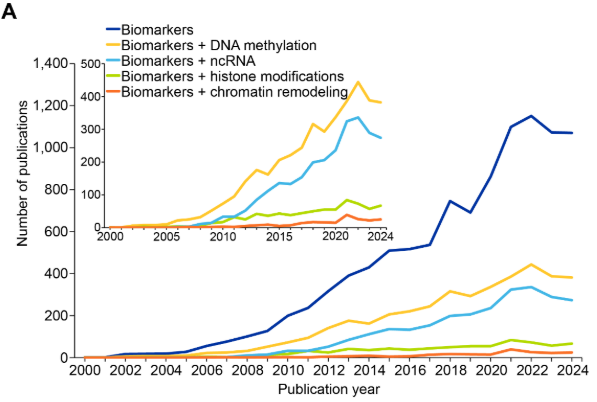
네 가지 주요 후성유전 기전 가운데 DNA 메틸화와 ncRNA가 가장 활발히 연구된 영역으로 나타났으며, DNA 메틸화 및 ncRNA 바이오마커 관련 간행물 수는 2015년부터 2022년 사이에 두 배로 증가하였습니다. 반면, 히스톤 변형과 크로마틴 리모델링은 이 맥락에서는 상대적으로 연구가 덜 이루어진 상태로 남아 있습니다. 그림 11B에서 볼 수 있듯이, 암은 후성유전 바이오마커 관련 간행물과 가장 빈번하게 동시 언급되는 질환으로 나타나며, 이는 종양형성 과정에서 후성유전 조절 이상이 차지하는 확립된 역할과 진단 및 예후 평가에 활용되는 MGMT516, VIM517과 같은 메틸화 마커의 임상적 유용성을 반영합니다. 또한 노화 관련 연구의 높은 비중은 최근 후성유전학 시계의 개발과 생물학적 연령 평가에서의 활용 확대와도 맥락을 같이합니다.
DNA 메틸화 바이오마커
비정상적인 DNA 메틸화 패턴은 질병의 특징적인 지표로 작용하며, 특히 종양 억제 유전자의 과메틸화는 다양한 암에서 공통적으로 관찰되는 바이오마커입니다. 예를 들어, SEPT9 메틸화는 대장내시경의 대안으로 혈액 기반 검출을 통해 비침습적인 대장암 선별검사를 가능하게 합니다. MGMT 메틸화는 교모세포종에서 테모졸로마이드 치료 반응을 예측하는 지표로 활용되며, 과메틸화가 더 나은 치료 결과와 연관됩니다. 또한 BRCA1 메틸화는 유방암 및 난소암 발생 위험 증가와 연관된 진단 및 예후 바이오마커로 작용합니다. 특히 DNA 메틸화는 후성유전 바이오마커 연구에서 가장 빈번하게 동시 언급되는 기전으로 나타나는데, 이는 화학적 안정성, 확립된 검출 방법론, 그리고 FDA 승인 검사로의 직접적인 임상 적용 가능성에 기인한 것으로 해석됩니다.
히스톤 변형 바이오마커
히스톤 변형은 염색질 구조와 유전자 발현에 영향을 미치며, 특정 히스톤 표식은 질병 상태와 연관되어 있습니다. 그림 11B에서 관찰되는 히스톤 변형의 비교적 낮은 동시 언급 빈도는 이 기전이 지닌 역동성과 치료 개입에 대한 반응성을 고려할 때 아직 충분히 활용되지 않은 잠재력이 있음을 시사합니다.
일부 암에서는 히스톤 H4 아세틸화 감소가 불량한 예후를 예측하는 지표로 작용하며, 히스톤 H3 라이신 27 삼중 메틸화(H3K27me3)는 PRC2 조절 이상을 반영하고 전립선암과 방광암에서 불량한 예후와 상관관계를 보입니다. 또한 히스톤 H3/H4 시트룰린화는 류마티스 관절염의 특징적 지표인 항-시트룰린화 단백질 항체(ACPAs) 생성과 연관되어, 질병의 진단과 모니터링에 활용됩니다.
이러한 유망한 결과에도 불구하고, 히스톤 변형은 본질적으로 불안정하며 효소적 분해에 취약해 시료 채취 후 수분 이내에 신호가 급격히 소실될 수 있다는 한계가 존재합니다. 현재의 분석 프로토콜은 프로테아제, 탈아세틸화효소, 탈메틸화효소 억제제를 포함한 특수 보존 완충액을 필요로 하며, 이는 일상적인 임상 적용을 복잡하게 만드는 요인으로 작용합니다.
ncRNA 바이오마커
miR-21529, miR-155530과 같은 miRNA를 포함한 ncRNA는 다양한 암에서 과발현되며, 체액을 통한 진단 및 예후 바이오마커로 활용됩니다. 후성유전 바이오마커 연구에서 ncRNA의 높은 동시 언급 빈도는 순환 miRNA와 lncRNA가 최소 침습적 바이오마커로서 주목받고 있음을 반영합니다.
예를 들어, miR-21의 과발현은 유방암, 폐암, 대장암 전반에서 종양 성장, 침윤, 전이, 그리고 화학요법 내성과 관련이 있습니다. miR-208a 수치 증가는 급성 심근경색(심장마비)의 바이오마커로 활용됩니다. 또한 HOTAIR lncRNA의 과발현은 유방암, 대장암, 췌장암에서 전이 발생과 불량한 예후를 시사합니다.
염색질 재구성 바이오마커
염색질 재구성 패턴은 치료 저항성을 예측하는 데 활용될 수 있으며, 약물 저항성 암세포에서 관찰되는 개방된 염색질 영역은 치료 실패를 예측하는 데 사용됩니다. 히스톤 변형과 마찬가지로, 염색질 재구성의 비교적 낮은 동시 언급 빈도는 아직 충분히 활용되지 않은 잠재력을 시사합니다.
전반적으로 후성유전 바이오마커의 미래는 견고한 고처리량 기술의 개발과 통합적 접근 방식에 달려 있습니다 후성유전체, 유전체, 전사체, 단백체 데이터를 결합하는 멀티오믹스 통합은 바이오마커 발굴과 검증을 한층 강화할 것입니다. 또한 체액에서 후성유전 바이오마커를 비침습적으로 검출하는 기술은 조기 진단과 질병 모니터링 방식을 혁신할 것으로 기대됩니다.
고도화된 계산 도구는 환자 계층화를 위한 복잡한 후성유전 시그니처를 식별하는 데 기여할 것으로 예상됩니다. 예를 들어, CRISPR 기반 후성유전체 편집은 질병과 연관된 후성유전 표지를 조작할 수 있게 하여, 바이오마커를 진단 도구에서 치료 도구로 확장할 가능성을 제시합니다.
의학에서의 후성유전학의 윤리적·법적·사회적 함의
후성유전학은 건강과 질병에 대한 우리의 이해를 근본적으로 확장할 잠재력을 지니고 있지만, 동시에 중요한 윤리적·법적·사회적 과제를 제기합니다. 이러한 과제를 해결하기 위해서는 후성유전학 연구의 이점과 개인의 권리 보호, 사회적 형평성 증진 사이의 균형을 고려한 선제적이고 협력적인 접근이 필요합니다. 견고한 윤리 지침, 법적 보호 장치, 공공 참여 전략을 마련함으로써, 잠재적 위해를 최소화하면서 건강과 웰빙을 증진하기 위해 후성유전학의 힘을 활용할 수 있습니다.
윤리적 고려 사항
- 프라이버시와 차별: 후성유전 정보는 유전 정보와 마찬가지로 개인의 건강 상태, 생활 방식, 환경 노출 이력 등 민감한 정보를 드러낼 수 있는 고도의 개인 정보이므로, 강력한 개인정보 보호가 요구됩니다. 예를 들어 질병 위험을 예측하는 후성유전 표지가 건강보험료 인상이나 보장 거절과 같은 보험 차별로 이어질 수 있습니다. 또한 과거 행동에 따른 후성유전 변화를 탐지할 수 있다는 점은 소급적 건강 평가나 고용 차별에 대한 우려를 불러일으킵니다.
- 개인의 책임과 세대 간 영향: 이와 관련하여, 후성유전 정보는 개인의 건강 상태를 개인 책임으로만 환원해 해석하게 만들 수 있으며 이는 사회적·환경적 건강 결정 요인을 간과하게 할 위험이 있습니다. 환경 요인에 의해 유발된 후성유전 변화는 경우에 따라 다음 세대로 전달될 수 있습니다. 이는 후성유전 마커를 변화시키는 개입이 장기적이로 미칠 영향에 대한 윤리적 우려를 제기합니다.
법적 요구 사항
- 규제 감독: 소비자 직접 대상 후성유전 검사 키트의 확산은 정확성, 해석, 규제와 관련된 우려를 동반합니다. 법적 제도는 이러한 기술이 과학적 근거와 윤리적 기준에 부합하도록 보장하는 한편, 검증되지 않은 기술의 성급한 상용화를 방지해야 합니다.
- 책임과 지식재산권: 환경 노출과 연관된 후성유전 변화는 복잡한 책임 문제를 야기합니다. 예를 들어 독성 물질로 인한 피해의 책임이 고용주, 제조업체, 정부 중 누구에게 있는지에 대한 판단이 필요합니다. 부모 또는 제3자의 과실이나 환경 노출로 인해 태아에게 발생한 후성유전적 피해에 대한 법적 책임 역시 신중한 검토가 요구됩니다. 또한 바이오마커나 치료제 등 후성유전 연구의 상업화는 특허와 소유권 문제를 수반하며, 혁신을 촉진하는 동시에 후성유전 기술에 대한 공공의 접근성을 유지하는 것 사이의 균형이 요구됩니다.
사회적 함의
- 공공 이해와 형평성: 후성유전학에 대한 대중의 이해가 제한적인 상황에서는 검증되지 않은 치료법(예: '후성유전 식이요법')에 대한 오해나 악용이 발생할 수 있습니다. 이 문제를 해결하고 정보에 기반한 의사 결정을 개선하기 위해서는 포괄적인 교육과 활발한 과학적 소통이 필수적입니다. 또한 환경 노출과 질병 간의 연관성을 다루는 후성유전 연구는, 오염 물질에 많이 노출된 특정 지역이나 집단에 대한 낙인으로 이어질 위험도 있습니다. 후성유전 치료에 대한 공정한 접근을 보장하고 건강 격차의 심화를 방지하기 위해서는 사회경제적 장벽을 고려한 정책적 개입이 필요합니다.
- 이행 전략: 효과적인 거버넌스를 위해서는 후성유전 데이터의 수집·사용·공유에 대한 명확한 윤리 지침, 후성유전 정보의 특수성을 반영한 법적 체계의 정비, 신뢰와 충분한 설명에 기반한 공공 참여, 그리고 국가 간 일관된 기준을 위한 국제 협력이 요구됩니다. 강력한 보호 조치를 개발하는 동시에 책임 있는 혁신을 촉진함으로써, 사회는 개인의 권리를 보호하고 건강 형평성을 증진하는 방향으로 후성유전학의 변혁적 잠재력을 활용할 수 있습니다.
후성유전학의 향후 방향
지난 10여 년간 후성유전학 연구의 지형은 괄목할 만한 변화를 겪었습니다. 분자생물학의 전문 분야로 여겨지던 후성유전학은 이제 인간의 건강과 치료 개입에 중대한 함의를 지니는 주류 바이오의학 분야로 발전했습니다. 후성유전 연구의 임상적 전환 또한 뚜렷한 성과를 거두었으며, 현재까지 미 FDA 승인을 받은 15개 치료제가 후성유전 표적이 치료적으로 실현 가능함을 입증하고 있습니다. 여러 개발 단계에 걸쳐 진행 중인 36건의 임상시험은 후성유전 치료제에 대한 지속적인 투자와 신뢰를 보여주며, 연구 대상도 종양학을 넘어 대사 질환, 신경계 질환, 염증성 질환, 희귀 질환으로 점차 확대되고 있습니다.
이러한 변화는 식이, 스트레스, 독소, 생활 방식과 같은 환경 요인이 세대를 넘어 영향을 미칠 수 있는 유전 가능한 후성유전 변화를 유도한다는 인식이 확산된 결과를 반영합니다. 환경 노출 데이터와 개인별 후성유전 프로파일을 통합하면 개인 맞춤형 위험 평가와 개입 전략이 가능해지며, 이는 예방 중심의 정밀의료 접근으로의 근본적인 전환을 의미합니다.
후성유전학의 미래는 밝으며, 생물학에 대한 이해를 향상시키고 인간의 건강을 개선할 수 있는 막대한 잠재력을 가지고 있습니다. 그러나 이러한 잠재력을 실현하기 위해서는 기술적 한계, 윤리적 쟁점, 후성유전 조절의 복잡성과 같은 중요한 과제를 극복해야 합니다. 학제 간 협력을 강화하고, 혁신적인 기술에 투자하며, 윤리적·사회적 함의를 함께 고려한다면, 후성유전학은 앞으로도 획기적인 발견을 이어가고 이를 의미 있는 임상적·사회적 성과로 연결해 나갈 수 있을 것입니다.