La epigenética, el estudio de los cambios hereditarios en la expresión génica que no implican alteraciones en la secuencia del ADN, ha surgido como un campo transformador en la biología y la medicina, revelando cómo se modula la expresión génica en respuesta a señales internas y externas. La regulación epigenética es fundamental para la biología del desarrollo, la patogénesis de las enfermedades, las interacciones entre los genes y el medioambiente, la herencia transgeneracional y el desarrollo terapéutico. Al elucidar cómo los genes se regulan dinámicamente más allá del genoma estático, la epigenética conecta la genética con las influencias ambientales, ofreciendo conocimientos sobre los mecanismos de la enfermedad y estrategias terapéuticas innovadoras.
Analizamos el CAS Content CollectionTM, el mayor repositorio de información científica seleccionado por humanos, para describir los avances realizados en la investigación epigenética e identificar los principales conceptos y desafíos emergentes. Este análisis exhaustivo examina los fundamentos científicos, las aplicaciones clínicas y las innovaciones tecnológicas que impactan las ciencias de la vida modernas y la atención médica.
Nuestro análisis reveló un crecimiento pronunciado y continuo de las publicaciones en las dos últimas décadas, con más de 120 000 publicaciones relacionadas con la epigenética actualmente en la Colección de contenidos de CAS (véase la Figura 1). El campo está dominado por los artículos de revistas (97 %), y las patentes solo representan el 3 % de las publicaciones (véase la Figura 1A), lo que indica que la epigenética sigue en fase de descubrimiento y validación.
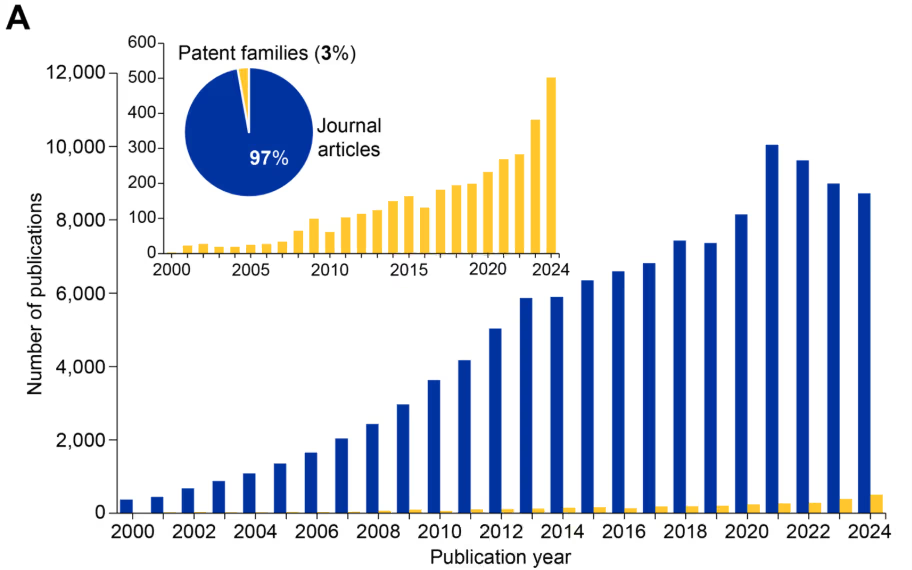


Sin embargo, el fuerte aumento de publicaciones de patentes (véase el gráfico insertado en la figura 1A) indica un creciente interés comercial y potencial traslacional en este campo en rápida evolución. Cabe destacar que las publicaciones en epigenética han superado a las de genética desde 2014 (Figura 1B). El surgimiento de la epitranscriptómica como un campo diferenciado es notable después de 2020 (Figura 1B).
Esta trayectoria de crecimiento se alinea con incrementos sustanciales de financiación: la financiación total de la investigación pasó de 200 millones de dólares estadounidenses en 2004 a más de 4500 millones de dólares estadounidenses en 2024, apoyando aproximadamente 2700 proyectos anuales (véase la Figura 1C). El aumento constante en el número de proyectos y los niveles de financiación, con una financiación media que pasa de 1,2 millones a 1,7 millones de dólares estadounidenses, subraya un compromiso sostenido tanto gubernamental como del sector privado para avanzar en la investigación epigenética y su traducción clínica.
La importancia comercial de la epigenética se ha expandido de forma espectacular: el mercado mundial de la epigenética se valora en 1840 millones de dólares estadounidenses en 2023 y se prevé que alcance los 6770 millones de dólares estadounidenses para 2033. Este crecimiento está impulsado por más de diez medicamentos epigenéticos aprobados por la FDA, incluidos la azacitidina (Vidaza ® ) y el vorinostat (Zolinza ®) para el tratamiento del cáncer. También hay más de 35 terapias epigenéticas en ensayos clínicos. Estos candidatos se centran principalmente en diversas malignidades, pero están empezando a mostrar diversificación más allá del cáncer.
Exploremos la epigenética con más detalle para comprender cómo está evolucionando y qué significa para el futuro de la medicina:
Mecanismos básicos de la regulación epigenética
Los mecanismos epigenéticos regulan la expresión de los genes mediante modificaciones químicas del ADN y de la estructura de la cromatina sin alterar la secuencia del ADN. Estos mecanismos comprenden cuatro clases principales: metilación del ADN, modificaciones de histonas, regulación de ARN no codificante (ncARN) y remodelación de la cromatina. Al examinar publicaciones relacionadas con la epigenética, vimos pocas publicaciones que abordaran estos mecanismos al principio, un resultado comprensible, ya que el campo se estaba estableciendo a principios de los 2000 (véase la Figura 2).
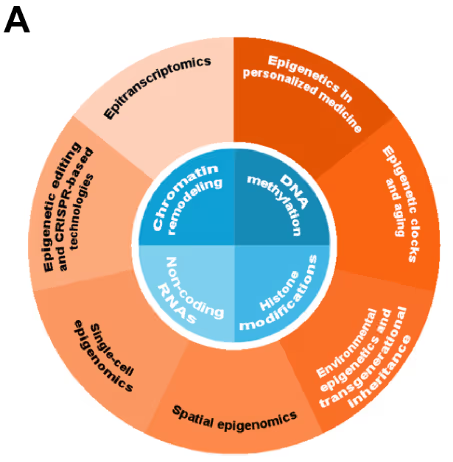

Posteriormente, los cuatro mecanismos mostraron un crecimiento acelerado, con la metilación del ADN experimentando el mayor aumento y llegando a dominar el panorama de la investigación, tanto en publicaciones de revistas como en patentes. Los demás mecanismos también experimentaron un aumento, lo que sugiere el reconocimiento creciente de objetivos epigenéticos para el desarrollo de fármacos.
Metilación del ADN
La metilación del ADN es un mecanismo epigenético fundamental que implica la adición de grupos metilo (-CH₃) a los anillos de citosina en los dinucleótidos CpG del ADN, lo que provoca una represión transcripcional. Esta modificación desempeña un papel fundamental en la inactivación del cromosoma X, la impronta genómica y la supresión de transposones.
La metilación del ADN es catalizada por las metiltransferasas de ADN (DNMT). La DNMT1 mantiene los patrones de metilación existentes durante la replicación, mientras que la DNMT3a/3b establece nuevos patrones de metilación durante el desarrollo o en respuesta a señales ambientales. La DNMT3L, que carece de actividad catalítica y se expresa principalmente en las primeras etapas del desarrollo, se limita a las células germinativas y al timo en la edad adulta. Las DNMT apuntan a las islas CpG, regiones con alta frecuencia de dinucleótidos CpG, a menudo ubicadas cerca de los promotores de genes.
Se han identificado patrones aberrantes de metilación en diversas enfermedades, como el cáncer, las enfermedades cardiovasculares, los trastornos mentales, la enfermedad de Alzheimer, el autismo y los síndromes metabólicos. La hipermetilación de los promotores génicos supresores tumorales silencia su expresión promoviendo la oncogénesis, mientras que la hipometilación global puede activar oncogenes y causar inestabilidad genómica. Los patrones de metilación del ADN cambian con la edad, lo que incluye la acumulación de errores y la pérdida de fidelidad en el mantenimiento de la metilación.
Modificaciones de histonas
Las modificaciones de histonas pueden heredarse a través de la división celular y pueden verse influenciadas por factores ambientales, lo que podría impactar el desarrollo y los estados de enfermedad. Las modificaciones postraduccionales de las histonas, como la acetilación, la metilación, la fosforilación y la ubiquitinación, alteran la estructura de la cromatina y la accesibilidad de los genes. Las histonas acetiltransferasas (HAT) y las desacetilasas (HDAC) regulan la acetilación catalizando la adición y eliminación de grupos acetilo de las histonas, mientras que las metiltransferasas (HMT) y desmetilasas (HDM) controlan la metilación. Estas modificaciones ocurren principalmente en residuos de lisina, arginina, serina y treonina en las colas de histonas, que son protuberancias del núcleo nucleosomico con Incremento de accesibilidad.
Las modificaciones de las histonas afectan a la estructura de la cromatina, que es el ADN empaquetado alrededor de las proteínas histonas que regulan la expresión génica, la reparación del ADN y la condensación de los cromosomas durante la mitosis. Las modificaciones aberrantes de las histonas pueden alterar los patrones de expresión génica y contribuir al desarrollo y metástasis tumoral, además de estar vinculadas a otras enfermedades y trastornos como el Alzheimer, la enfermedad de Huntington, el autismo, los cambios asociados a la cromatina asociados al envejecimiento y la desregulación inmunitaria.
Estos cambios suelen formar un «código de histonas», con combinaciones de modificaciones en diferentes residuos que sinergizan o antagonizan estados finos de cromatina. Son un sistema dinámico y versátil para regular la estructura de la cromatina y la expresión de los genes, y su naturaleza reversible las convierte en objetivos prometedores para intervenciones terapéuticas.
ARN no codificantes (ncARN)
Las ncARN constituyen una clase diversa de moléculas reguladoras que desempeñan funciones reguladoras fundamentales en la expresión génica y la dinámica de la cromatina sin codificar proteínas. Estos ARN ajustan el procesamiento de los genes dirigiéndose al ARN mensajero (ARNm) para su degradación o modulando la maquinaria transcripcional.
Han surgido tres clases como reguladores epigenéticos principales: microARN (miARN), ARN largos no codificantes (lncARN) y ARN interactuantes con PIWI (piARN). Estos ncARN orquestan la regulación epigenética a través de cinco mecanismos principales:
- Remodelación de la cromatina: los IncARN reclutan complejos modificadores de la cromatina a loci genómicos específicos, influyendo en la estructura de la cromatina y la expresión génica. Por ejemplo, el transcrito específico inactivo del cromosoma X (XIST) media en la inactivación del cromosoma X al reclutar el complejo represivo polycomb 2 (PRC2).
- Regulación transcripcional: los miARN y los lncARN modulan la transcripción al interactuar con los factores de transcripción o las ARN polimerasas. Por ejemplo, el ARN intergénico antisentido del transcrito HOX (HOTAIR) recluta al PRC2 para reprimir genes en un cromosoma diferente.
- Control post-transcripcional: los miARN se unen a las regiones 3′ no traducidas (UTR) de los ARN mensajeros (mARN) diana, lo que conduce a la degradación o inhibición de la traducción. Los lncARN pueden actuar como esponjas moleculares para secuestrar los miARN, lo que les impide dirigirse a los miARN.
- Modificación del ARN: Algunos ncARN guían la metilación del ARN (por ejemplo, N6-metiladenosina, m6A) o la edición, lo que afecta a la estabilidad y la traducción del ARN.
- Defensa del genoma: los piARN y los siARN suprimen los elementos transponibles y protegen la integridad genómica. Los siARN pueden guiar la formación de heterocromatina en regiones con secuencias repetitivas.
Remodelación de la cromatina
La remodelación de la cromatina modifica dinámicamente la arquitectura de la cromatina entre los estados de eucromatina (abierta, transcripcionalmente activa) y heterocromatina (condensada, transcripcionalmente silenciosa). La unidad básica de la cromatina es el nucleosoma, compuesto de ADN envuelto alrededor de un octámero de proteínas histonas. La remodelación de la cromatina se realiza mediante complejos dependientes de ATP, como switch/sacarosa no fermentable (SWI/SNF), switch de imitación (ISWI), proteínas que se unen al ADN helicasa del cromodominio (CHD) y familias INO80 que utilizan hidrólisis de ATP para alimentar el reposicionamiento, eyección o reestructuración de nucleosomas.
Los mecanismos de remodelación incluyen el deslizamiento de nucleosomas, la expulsión/intercambio de histonas y la compactación/descomposición de cromatina. Estos procesos trabajan con la metilación del ADN y las modificaciones de las histonas para regular la expresión genética, la diferenciación celular y el mantenimiento de la identidad.
La desregulación de la remodelación de la cromatina está relacionada con el cáncer, los trastornos neurológicos y las enfermedades del desarrollo. Por ejemplo, las mutaciones en los remodeladores de la cromatina, como el dominio de interacción 1A rico en AT (ARID1A) (un componente del complejo SWI/SNF), se observan con frecuencia en las neoplasias malignas. Los remodeladores de cromatina representan objetivos terapéuticos prometedores para revertir la expresión génica aberrante. Por ello, la remodelación de la cromatina se reconoce como mediadora de las influencias ambientales (dieta, estrés, toxinas, etc.) en la expresión génica y la salud.
Avances recientes en epigenética
Los avances recientes han demostrado cómo las modificaciones epigenéticas, incluyendo la metilación del ADN, las modificaciones de histonas, la regulación de ncARN y la remodelación de la cromatina, contribuyen a la patogénesis de la enfermedad, especialmente en el cáncer. La investigación emergente sobre miARN y otros ncARN como reguladores epigenéticos ha identificado nuevos objetivos terapéuticos, mientras que los avances en el perfilado epigenético individual están ayudando a los avances en el concepto de medicina personalizada. Las tendencias de publicación muestran los principales campos de interés (véase la Figura 3).

Epigenética ambiental
Los factores ambientales como la dieta, el estrés, las toxinas y el estilo de vida pueden inducir cambios epigenéticos a través de los diversos mecanismos comentados anteriormente. Estas modificaciones podrían contribuir al desarrollo de enfermedades como el cáncer, los trastornos metabólicos y las afecciones neurológicas al alterar la función celular y la homeostasis de los tejidos. Las influencias específicas incluyen:
- Disponibilidad de nutrientes (p. ej., folato, vitamina B12) que afectan a los patrones de metilación del ADN.
- Exposiciones químicas (p. ej., bisfenol A, pesticidas, contaminantes atmosféricos) que alteran las marcas epigenéticas y provocan consecuencias para la salud a largo plazo.
- El estrés psicológico y fisiológico provoca cambios epigenéticos en los genes de respuesta al estrés y modula la salud mental.
- Los factores del estilo de vida (por ejemplo, el tabaquismo, el alcohol, los niveles de actividad física) influyen en el riesgo de enfermedad mediante la modulación de los estados epigenéticos.
Epitranscriptómica
La epitranscriptómica se centra en el estudio de las modificaciones químicas de las moléculas de ARN y su papel en la regulación de la expresión génica y las funciones celulares. Así como la epigenética explora las modificaciones al ADN y las histonas que influyen en la actividad génica sin alterar la secuencia subyacente de ADN, la epitranscriptómica investiga cómo las modificaciones del ARN afectan a la estabilidad, la traducción, el empalme y otros procesos del ARN.
Se han identificado más de 170 modificaciones distintas del ARN en el mARN, el tARN, el rARN y los ncARN; la N6-metiladenosina (m6A) es la modificación más abundante y estudiada del mARN eucariota. Algunas modificaciones clave son: metilación de m6A en la posición N6 de la adenosina, influencia en la estabilidad del ARNm, empalme, exportación y traslación; metilación m5C en la posición N5 de la citosina en el ARNm y ARNt, afectando la estabilidad y traducción del ARN; pseudouridina (Ψ), un isómero de la uridina, que mejora la estabilidad del ARN y la eficiencia de traslación; y la desaminación adenosina-inosina, alterando las propiedades de emparejamiento de bases y afectando el empalme y la codificación de proteínas.
La maquinaria epitranscriptómica comprende tres clases principales de proteínas:
- «Escritoras»: enzimas que añaden modificaciones (por ejemplo, complejo METTL3/METTL14 para la metilación m6A).
- «Borradoras»: enzimas que eliminan modificaciones (p. ej., proteína asociada a masa grasa y obesidad (FTO) y homólogo alkB 5, ARN desmetilasa (ALKBH5) para la desmetilación de m6A).
- «Lectoras»: proteínas que reconocen y se unen al ARN modificado (por ejemplo, proteínas del dominio YTH para el reconocimiento de m6A), que regulan colectivamente la dinámica de modificación del ARN.
Las modificaciones del ARN regulan varios procesos celulares y la desregulación de estas modificaciones contribuye a diversas patologías. En el cáncer, las modificaciones m6A suelen alterarse en tumores y se relacionan con la progresión tumoral, la metástasis y la resistencia a los fármacos. La edición y las modificaciones aberrantes del ARN se asocian a enfermedades neurodegenerativas como el Alzheimer, el Parkinson y la ELA. Además, los virus de ARN, incluidos el VIH y el SARS-CoV-2, explotan la maquinaria de modificación del ARN del huésped para regular la replicación viral y la evasión inmunológica, incluidas las modificaciones epigenéticas.
Las tecnologías de secuenciación de alto rendimiento permiten cartografiar las modificaciones del ARN en todo el genoma, complementadas con técnicas de espectrometría de masas y etiquetado químico para la detección y cuantificación de dichas modificaciones. Estos avances facilitan el desarrollo terapéutico dirigido a las enzimas de modificación del ARN.
Se está estudiando atacar los componentes de la maquinaria de modificación del ARN (escritores, borradores y lectores) como estrategia para tratar enfermedades. Por ejemplo, los inhibidores de FTO, que son las desmetilasas m6A, han mostrado potencial en la terapia contra el cáncer, mientras que los nucleótidos modificados en vacunas de ARNm mejoran la estabilidad y la eficiencia de la traducción.
En general, la investigación actual se centra en descifrar el «código epitranscriptoma», desarrollar herramientas para la manipulación precisa in vivo de modificaciones de ARN y explorar modificaciones en los ncARN. La epitranscriptómica de célula única está revelando patrones de modificación del ARN específicos de cada tipo celular y sus consecuencias funcionales. Una tecnología emergente, la integración multi-ómica, combina datos epigenómicos con transcriptómica, proteómica y metabolómica utilizando tecnologías como CUT&RUN e integración Hi-C, proporcionando vistas holísticas de la función celular. Estos métodos permiten el análisis exhaustivo de las vías y el descubrimiento de biomarcadores en enfermedades complejas.
Herencia transgeneracional
La herencia transgeneracional se refiere a la transmisión de cambios epigenéticos inducidos por el medioambiente a través de múltiples generaciones, independientemente de las alteraciones de la secuencia del ADN. Este fenómeno se ha observado en plantas y animales, lo que sugiere que las exposiciones ambientales sufridas por una generación pueden afectar a la salud y al desarrollo de las generaciones siguientes. Sin embargo, verificar el alcance y la importancia de este proceso en los seres humanos es todo un reto.
Los ejemplos de herencia epigenética transgeneracional incluyen el invierno del hambre holandés (1944-1945), en el que se observaron patrones alterados de metilación del ADN y un aumento del riesgo metabólico en las generaciones posteriores de personas que estuvieron expuestas a la hambruna en los Países Bajos. Los estudios en animales también han proporcionado ejemplos de efectos transgeneracionales de los disruptores endocrinos (por ejemplo, vinclozolina) sobre la reproducción, el comportamiento y la susceptibilidad a enfermedades, mientras que en humanos el tabaquismo paterno y el estrés materno se han relacionado con cambios epigenéticos en la descendencia.
Aunque los mecanismos subyacentes a la herencia epigenética transgeneracional no se comprenden completamente, su efecto en el aumento del perfil de riesgo de enfermedades como la obesidad, la diabetes y los trastornos cardiovasculares en descendientes de personas expuestas significa que sigue siendo un área de investigación activa. Comprender los efectos transgeneracionales también puede informar normativas para reducir la exposición a factores ambientales perjudiciales, especialmente durante ventanas críticas de desarrollo (por ejemplo, el embarazo).
Edición epigenética y tecnologías basadas en CRISPR
La llegada de la tecnología CRISPR-Cas9 ha revolucionado la ingeniería genética, y su aplicación a la epigenética no es una excepción. La edición epigenética consiste en la modificación dirigida de las marcas epigenéticas sin alterar la secuencia del ADN, lo que ofrece una poderosa herramienta para estudiar la regulación de los genes y desarrollar nuevas terapias.
El sistema CRISPR-Cas9 emplea ARN guía (gARN) para dirigir la Cas9 catalíticamente inactiva (dCas9), fusionada con dominios efectores epigenéticos, a loci genómicos específicos. Los dominios efectores clave incluyen DNMT (p. ej., DNMT3A), desmetilasas de ADN (p. ej., TET1), modificadores de histonas (p. ej., p300, HDACs) y remodeladores de cromatina, que permiten añadir o eliminar con precisión modificaciones epigenéticas.
La tecnología CRISPR-Cas9 permite la activación selectiva o represión de la expresión génica al dirigirse a elementos reguladores, incluidos potenciadores y promotores, permitiendo a los investigadores probar directamente los roles causales de marcas epigenéticas específicas en la regulación génica, la diferenciación celular y la enfermedad. Asimismo, permite examinar la herencia epigenética a través de las divisiones celulares, el desarrollo y la generación de modelos de enfermedad impulsados por la desregulación epigenética.
Las aplicaciones terapéuticas incluyen silenciar genes causantes de enfermedades (oncogenes, genes virales) y reactivar genes silenciados beneficiosos (supresores tumorales) en cáncer e hipercolesterolemia, entre otros. Este concepto ofrece el potencial de terapias altamente personalizadas con efectos fuera del objetivo mínimos y aplicaciones en la reprogramación celular para la medicina regenerativa. Las principales ventajas de la edición del epigenoma basada en CRISPR incluyen la alta precisión de direccionamiento, la versatilidad a través de dominios efectores intercambiables y la reducción del riesgo mutágeno en comparación con la edición genética.
Avanzar en esta tecnología requiere desarrollar variantes de Cas de alta fidelidad y diseños optimizados de gARN para minimizar los efectos fuera del objetivo. Además, la segmentación multiplexada permitirá investigar redes regulatorias complejas, mientras que los métodos de administración mejorados (vectores virales, nanopartículas) facilitarán la traducción clínica. Las tecnologías emergentes en este espacio incluyen herramientas de edición del epigenoma, en particular los sistemas basados en CRISPR/dCas9 fusionados con efectores epigenéticos (DNMT, TET, HDAC). Plataformas alternativas incluyen proteínas TALE549 y dedo de zinc para la selección específica del locus.
Epigenómica de células únicas
Las tecnologías epigenómicas unicelulares permiten elaborar perfiles de las modificaciones epigenéticas con la resolución de células individuales. Esto proporciona unas percepciones sin precedentes sobre la diversidad y función celular y supera los inconvenientes de los métodos tradicionales de secuenciación masiva, que analizan marcas epigenéticas medias en millones de células.
Las técnicas que incluyen ATAC-seq de una sola célula (ensayo para cromatina accesible a transposasa usando secuenciación) y ChIP-seq de una sola célula (secuenciación por inmunoprecipitación de cromatina) perfilan la accesibilidad de la cromatina y las modificaciones de histonas en células individuales y están a la vanguardia de esta tendencia. Las aplicaciones incluyen el mapeo de panoramas epigenéticos durante la embriogénesis, la diferenciación celular y tisular, las decisiones sobre el destino celular y la heterogeneidad del sistema inmunitario.
En la investigación del cáncer, la epigenómica unicelular puede descubrir heterogeneidad epigenética intratumoral que corresponda a la evolución clonal, la resistencia a fármacos y la metástasis. La tecnología también se utiliza para dilucidar cambios epigenéticos en el neurodesarrollo, la neurodegeneración y la diferenciación de células inmunitarias, informando nuestra comprensión de las enfermedades autoinmunes y las respuestas de inmunoterapia.
Las direcciones futuras incluyen la integración con la transcriptómica espacial, el perfil temporal de las marcas epigenéticas en respuesta a los procesos celulares o los estímulos ambientales y las aplicaciones clínicas para la identificación de biomarcadores y la medicina personalizada.
Epigenómica espacial
La epigenómica espacial es una tecnología de vanguardia que combina el estudio de las modificaciones epigenéticas con el contexto espacial dentro de los tejidos. Este concepto une la epigenómica unicelular y la histología, para revelar cómo la regulación epigenética varía entre regiones tisulares e influye en la organización, función y comunicación celular en salud y enfermedad.
Las aplicaciones incluyen el mapeo de patrones de tejido durante la organogénesis guiada por cambios epigenéticos; la identificación de firmas epigenéticas espacialmente distintas dentro de los tumores (núcleo frente a márgenes invasivos), que pueden llevar a la metástasis o la resistencia a los medicamentos; la caracterización de cambios epigenéticos específicos de la región en tejidos cerebrales o tipos de células que brindan conocimientos sobre el desarrollo neurológico, la plasticidad y las enfermedades neurodegenerativas; la comprensión de la regulación epigenética en nichos de células inmunes; y la influencia de los estados epigenéticos en el microambiente tisular.
Epigenética en salud y enfermedad
Las modificaciones epigenéticas guían el desarrollo embrionario y las decisiones sobre el destino celular al activar o silenciar conjuntos de genes específicos. La desregulación de estos procesos afecta a numerosas patologías, y aunque el cáncer ha sido el área principal de investigación de enfermedades, se está explorando el papel de la epigenética en otras condiciones.
Cáncer
Hace tiempo que se reconoce que las mutaciones genéticas son las causas del cáncer, y ahora se entiende que las alteraciones epigenéticas desempeñan un papel igual de importante en la tumorogénesis. El panorama de la investigación revela la dominancia del cáncer con el 47% de las publicaciones, reflejando tanto la madurez del campo como el éxito en la traducción clínica (véase la Figura 4).
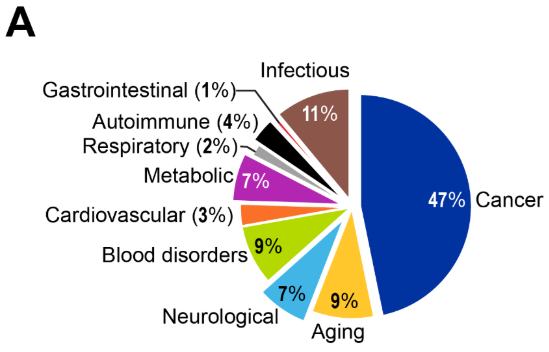

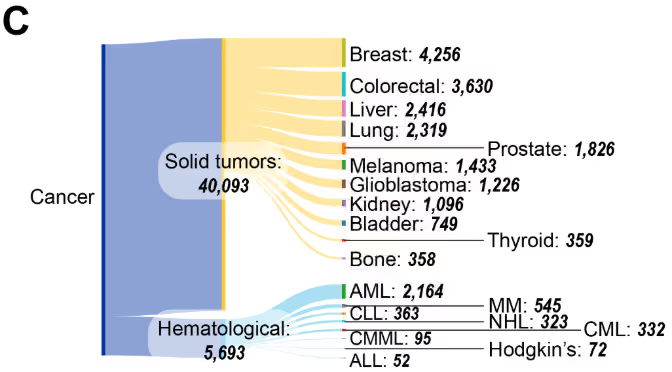
Los tumores sólidos representan la gran mayoría de las publicaciones (Figura 4C), siendo el cáncer de mama, colorrectal, hígado y pulmón los que lideran en términos de actividad de investigación. Entre las malignidades hematológicas, predomina la leucemia mieloide aguda (LMA), seguida por la leucemia linfocítica crónica (LLC) y el mieloma múltiple (MM). Esta distribución basada en datos de publicaciones de la CAS colección de contenidos se alinea con las terapias epigenéticas aprobadas por la FDA de EE. UU. que tienen como objetivo estas malignidades, incluyendo azacitidina y decitabina utilizadas para el tratamiento de la LMA y vorinostat para el linfoma cutáneo de células T.
La regulación epigenética del cáncer implica tres mecanismos principales:
- Metilación del ADN: la hipermetilación de las regiones promotoras a menudo conduce al silenciamiento de los genes supresores de tumores, mientras que la hipometilación global puede activar oncogenes y promover la inestabilidad genómica.
- Modificaciones de las histonas: las alteraciones de la acetilación, metilación y fosforilación de las histonas pueden modificar la estructura de la cromatina y la expresión de los genes.
- ncARN: la desregulación de los miARN (por ejemplo, la sobreexpresión de miR-21) puede promover la progresión del cáncer al dirigirse a los supresores de tumores o a los oncogenes.
El mapa de calor de coocurrencia de mecanismos genéticos y epigenéticos que se muestra en la Figura 5 muestra patrones distintos. Por ejemplo, el predominio de la metilación del ADN refleja su papel como importante mecanismo epigenético. La remodelación de la cromatina muestra una coocurrencia mínima en la mayoría de los genes, lo que sugiere que tiene un papel en cambios arquitectónicos más amplios que en la regulación específica de un gen. Las publicaciones asociadas con modificaciones de ncARN e histonas se sitúan entre los dos extremos: metilación del ADN y remodelación de la cromatina.
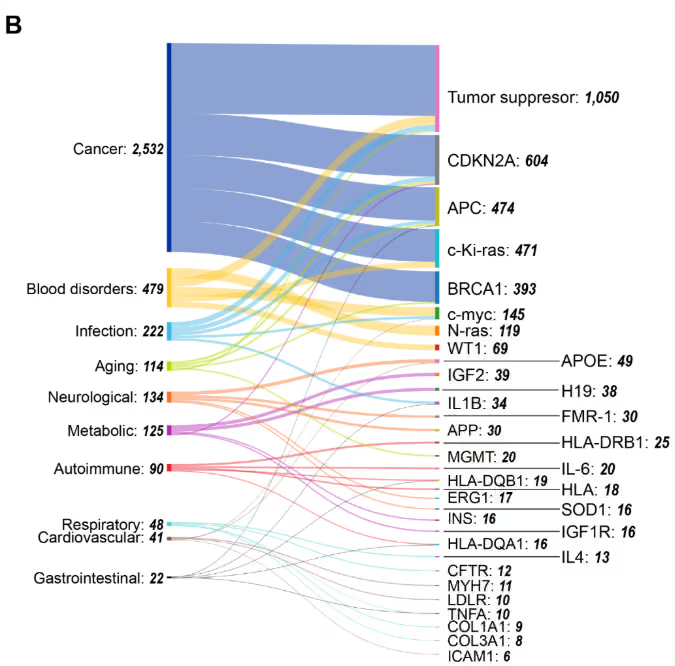
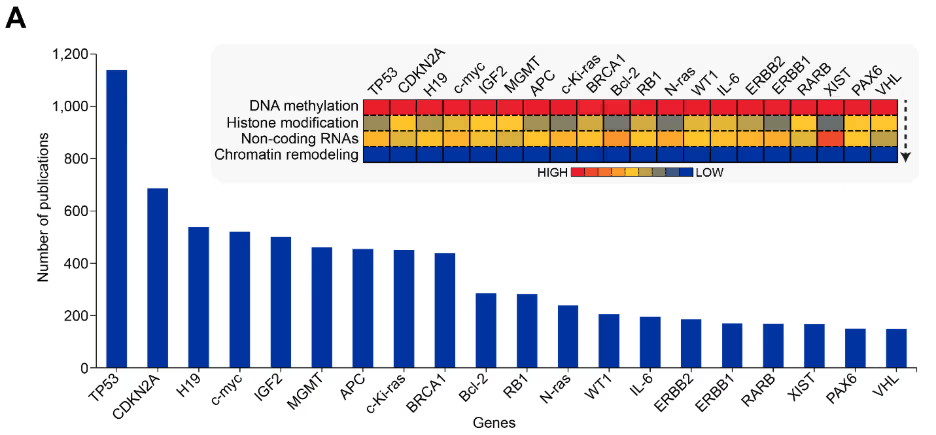
Nuestro análisis de coocurrencias de genes y enfermedades (Figura 5B) ilustra la posición central del cáncer, así como que los genes supresores de tumores muestran la mayor conectividad. Otros genes con alta coocurrencia en múltiples tipos de cáncer incluyen el CDKN2A, seguido del APC y el c-Ki-ras (KRAS325). Este patrón refleja las funciones de estos genes como centros epigenéticos sujetos al silenciamiento mediado por la metilación en diversas neoplasias malignas.
Relojes epigenéticos y condiciones relacionadas con el envejecimiento
Los relojes epigenéticos son un concepto innovador que utiliza modelos computacionales que predicen la edad biológica basándose en los patrones de metilación del ADN. Pueden revelar discrepancias entre la edad biológica y cronológica de una persona, para ofrecer conocimientos sobre el proceso de envejecimiento y el impacto de los factores de estilo de vida y ambientales. Estos modelos aprovechan los cambios predecibles relacionados con la edad en la metilación del ADN, en los que regiones genómicas específicas se hipermetilan o hipometilan según patrones reproducibles.
El reloj epigenético de primera generación, el reloj de Horvath, fue desarrollado por Steve Horvath en 2013 y utiliza datos de metilación del ADN de 353 sitios CpG en múltiples tejidos y tipos de células para estimar la edad biológica. El reloj de Hannum, desarrollado ese mismo año, emplea 71 sitios de CpG, principalmente en la sangre. Los relojes más recientes, como los de GriMage y PhenoAge, incorporan biomarcadores adicionales (por ejemplo, proteínas plasmáticas) para mejorar la precisión y predecir la mortalidad y el riesgo de enfermedad.
En la investigación sobre longevidad, los centenarios y las personas con una longevidad excepcional suelen mostrar un envejecimiento epigenético más lento, lo que proporciona pistas sobre los factores genéticos y ambientales que promueven un envejecimiento saludable. La investigación actual explora la reversibilidad a través de compuestos senolíticos y epigenéticos dirigidos a los reguladores.
Las tendencias de publicación de investigaciones que se observan en la Figura 4A demuestran que el envejecimiento representa el 9 % de la investigación epigenética que menciona explícitamente la enfermedad y el envejecimiento, significativamente menor que la investigación sobre el cáncer (47 %), pero que muestra un crecimiento constante entre 2010 y 2024, especialmente notable después de 2019 (Figura 4B). Esta proporción refleja el papel especializado pero creciente de la investigación sobre envejecimiento dentro del panorama epigenético más amplio dominado por aplicaciones relacionadas con el cáncer.
Enfermedades neurodegenerativas
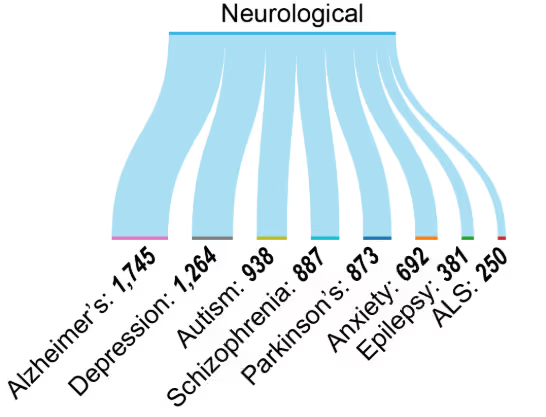
Las modificaciones epigenéticas se han relacionado con enfermedades neurodegenerativas como el Alzheimer, el Parkinson y la ELA, así como con trastornos mentales como la depresión y la esquizofrenia (Figura 6). La sustancial producción de investigación refleja el creciente reconocimiento de los mecanismos epigenéticos en patologías neuropsiquiátricas y neurodegenerativas (véase la Figura 4A).
Las alteraciones epigenéticas afectan a los genes implicados en la producción de amiloide beta (Aβ) y la fosforilación de tau en la enfermedad de Alzheimer, asociándose con la desregulación de miARN como miR-29352 y miR-34354, lo que se asocia con el deterioro cognitivo. La enfermedad de Parkinson muestra cambios epigenéticos en los genes de la función mitocondrial (por ejemplo, PINK1355) y en las vías de agregación de la α-sinucleína. Los patrones de acetilación de histonas y de metilación del ADN se alteran en los modelos de enfermedad de Parkinson, lo que afecta la supervivencia neuronal.
Los trastornos del espectro autista muestran una desregulación de los genes sinápticos (por ejemplo, el SHANK3360) a través de modificaciones aberrantes en la metilación del ADN y las histonas, y se ha demostrado que los factores ambientales, como la exposición prenatal al ácido valproico, inducen cambios epigenéticos en modelos animales. En la epilepsia, los mecanismos epigenéticos regulan los genes de los canales iónicos y los genes de la plasticidad sináptica, lo que contribuye a la susceptibilidad a las convulsiones, y se observan modificaciones en las histonas y una desregulación del miARN. Los trastornos del neurodesarrollo ejemplifican una regulación epigenética crítica, como se evidencia en mutaciones en el gen MECP2, que codifica una proteína que se une a metil-CpG, causando el síndrome de Rett e hipermetilación de FMR1 en el síndrome del X frágil.
Las alteraciones epigenéticas son cada vez más reconocidas como biomarcadores de trastornos neurológicos. Los patrones de metilación de genes como BDNF372 y COMT374 están asociados con la función cognitiva y los trastornos psiquiátricos, mientras que algunas marcas específicas de histonas (por ejemplo, H3K27me3) están vinculadas a redes regulatorias de genes en la neurodegeneración. Los miARN circulantes, en particular miR-132376 y miR-124378, han mostrado potencial como biomarcadores no invasivos para el diagnóstico de la enfermedad de Alzheimer y Parkinson, respectivamente, lo que ofrece potencial para la detección precoz y el seguimiento terapéutico.
Enfermedad cardiovascular
Los mecanismos epigenéticos contribuyen a la patogénesis de varias enfermedades cardiovasculares, aunque nuestro análisis de datos de publicaciones sugiere una fracción más pequeña de interés de investigación en comparación con el cáncer (véase Figura 4A). Por ejemplo, en la aterosclerosis, la metilación del ADN y las modificaciones de las histonas regulan los genes implicados en la inflamación, el metabolismo de los lípidos y la función endotelial. La hipometilación de genes proinflamatorios (p. ej., IL-6384) y la hipermetilación de genes antiinflamatorios (p. ej., PPARγ385) promueven la formación de placa.
Los cambios epigenéticos en los genes que regulan el tono vascular y la homeostasis sódica contribuyen a la hipertensión, mientras que factores ambientales como una dieta alta en sal y el estrés pueden inducir estas alteraciones epigenéticas. La regulación epigenética de los genes de los canales iónicos (por ejemplo, el SCN5A y el KCNQ1392) puede predisponer a las personas a las arritmias. De forma similar, las modificaciones epigenéticas llevan a la remodelación cardíaca patológica, incluyendo la hipertrofia y la fibrosis. La metilación del ADN, las modificaciones de las histonas y los miARN son reguladores clave de estos procesos. En la cardiopatía isquémica y el ictus, la metilación del ADN y las modificaciones de las histonas alteran la expresión de los genes que rigen la supervivencia celular, las respuestas al estrés y las vías inflamatorias.
Al igual que ocurre con los trastornos neurológicos, estas alteraciones se documentan cada vez más como biomarcadores. Los patrones de metilación de genes como F2RL3400 y AHRR401 están asociados con el riesgo y los resultados cardiovasculares. Las marcas específicas de histonas están vinculadas a redes regulatorias génicas en insuficiencia cardíaca y aterosclerosis. Los miARN circulantes se utilizan como biomarcadores para el infarto agudo de miocardio y la insuficiencia cardíaca.
Trastornos metabólicos
Las modificaciones epigenéticas regulan los genes que controlan la sensibilidad a la insulina, el almacenamiento de grasa y la inflamación en las enfermedades metabólicas. Los factores ambientales, como la dieta y el ejercicio, inducen cambios epigenéticos persistentes que contribuyen a la resistencia a la insulina y a la disfunción metabólica.
Las enfermedades metabólicas representan una fracción considerable de la investigación epigenética (véase la Figura 4A); los estudios sobre obesidad y la diabetes tipo 2 dominan este campo. El extenso volumen de publicaciones refleja la epidemia global de enfermedades metabólicas y una comprensión creciente de las contribuciones epigenéticas a la disfunción metabólica. El crecimiento constante, aunque modesto, de la investigación de la epigenética metabólica es comparable a los trastornos neurológicos y hematológicos (Figura 4B), pero contrasta con el aumento exponencial en los estudios de cáncer, lo que sugiere que hay un gran potencial sin explotar en esta área.
Se ha comprobado que la epigenética desempeña un papel clave en:
- La obesidad: la metilación del ADN y las modificaciones de histonas regulan la adipogénesis, el control del apetito y los genes del gasto energético, mientras que los miARN desregulados se asocian con la obesidad y la disfunción del tejido adiposo. La metilación del ADN y las modificaciones de las histonas regulan la adipogénesis, el control del apetito y los genes del gasto energético, y los miARN desregulados se asocian con la obesidad y la disfunción del tejido adiposo.
- La diabetes tipo 2 (T2D): los cambios epigenéticos en las células β pancreáticas, hígado y músculo esquelético afectan a la producción y sensibilidad de la insulina, inncluida la metilación del ADN de los genes PPARGC1A e IRS1.
- La enfermedad hepática grasa no alcohólica (EHGNA): la metilación del ADN y las modificaciones de las histonas regulan el metabolismo lipídico hepático y la inflamación, y los miARN contribuyen a la progresión de la enfermedad.
- El síndrome metabólico: los cambios epigenéticos afectan al metabolismo de la glucosa, el metabolismo de los lípidos y los genes reguladores de la presión arterial.
- Las enfermedades cardiometabólicas: los mecanismos epigenéticos vinculan la desregulación metabólica con las complicaciones cardiovasculares a través de la metilación del ADN de genes como FTO418 y ABCA1419, asociados con el riesgo de aterosclerosis e hipertensión.
Los biomarcadores epigenéticos para las enfermedades metabólicas incluyen patrones de metilación de los genes TXNIP y SREBF1 asociados con la DT2 y la NAFLD; marcas específicas de histonas vinculadas a redes metabólicas regulatorias de genes; y miARN circulantes que actúan como biomarcadores para la diabetes tipo 2 y la obesidad. Estos biomarcadores permiten la detección temprana, la estratificación del riesgo y el seguimiento terapéutico en trastornos metabólicos.
Enfermedades autoinmunes
La metilación aberrante de genes de tolerancia inmunitaria puede activar células T autorreactivas, lo que provoca enfermedades autoinmunes. A pesar de su importancia clínica, las enfermedades autoinmunes representan una pequeña parte de la investigación epigenética (véase la Figura 4A), con un crecimiento constante pero limitado entre 2010 y 2024 en comparación con el aumento exponencial de los estudios sobre el cáncer (Figura 4B). Esta carencia de investigación sugiere que hay un gran potencial para la investigación ampliada en la epigenética autoinmune.
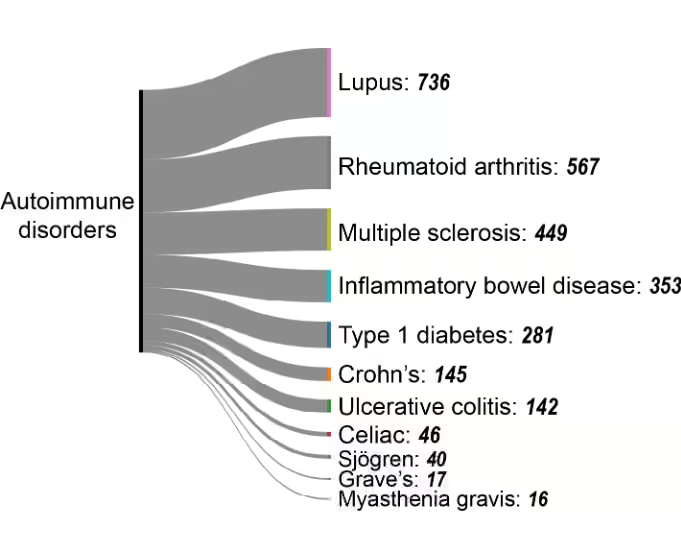
Dentro de las enfermedades autoinmunes, ciertas afecciones se han convertido en las principales áreas de investigación (figura 7):
- El lupus eritematoso sistémico (LES), una patogénesis asociada con los miARN desregulados.
- La artritis reumatoide (AR), que implica cambios en la metilación del ADN en los fibroblastos sinoviales y en las células inmunitarias que promueven la inflamación articular, mientras que las modificaciones de histonas regulan la producción de citocinas proinflamatorias.
- La esclerosis múltiple (EM), que muestra cambios epigenéticos en las células T y B que afectan los genes de regulación inmunitaria y destrucción de la mielina, con una desregulación de miARN vinculada a la progresión de la enfermedad.
- La diabetes tipo 1 (T1D), que implica la metilación del ADN y las modificaciones de histonas en las células β pancreáticas y las células inmunes que contribuyen a la destrucción autoinmune de las células productoras de insulina, con miARN (por ejemplo, miR-21, miR-34a) implicados en la patogénesis.
- La enfermedad inflamatoria intestinal (EII), como la enfermedad de Crohn y la colitis ulcerosa, que presenta cambios epigenéticos en las células epiteliales e inmunes intestinales, lo que provoca inflamación crónica junto con una asociación con la desregulación de miARN.
Terapia epigenética: aplicaciones clínicas de los epifármacos
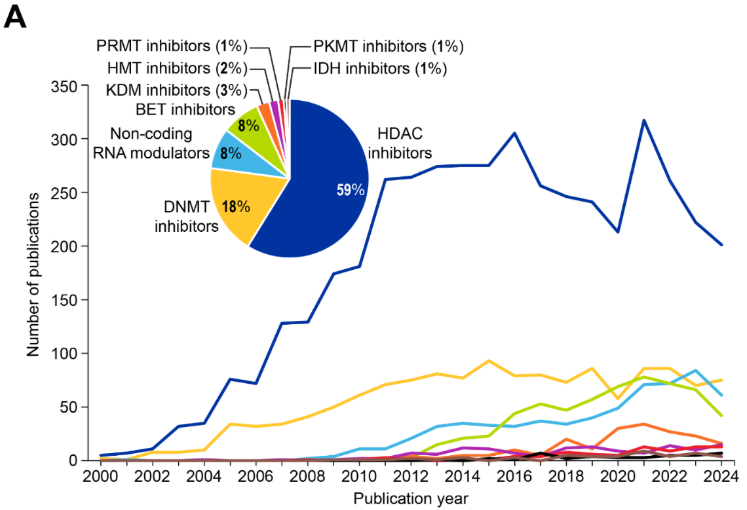
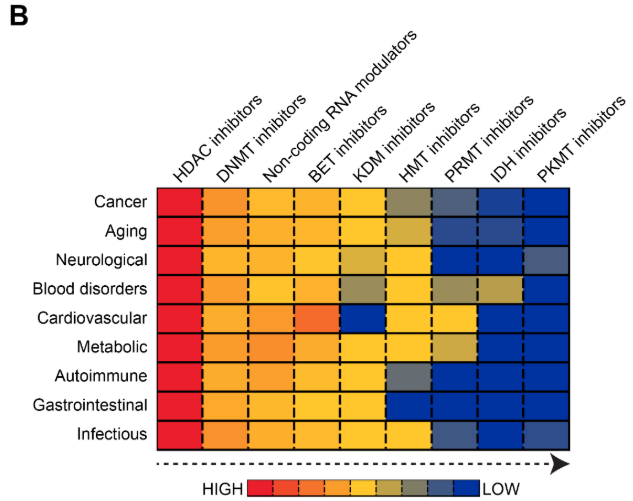
Los fármacos epigenéticos (epifármacos) invierten las modificaciones epigenéticas aberrantes para restablecer la expresión génica normal en las enfermedades caracterizadas por una desregulación epigenética. El panorama terapéutico (véase la Figura 8A) muestra que los inhibidores de HDAC dominan con el 59 % de las publicaciones, seguidos por los inhibidores de DNMT (18 %) y los moduladores de ARN (8 % cada uno para los moduladores de ncARN ).
Fármacos epigenéticos actuales:
- Los inhibidores de la histona deacetilasa (HDAC) impiden la eliminación de los grupos acetilo de las histonas, lo que favorece las estructuras de cromatina relajadas y un incremento/aumento de la expresión génica, incluidos los genes supresores de tumores. Los inhibidores de HDAC también afectan a las proteínas no histonas, como los factores de transcripción y las proteínas chaperonas, contribuyendo aún más a sus efectos anticancerígenos.
- Los inhibidores de las metiltransferasas de ADN (DNMT) representan la segunda clase más numerosa de fármacos en términos de publicaciones de investigación asociadas. Bloquean los DNMT, y ayudan así a la reactivación de genes supresores tumorales silenciados en el cáncer. Los inhibidores de DNMT actualmente aprobados para uso clínico son la azacitidina (Vidaza®) y la decitabina (Dacogen®), que son análogos de nucleósidos que incorporan ADN durante la replicación, se unen irreversiblemente a los DNMT y previenen la metilación.
- Los moduladores del ncARN atacan a los miARN o IncARN para influir en la regulación génica. Los moduladores de ARN parecen ser una categoría de rápido crecimiento, especialmente desde 2018 (Figura 8A), lo que refleja el reconocimiento de los miARN y los lncARN como dianas farmacológicas para la medicina de precisión.
- Los inhibidores del dominio bromo y del dominio extraterminal (BET) bloquean la unión de las proteínas BET a las histonas acetiladas, lo que interrumpe la activación transcripcional de los oncogenes. Las proteínas BET (por ejemplo, BRD2, BRD3, BRD4) participan en el reconocimiento y la unión de lisinas acetiladas en histonas y actúan como «lectoras» de las marcas epigenéticas.
- Inhibidores de histona lisina desmetilasas (KDMs) bloquean las enzimas que pertenecen a las lisina desmetilasas (LSD) o a la familia de enzimas desmetilasas de N-metil lisina que contienen el dominio Jumonji (JmjC). Hasta ahora no existen inhibidores aprobados de la KDM, sin embargo, actualmente hay un inhibidor de la KDM4 en un ensayo clínico (zavondemstat) y otras investigaciones en curso para desarrollar más.
- Inhibidores de la metiltransferasa de histonas (HMT) se dirigen a enzimas que añaden grupos metilo a residuos específicos de lisina o arginina en las proteínas histonas, lo que puede activar o reprimir la expresión génica dependiendo de la histona específica y la ubicación de la metilación.
- Los inhibidores de la proteína arginina metiltransferasa (PRMT) se dirigen a las proteínas metiltransferasas, las enzimas responsables de añadir grupos metilo a las proteínas y afectar a la expresión génica y a los procesos celulares. Los inhibidores del HMT y los de la proteína metiltransferasa, como los inhibidores del PRMT y la PKMT, siguen en fase de desarrollo, mientras que los inhibidores de la KDM muestran un potencial terapéutico novedoso.
- Los inhibidores de la isocitrato deshidrogenasa (IDH) se dirigen a las formas mutantes de las enzimas IDH, como la IDH1 y la IDH2, que producen el oncometabolito 2-hidroxiglutarato. Estas enzimas provocan la hipermetilación del ADN y bloquean la diferenciación celular al acumularse en las células e inhibir las enzimas implicadas en la regulación epigenética, como las proteínas TET y las desmetilasas de histonas.
- El potenciador de los inhibidores del homólogo ZESTE 2 (EZH2) actúa como inhibidores específicos de la HMT, lo que reduce los niveles de H3K27me3 y reactiva los genes supresores de tumores silenciados, que pueden restaurar la diferenciación celular normal e inhibir el crecimiento tumoral, especialmente en cánceres con mutaciones o sobreexpresión en EZH2.
- Los moduladores de doble acción o multiepigenéticos combinan mecanismos dirigidos a múltiples vías epigenéticas. Estos fármacos pueden aumentar la eficacia terapéutica en enfermedades complejas.
Análisis de coocurrencia
El panorama clínico de las terapias epigenéticas demuestra un buen desempeño regulatorio, con 13 fármacos aprobados por la FDA en EE. UU. dirigidos a reguladores epigenéticos clave (véase la Figura 9).
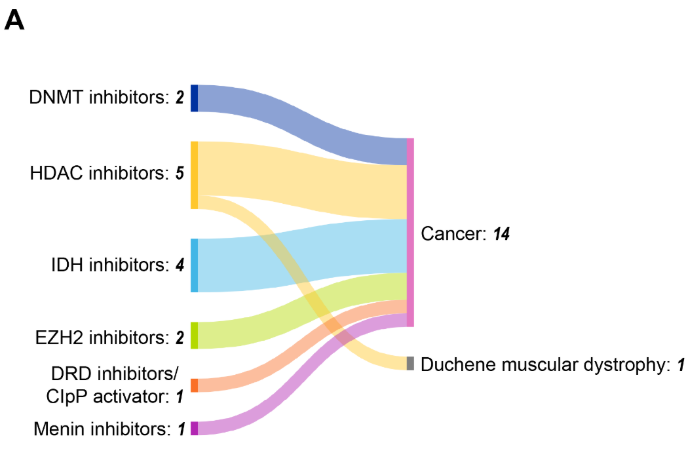
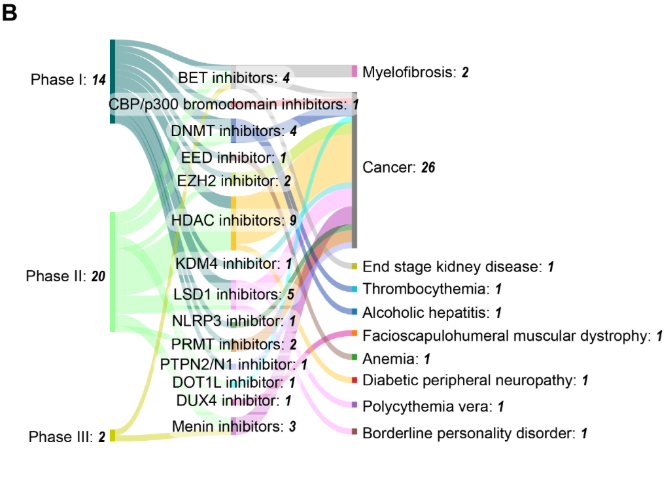
Los inhibidores de HDAC lideran con cinco aprobaciones, y las malignidades hematológicas representan la aplicación terapéutica principal, representando 12 de las 15 indicaciones aprobadas. Esta concentración refleja la sensibilidad de los cánceres de sangre a la desregulación epigenética y a la accesibilidad de los objetivos hematológicos en comparación con los tumores sólidos.
Los inhibidores de DNMT azacitidina (2004) y decitabina (2006) estuvieron entre los primeros fármacos epigenéticos aprobados, estableciendo pruebas de concepto para dirigir la metilación del ADN en síndromes mielodisplásicos y LMA. Los inhibidores de la HDAC, incluidos el vorinostat, la romidepsina y el belinostat, han demostrado su eficacia en múltiples neoplasias hematológicas, lo que valida la modificación de las histonas como objetivo terapéutico.
Fármacos epigenéticos en ensayos clínicos
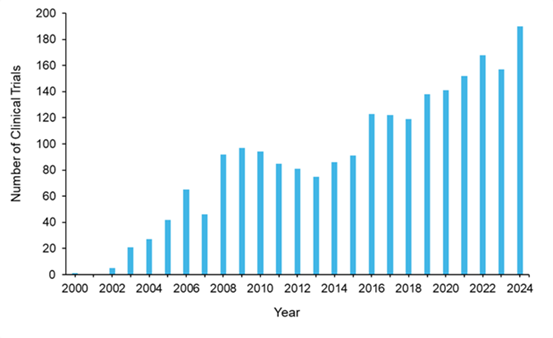
El panorama de los fármacos epigenéticos en los ensayos clínicos se ha ampliado de forma espectacular en 25 años, con cerca de 2200 ensayos registrados en clinicaltrials.gov (véase la Figura 10). Ha habido un aumento sostenido desde un único ensayo en 2000 hasta poco menos de 200 ensayos clínicos al año en 2024, con oscilaciones notables que reflejan hitos regulatorios y dinámicas del mercado. Después de la aprobación de azacitidina por parte de la FDA de EE. UU. en 2004, la actividad de los ensayos demostró patrones de aumento y disminución con una trayectoria general ascendente. Este patrón de crecimiento indica una inversión farmacéutica sostenida a pesar de fases periódicas de consolidación.
El análisis de los ensayos clínicos epigenéticos terapéuticos con respecto a la distribución de fases revela que los ensayos de Fase II dominan con un 57 %, seguidos de los de Fase I (32 %) y Fase III (9
%). Esta distribución es típica del desarrollo de fármacos y refleja la alta tasa de abandono en el desarrollo epigenético de fármacos y la naturaleza exploratoria de muchas estrategias combinadas. Cabe destacar que el 62 % de los ensayos involucran medicamentos aprobados por la FDA en EE. UU., lo que sugiere muchas iniciativas para ampliar las indicaciones de los prospectos y explorar terapias combinadas más allá de las indicaciones iniciales. El 38 % restante de los ensayos clínicos son para medicamentos nuevos o no aprobados.
El proceso de desarrollo clínico revela una actividad sólida, con 36 ensayos en curso en tres fases. Los ensayos de fase II dominan (23 ensayos) y los inhibidores de la DNMT y la HDAC mantienen una fuerte presencia clínica con 4 y 11 ensayos, respectivamente. También existe diversificación más allá de los inhibidores de DNMT y HDAC, explorando cada vez más los inhibidores de LSD1, BET y menin (véase la Figura 9B). Esta distribución demuestra tanto la optimización continua de objetivos establecidos como la expansión hacia nuevos reguladores epigenéticos. Las aplicaciones para el cáncer siguen predominando con 26 de 36 ensayos, aunque los datos sugieren fomentar la diversificación hacia condiciones no oncoológicas, incluyendo trombocitemia, hepatitis alcohólica, mielofibrosis y neuropatía periférica diabética.
Agentes prometedores en el desarrollo clínico
De los distintos fármacos en desarrollo, varios destacan como prometedores para el cáncer y otras condiciones:
- Agentes oncológicos:
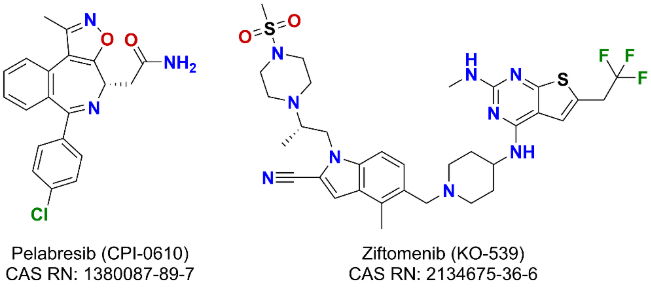
- Pelabresib (CPI-0610), un inhibidor avanzado de BET, alcanzó la fase II de ensayos para la mielofibrosis.
- El ziftomenib (KO-539), un inhibidor selectivo de molécula pequeña de la interacción menin-KMT2A proteína, recibió la designación de Terapia Breakthrough de la FDA de EE. UU. en marzo de 2024 para LMA NPM1 mutante recidivante o refractaria.
- Agentes no oncológicos:
- La apabetalona (RVX-208), un inhibidor selectivo de BET dirigido a los dominios BD2, se encuentra actualmente en Fase I/II para la enfermedad renal terminal.
- El larsucosterol (DUR-928), un oxisterol sulfatado endógeno y regulador epigenético de primera clase, está en ensayos de fase II para hepatitis alcohólica.
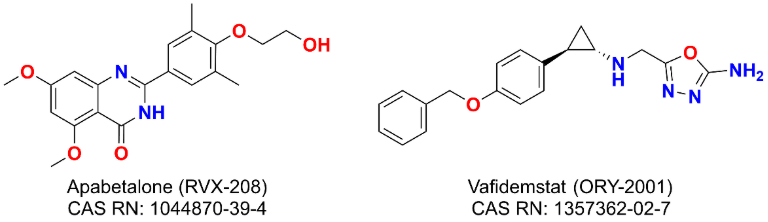
- Vafidemstat (ORY-2001) es un inhibidor selectivo de la LSD1 que se está evaluando actualmente en ensayos clínicos de fase II para el trastorno límite de la personalidad.
- Agentes aprobados recientemente:
- Modeyso (Dordaviprone) recibió la aprobación rápida de la FDA de EE. UU. en agosto de 2025 para los gliomas difusos de la línea media con mutación H3K27M en pacientes mayores de un año.
- Revuforj (Revumenib) obtuvo la aprobación de la FDA de EE. UU. en noviembre de 2024 para la leucemia mieloide aguda (LMA) con reordenamiento de KMT2A recidivante/refractaria en pacientes adultos y pediátricos.
La epigenética en la medicina personalizada
La integración de los datos epigenéticos ayuda al desarrollo de herramientas de diagnóstico, marcadores de pronóstico y métodos terapéuticos de gran precisión, en particular para las enfermedades complejas. Como se ha señalado, los fármacos epigenéticos, incluidos los inhibidores de DNMT y de HDAC, están clínicamente establecidos y siguen desarrollándose. Las terapias combinadas que combinan los fármacos epigenéticos con la quimioterapia y la inmunoterapia también mejoran la eficacia del tratamiento, lo que representa un avance clave en los métodos terapéuticos personalizados.
Otro avance clave en epigenética es el uso de estas modificaciones como biomarcadores específicos de tejido. Algunos ejemplos de estos patrones específicos de enfermedades son la hipermetilación de genes supresores de tumores en el cáncer, y la metilación aberrante y las modificaciones de histonas en pacientes con la enfermedad de Alzheimer o de Parkinson.
La identificación de estos biomarcadores epigenéticos permite la detección y el diagnóstico precoz de la enfermedad. Por ejemplo, esto podría lograrse mediante biopsias líquidas utilizadas para detectar patrones de metilación del ADN específicos del cáncer en sangre u otros fluidos corporales para diagnóstico y monitoreo no invasivos y pruebas prenatales a través de marcadores epigenéticos en sangre materna para evaluar la salud fetal. En cuanto a la prognosis, los marcadores epigenéticos pueden predecir los resultados de la enfermedad y la respuesta a la terapia. Por ejemplo, el estado de metilación predice los resultados y la probabilidad de metástasis en algunos tipos de cáncer, mientras que los cambios epigenéticos en los trastornos psiquiátricos pueden predecir la respuesta a los medicamentos.
Aplicaciones clínicas de biomarcadores epigenéticos
Los biomarcadores epigenéticos son importantes para el diagnóstico de enfermedades, el pronóstico y la toma de decisiones terapéuticas. Analizamos varias publicaciones en la colección de contenidos de CAS específicas sobre biomarcadores epigenéticos, y encontramos un aumento pronunciado a partir de 2008-2009, con algunos periodos de estancamiento (2015-2017 y 2023-2024) (véase la Figura 11).
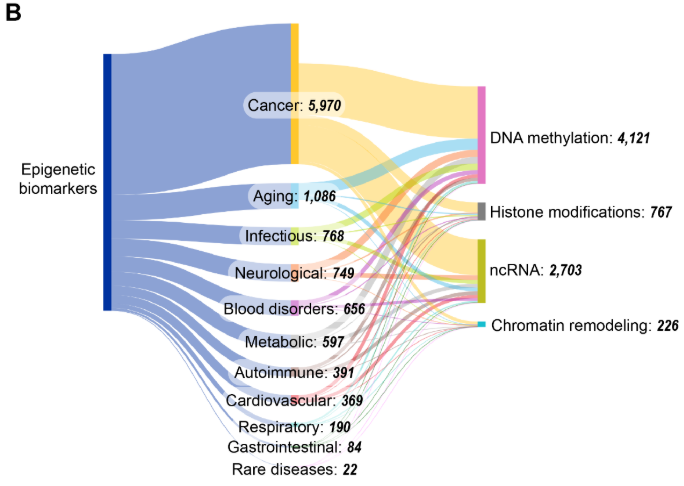
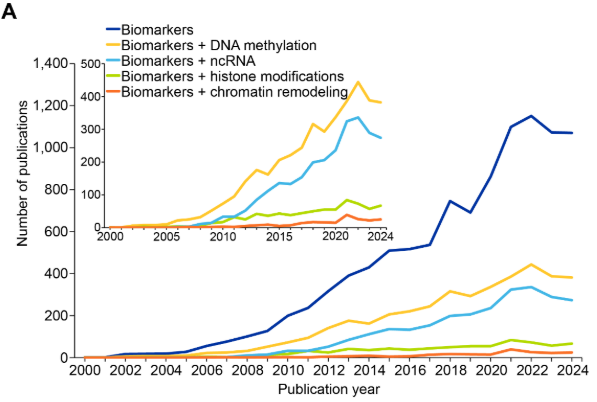
Entre los cuatro mecanismos epigenéticos principales, la metilación del ADN y el ncARN parecen ser los más estudiados, ya que las publicaciones relacionadas con la metilación del ADN y los biomarcadores de ncARN se han duplicado entre 2015 y 2022, mientras que las modificaciones de las histonas y la remodelación de la cromatina siguen siendo comparativamente poco exploradas en este contexto. Como se ve en la Figura 11B, el cáncer parece coexistir con mayor frecuencia con publicaciones relacionadas con biomarcadores epigenéticos, lo que refleja el papel bien establecido de la desregulación epigenética en la oncogénesis y la utilidad clínica de los marcadores de metilación como MGMT516 y VIM517 para el diagnóstico y el pronóstico. La importante representación de la investigación sobre el envejecimiento se alinea con los recientes avances en el desarrollo de relojes epigenéticos y sus aplicaciones en la evaluación de la edad biológica.
Biomarcadores de metilación del ADN
Los patrones aberrantes de metilación del ADN son el sello distintivo de la enfermedad, en particular la hipermetilación de los supresores de tumores, que es un biomarcador común de varios tipos de cáncer. Por ejemplo, la metilación del SEPT9 permite la detección no invasiva del cáncer colorrectal mediante la detección sanguínea como alternativa a la colonoscopia. La metilación de MGMT predice la respuesta a la temozolomida en el glioblastoma, y la hipermetilación se asocia con mejores resultados. La metilación de BRCA1 actúa como marcador diagnóstico y pronóstico asociado a un riesgo incrementado de cáncer de mama y de ovario. Cabe destacar que la metilación del ADN coocurre principalmente con la investigación de biomarcadores epigenéticos, probablemente debido a su estabilidad química, metodologías de detección establecidas y traducción clínica directa mediante pruebas aprobadas por la FDA.
Biomarcadores de modificación de histonas
Las modificaciones de histonas influyen en la estructura de la cromatina y la expresión génica, y se asocian marcas de histonas específicas con estados de enfermedad. La relativamente modesta coincidencia de modificaciones de histonas que vemos en la Figura 11B sugiere un potencial sin explotar, especialmente dada su naturaleza dinámica y su capacidad de respuesta a las intervenciones terapéuticas.
La pérdida de acetilación de la histona H4 predice un mal pronóstico en ciertos cánceres, mientras que la trimetilación de la histona H3 lisina 27 (H3K27me3) refleja una desregulación de PRC2 y se correlaciona con un mal pronóstico en cánceres de próstata y vejiga. La citrulinación de las histonas H3/H4 está relacionada con la producción de anticuerpos antiproteínas citrulinadas (ACPA), un sello distintivo de la artritis reumatoide que permite su diagnóstico y seguimiento.
A pesar de estos resultados prometedores, persisten desafíos como la naturaleza altamente inestable de las modificaciones de las histonas y su susceptibilidad a la degradación enzimática, lo que provoca una rápida pérdida de señal en cuestión de minutos tras la recopilación de la muestra. Los protocolos actuales requieren buffers de preservación especializados que contengan inhibidores de proteasa, desacetilasa y desmetilasa, lo que complica la implementación clínica rutinaria.
Biomarcadores de ncRNA
Los ncARN, incluidos los miARN, como el miR-21529 y el miR-155530, se sobreexpresan en varios tipos de cáncer y sirven como biomarcadores de diagnóstico y pronóstico en los fluidos corporales. La coocurrencia sustancial de ncARN con la investigación de biomarcadores epigenéticos refleja el creciente interés en los miARN e lncARN circulantes como biomarcadores mínimamente invasivos.
Por ejemplo, la sobreexpresión del miR-21 se asocia con el crecimiento tumoral, la invasión, la metástasis y la resistencia a la quimioterapia en el cáncer de mama, pulmón y colorrectal. Los niveles elevados de miR-208a sirven como biomarcador para el infarto agudo de miocardio (ataque cardíaco). La sobreexpresión del lncARN HOTAIR también se asocia con la metástasis y el mal pronóstico en los cánceres de mama, colorrectal y de páncreas.
Biomarcadores de remodelación de la cromatina
Los patrones de remodelación de la cromatina predicen la resistencia terapéutica, y las regiones de cromatina abiertas de las células cancerosas resistentes a los fármacos se utilizan para predecir el fracaso del tratamiento. Al igual que las modificaciones de histonas, la relativamente baja coocurrencia de la remodelación de la cromatina sugiere un potencial no explotado.
En general, el futuro de los biomarcadores epigenéticos reside en el desarrollo de tecnologías robustas y de alto rendimiento y métodos integradores. La integración multiómica que combina datos epigenéticos, genómicos, transcriptómicos y proteómicos mejorará el descubrimiento y validación de biomarcadores. La detección no invasiva de biomarcadores epigenéticos en fluidos corporales revolucionará el diagnóstico precoz y el monitoreo.
Se prevé que las herramientas computacionales avanzadas ayuden a identificar las firmas epigenéticas complejas para la estratificación de los pacientes. Por ejemplo, la edición epigenómica basada en CRISPR puede permitir la manipulación de marcas epigenéticas asociadas a la enfermedad con fines terapéuticos, potencialmente haciendo la transición de biomarcadores de herramientas diagnósticas a terapéuticas.
Implicaciones éticas, legales y sociales de la epigenética en la medicina
La epigenética tiene el potencial de transformar nuestra comprensión de la salud y la enfermedad, pero también plantea importantes desafíos éticos, legales y sociales. Afrontar estos desafíos requiere un métodos proactivo y colaborativo que equilibre las ventajas de la investigación epigenética con la necesidad de proteger los derechos de las personas y promover la justicia social. Al desarrollar directrices éticas sólidas, protecciones legales y estrategias de participación pública, podemos aprovechar el poder de la epigenética para mejorar la salud y el bienestar, al tiempo que minimizamos los posibles daños.
Consideraciones éticas
- Privacidad y discriminación: la información epigenética, al igual que los datos genéticos, es personal y puede revelar información confidencial sobre la salud, el estilo de vida y las exposiciones ambientales de una persona, por lo que requiere sólidas protecciones de privacidad. Por ejemplo, los marcadores epigenéticos que predicen el riesgo de enfermedad podrían permitir la discriminación por parte de las aseguradoras de salud mediante aumentos de primas o denegación de cobertura. Del mismo modo, la capacidad de detectar modificaciones epigenéticas a partir de comportamientos pasados plantea el riesgo de evaluaciones de salud retroactivas y discriminación laboral.
- Responsabilidad individual e impactos transgeneracionales: en relación con lo anterior, la información epigenética podría llevar a culpar a las personas de sus problemas de salud, ignorando los determinantes sociales y medioambientales generales relacionados con ella. En ocasiones, los cambios epigenéticos inducidos por factores medioambientales pueden transmitirse a las generaciones futuras. Esto plantea problemas éticos sobre las consecuencias a largo plazo de las intervenciones que alteran los marcadores epigenéticos.
Requisitos legales
- Supervisión regulatoria: la proliferación de kits de pruebas epigenéticas directas para el consumidor plantea problemas relacionados con su precisión, interpretación y regulación. Los marcos legales deben garantizar que estas aplicaciones estén basadas en la evidencia y sean éticas, evitando al mismo tiempo la comercialización prematura de tecnologías no probadas.
- Responsabilidad y propiedad intelectual: las modificaciones epigenéticas vinculadas a la exposición ambiental plantean cuestiones de responsabilidad complejas. Por ejemplo, ¿los daños provocados por las toxinas deben ser responsabilidad de los empresarios, los fabricantes o los gobiernos? La posible responsabilidad legal por el daño epigenético a los fetos provocado por la negligencia de los padres o de terceros o por la exposición ambiental requeriría una consideración cuidadosa. La comercialización de la investigación epigenética, como los biomarcadores o las terapias, plantea dudas sobre las patentes y la propiedad, y exige un equilibrio entre la innovación y el mantenimiento del acceso público a las tecnologías epigenéticas.
Implicaciones sociales
- Comprensión pública y equidad: el conocimiento público limitado de la epigenética permite que se extiendan conceptos erróneos y que proliferen las terapias no probadas (por ejemplo, las «dietas epigenéticas»). Una educación integral y una comunicación científica sólida son esenciales para solucionar este problema y mejorar la toma de decisiones fundamentadas. La investigación epigenética que vincula las exposiciones ambientales a enfermedades también puede contribuir a la estigmatización de ciertas comunidades o poblaciones, especialmente aquellas expuestas a altos niveles de contaminación o toxinas. Garantizar un acceso equitativo a las terapias epigenéticas y prevenir la exacerbación de las disparidades en salud requiere intervenciones normativas conscientes que eliminen las barreras socioeconómicas.
- Estrategias de implementación: una gobernanza eficaz requiere directrices éticas claras para recopilar, usar y compartir los datos epigenéticos; marcos legales actualizados que afronten los nuevos problemas de la información epigenética; participación pública que fomente la confianza y el consentimiento informado, y cooperación internacional que garantice estándares uniformes en todas las jurisdicciones. Al desarrollar protecciones sólidas y, al mismo tiempo, promover la innovación responsable, la sociedad puede aprovechar el potencial transformador de la epigenética mientras protege los derechos individuales y promueve la equidad en salud.
Perspectivas para el futuro de la epigenética
El panorama de la investigación en epigenética ha experimentado una transformación notable en la última década; ha pasado de ser un área especializada de la biología molecular a una disciplina biomédica convencional con profundas implicaciones para la salud humana y la intervención terapéutica. La aplicación clínica de la investigación epigenética ha logrado un éxito notable, con 15 medicamentos aprobados por la FDA que validan los objetivos epigenéticos como terapéuticamente viables. Los 36 ensayos clínicos en curso y en distintas fases de desarrollo demuestran que hay inversión sostenida y confianza en las terapias epigenéticas, con una diversificación alentadora fuera de la oncología: los ensayos abarcan ahora enfermedades metabólicas, neurológicas, inflamatorias y raras.
Este cambio refleja el creciente reconocimiento de que los factores ambientales como la dieta, el estrés, las toxinas y las elecciones de estilo de vida crean cambios epigenéticos heredables con implicaciones transgeneracionales. La integración de los datos de exposición ambiental con los perfiles epigenéticos personales permite una evaluación personalizada del riesgo y estrategias de intervención, lo que representa un cambio fundamental hacia la medicina preventiva de precisión.
El futuro de la epigenética es prometedor y tiene un inmenso potencial para hacer avanzar nuestra comprensión de la biología y mejorar la salud humana. Sin embargo, para hacer realidad este potencial será necesario superar importantes retos, como las limitaciones tecnológicas, los problemas éticos y la complejidad de la regulación de la epigenética. Al fomentar la colaboración interdisciplinaria, invertir en tecnologías innovadoras y afrontar las implicaciones éticas y sociales, el campo de la epigenética puede seguir ofreciendo descubrimientos innovadores y traducirlos en beneficios clínicos y sociales importantes.