Resumo executivo
As tecnologias de reprodução assistida (ART) revolucionaram a medicina reprodutiva, oferecendo esperança a milhões de pessoas que enfrentam problemas de fertilidade por meio de métodos como inseminação artificial e edição de genes de última geração. Embora técnicas estabelecidas como fertilização in vitro e injeção intracitoplasmática de espermatozoides sejam amplamente usadas atualmente, tecnologias emergentes como gametogênese in vitro, terapia genética e terapias baseadas em células-tronco estão expandindo os limites do que é possível.
ART é um campo que avança rapidamente, mas o uso de certas tecnologias novas e emergentes em seres humanos ainda é altamente experimental, rigorosamente regulamentado e cercado de desafios éticos e legais. Muitas inovações em ART estão sendo testadas apenas em modelos animais, mas algumas fizeram a transição com sucesso para aplicações humanas, incluindo testes genéticos pré-implante, terapia de reposição mitocondrial, imagens em lapso de tempo e maturação in vitro. Além disso, a inteligência artificial está transformando a medicina reprodutiva ao permitir a seleção precisa de embriões, otimizar protocolos clínicos e prever resultados de tratamentos.
Este relatório explora dados da Coleção de conteúdo do CASTM para delinear o progresso da pesquisa em ART e identificar os principais conceitos e desafios emergentes para entender melhor como a ART está moldando o futuro da saúde reprodutiva.
Estado da Arte: uma introdução
A tecnologia de reprodução assistida (ART) abrange um amplo espectro de técnicas médicas destinadas a ajudar indivíduos e casais a superar os desafios da infertilidade e possibilitar a concepção de filhos. A infertilidade afeta aproximadamente 10% a 15% dos casais no mundo todo, tornando a ART um componente essencial da saúde moderna.
Os procedimentos de ART normalmente envolvem o manuseio de óvulos, espermatozoides e embriões para alcançar a fertilização e a implantação. Técnicas como FIV e criopreservação são agora práticas padrão em clínicas de fertilidade em todo o mundo. Nos últimos anos, tecnologias emergentes como inteligência artificial (IA), testes genéticos e pesquisa com células-tronco refinaram ainda mais a ART, melhorando suas taxas de sucesso enquanto abordam as implicações éticas e sociais. Além disso, inovações experimentais como a gametogênese in vitro (IVG) poderiam proporcionar gametas para indivíduos que não conseguem produzir os seus próprios.
No entanto, muitas questões éticas permanecem em torno de várias inovações de ART, e muitas ainda dependem fortemente de modelos animais. Essa abordagem fornece insights valiosos sobre a biologia reprodutiva e os efeitos de várias intervenções de ART, mas mostra que muitas inovações ainda estão longe do uso clínico em humanos.
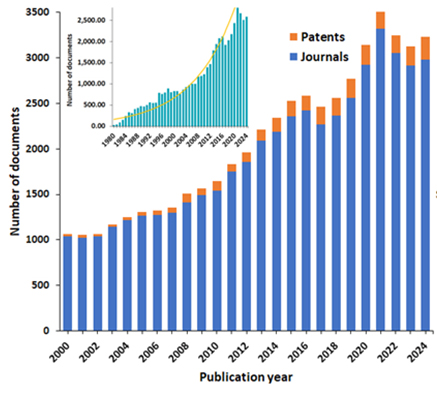
Exploramos dados do Coleção de conteúdo do CASTM, o maior repositório de informações científicas com curadoria humana, para delinear o progresso da pesquisa em ART. O crescimento nas publicações desde o ano 2000 demonstra o amplo interesse de pesquisa e comercial nessas inovações, com o número de publicações relacionadas à ART triplicando nas últimas duas décadas (veja a Figura 1).
Métodos atuais de tecnologia de reprodução assistida
Os esforços para superar a infertilidade têm uma longa história, começando com o primeiro caso documentado de inseminação artificial em 1790. A primeira gravidez alcançada por meio da fertilização in vitro de um oócito humano aconteceu em 1973, embora tenha terminado em aborto espontâneo. Em 1978, ocorreu a primeira gravidez e nascimento vivo bem-sucedidos de fertilização in vitro e, na década de 1980, a fertilização in vitro se tornou predominante.
Mais de 8 milhões de bebês nasceram com fertilização in vitro e os métodos ART são agora partes bem estabelecidas da medicina reprodutiva no mundo todo. Os métodos tradicionais mais comuns são:
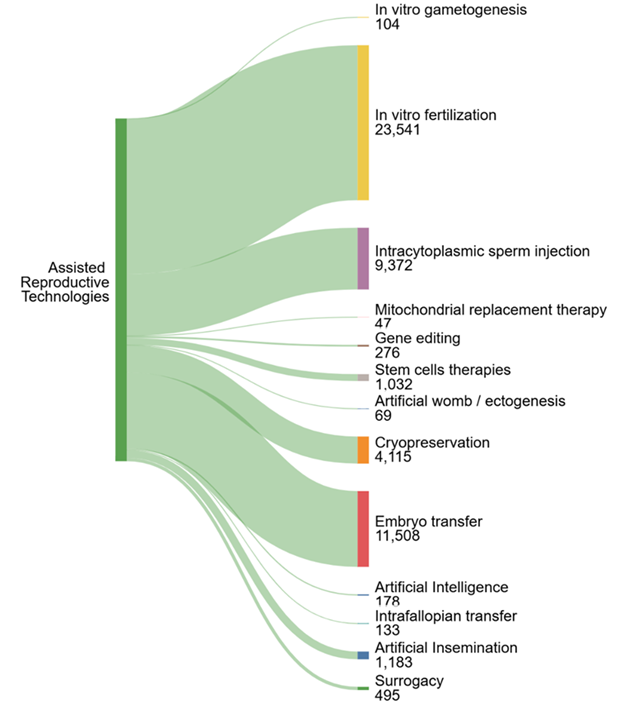
- A fertilização in vitro é um dos pilares do tratamento de fertilidade humana, possibilitando milhões de nascimentos no mundo todo. A fertilização in vitro inclui estimulação ovariana com medicamentos de fertilidade para produzir múltiplos óvulos, recuperação de óvulos maduros por meio de um pequeno procedimento cirúrgico, fertilização de óvulos com esperma em uma placa de laboratório e transferência dos embriões resultantes para o útero. Atualmente totalmente integrado à prática clínica, ele é aplicado com sucesso em casos de infertilidade tubária, endometriose, infertilidade masculina e infertilidade inexplicada. As taxas de sucesso variam de acordo com a idade, com as maiores taxas de sucesso (30-40% por ciclo) para mulheres com menos de 35 anos. Em nossa análise da Coleção de Conteúdo do CAS, descobrimos que a FIV constitui a maior parte dos documentos relacionados à TRA (ver Figura 2).
- A inseminação artificial é um procedimento médico no qual o esperma é introduzido no trato reprodutivo da mulher para facilitar a fertilização e a gravidez. A amostra de esperma é coletada, lavada e concentrada para isolar espermatozoides saudáveis e, em seguida, colocada diretamente no útero (inseminação intrauterina, IIU) ou colo do útero (inseminação intracervical, ICI) durante a ovulação. É aplicado principalmente em casos de infertilidade masculina leve, infertilidade inexplicável ou problemas de muco cervical. É mais simples e menos invasivo que a fertilização in vitro. As taxas de sucesso são normalmente de 10 a 20% por ciclo, dependendo de fatores como idade e qualidade do esperma.
- Transferência intrafalopiana de gametas (GIFT) é um procedimento que ajuda as mulheres a engravidar colocando óvulos e espermatozoides diretamente nas trompas de Falópio. Os óvulos e os espermatozoides são coletados e misturados antes de serem colocados na trompa de Falópio por laparoscopia, possibilitando que a fertilização ocorra naturalmente no corpo. Atualmente esse método é menos comum devido aos avanços na fertilização in vitro.
- A transferência intrafalópica do zigoto (ZIFT) é como a fertilização in vitro, mas o óvulo fertilizado (zigoto) é transferido para a trompa de Falópio em vez do útero. É aplicado a pacientes inférteis com trompas de Falópio saudáveis. Ele combina os benefícios da FIV e da GIFT, mas é menos comum atualmente.
- A criopreservação (preservação da fertilidade) envolve o congelamento e armazenamento de células reprodutivas, como óvulos, espermatozoides ou embriões, para uso futuro. A criopreservação é agora um procedimento de rotina para embriões e espermatozoides e está se tornando mais comum para oócitos. É aplicado para a preservação da fertilidade, como para pacientes com câncer submetidos a quimioterapia ou radioterapia, embriões excedentes de fertilização in vitro ou pessoas que estão adiando a gravidez por motivos pessoais ou profissionais.
- A doação de óvulos e espermatozoides pode ajudar as pessoas a terem filhos se não conseguirem produzir óvulos ou espermatozoides saudáveis por si mesmas. Os óvulos ou espermatozoides são doados por terceiros e usados em procedimentos de ART, como FIV ou inseminação intrauterina, para alcançar a gravidez. Esse método é amplamente utilizado por mulheres idosas, casais do mesmo sexo ou pais solteiros.
- A substituição gestacional envolve uma mulher que gera e dá à luz uma criança para outra pessoa ou casal usando seus embriões (substituição gestacional) ou seu próprio óvulo (substituição tradicional). Enquanto na substituição tradicional o óvulo da substituta é fertilizado com esperma (por meio de IUI ou FIV), tornando-a a mãe biológica, na substituição gestacional, a substituta carrega um embrião criado por meio de FIV com óvulos e esperma dos pais ou doadores pretendidos, de modo que ela não tem vínculo genético com a criança.
Métodos de ART de crescimento mais rápido: IA e gametogênese in vitro
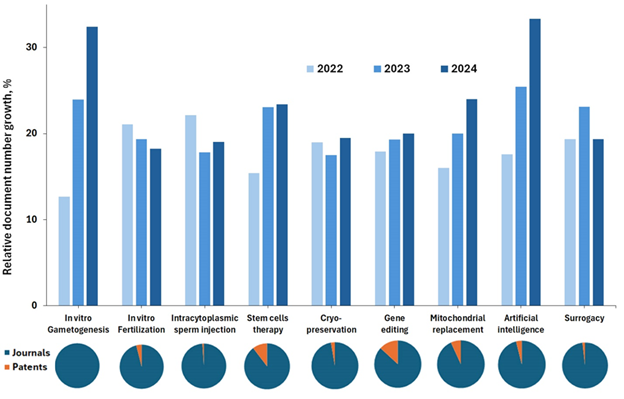
Os métodos tradicionais de ART foram inovadores, mas apresentam muitas desvantagens, incluindo altos custos, estresse físico e emocional, riscos à saúde e questões éticas e legais. Novas inovações estão oferecendo maior esperança para pessoas que lutam contra a infertilidade e nossa análise da Coleção de conteúdo do CAS mostra que o uso de IA em ART e gametogênese in vitro (IVG) são os novos métodos que mais crescem nos últimos três anos (2022-2024) (ver a Figura 3).
IA em ART
Para a seleção de embriões, os algoritmos de IA analisam imagens de embriões para avaliar sua qualidade e o potencial de implantação bem-sucedida. Esses algoritmos utilizam:
- Imagem por lapso de tempo: a IA monitora o desenvolvimento do embrião ao longo do tempo, avaliando fatores como morfologia, padrões de divisão celular e dinâmica.
- Dados morfocinéticos: algoritmos preveem a probabilidade de um embrião se desenvolver em uma gravidez viável, identificando características sutis não visíveis ao olho humano.
A IA também ajuda a melhorar a seleção de espermatozoides identificando os espermatozoides mais móveis e morfologicamente normais e por meio de verificações de integridade do DNA, que avaliam os níveis de fragmentação do DNA nos espermatozoides para selecionar os candidatos mais saudáveis.
Os modelos de aprendizado de máquina analisam múltiplos pontos de dados para prever a taxa de sucesso da FIV, incluindo histórico do paciente (idade, níveis hormonais, fatores de estilo de vida), dados clínicos (marcadores de reserva ovariana, receptividade endometrial) e métricas de qualidade do embrião. A IA pode otimizar os protocolos de estimulação ovariana personalizando as dosagens de medicamentos com base nas respostas específicas da paciente e prevendo as respostas ovarianas à estimulação, reduzindo o risco da síndrome de hiperestimulação ovariana (OHSS). Identificar o momento ideal para intervenções clínicas, como a retirada de óvulos e a transferência de embriões, é fundamental para o sucesso dos ciclos de ART e os pesquisadores viram melhorias notáveis com modelos baseados em IA.
Nossa análise revelou um aumento de patentes relacionadas a inovações baseadas em IA, como uma patente atribuída à Cornell University em 2025 que utiliza aprendizado de máquina e/ou deep learning para analisar e prever o status de ploidia de um embrião. A Univfy também patenteou recentemente métodos auxiliados por computador para avaliar a probabilidade de um paciente ter uma falha na fertilização in vitro ou um resultado intermediário do tratamento.
A automação baseada em IA agiliza processos nos laboratórios de ART, incluindo o monitoramento e controle das condições da incubadora, a padronização da classificação de embriões para minimizar o erro humano e o gerenciamento de protocolos de criopreservação. Aproveitando grandes conjuntos de dados de clínicas e estudos de pesquisa para identificar tendências e fatores que influenciam o sucesso da ART, a IA pode reconhecer padrões nos dados de pacientes e embriões e aprimorar os protocolos de tratamento. Assim, os usos da IA na ART são extensos e podem fornecer melhores resultados para muitos pacientes.
IVG em ART
IVG é uma tecnologia experimental que possibilita a criação de espermatozoides ou óvulos a partir de células somáticas, como células da pele ou do sangue. A IVG envolve a diferenciação de células-tronco pluripotentes (PSCs), como células-tronco embrionárias (ESCs) ou células-tronco pluripotentes induzidas (iPSCs), em gametas. Esse processo imita a progressão natural da gametogênese, em que as células germinativas primordiais se desenvolvem em gametas maduros por meio de intrincadas vias moleculares e celulares. O que torna isso animador é que poderia disponibilizar gametas para aqueles que não conseguem produzir óvulos ou espermatozoides viáveis.
Os pesquisadores conseguiram produzir gametas funcionais em modelos animais, incluindo camundongos, levando a uma prole saudável. No entanto, a aplicação dessas técnicas em sistemas humanos ainda está em desenvolvimento devido à complexidade da gametogênese humana e a importantes preocupações éticas. Em 2024, cientistas da Universidade de Kyoto criaram precursores de gametas humanos a partir de células-tronco pluripotentes induzidas (iPSCs), mas ainda há obstáculos consideráveis até que essa técnica possa ser amplamente utilizada.
Apesar das recentes descobertas importantes em IVG, os problemas éticos persistem. A criação e manipulação de embriões, ou seja, a criação e o descarte de um grande número de embriões, devem ser abordadas antes da implementação. A segurança e a eficácia também exigem ampla validação antes da aplicação clínica.
Métodos de maior interesse comercial: terapia celular e edição de genes
Como se vê nos gráficos circulares na parte inferior da Figura 3, a edição de genes e as terapias baseadas em células-tronco têm a maior fração de patente de todos os documentos (13% e 10%, respectivamente), o que é indicativo de alto interesse comercial.
Terapias baseadas em células-tronco
As células-tronco podem se diferenciar em tipos de células reprodutivas, como células-tronco embrionárias ou células-tronco pluripotentes induzidas para formar oócitos ou espermatozoides; elas secretam sinais parácrinos que melhoram o reparo tecidual e a função celular; e podem se integrar aos tecidos reprodutivos, contribuindo para a recuperação estrutural e funcional.
As aplicações de terapias baseadas em células-tronco na ART poderiam acionar numerosas descobertas importantes:
- O declínio da reserva ovariana relacionado à idade é uma das principais causas de infertilidade. As células-tronco mesenquimais e as células-tronco derivadas da medula óssea mostraram-se promissoras na regeneração do tecido ovariano, melhorando a foliculogênese e restaurando o equilíbrio hormonal.
- O transplante de células-tronco demonstrou potencial de restauração da espermatogênese em indivíduos com azoospermia ou outras formas de infertilidade masculina. As células-tronco espermatogônicas (SSCs) podem ser colhidas, cultivadas e reintroduzidas nos testículos para reiniciar a produção de espermatozoides.
- Condições como a síndrome de Asherman e o endométrio fino representam desafios significativos para o sucesso da implantação. Células-tronco endometriais (ESCs) e MSCs foram exploradas para regenerar e aumentar a receptividade endometrial.
- Como observado, a derivação de gametas (óvulos e espermatozoides) de células-tronco pluripotentes via IVG abre novas possibilidades para a paternidade biológica.
Vários tipos de células-tronco usados na ART estão resumidos na Tabela 1.
| Tipo de células-tronco | Órgão | Aplicado a | Efeito / Estimulação |
|---|---|---|---|
| Derivado de tecido adiposo (ADSC) |
Testículo |
Rato |
|
|
Ovário |
Camundongo, rato |
||
|
Cordão umbilical (UCSC) |
Testículo |
Mouse |
|
|
Endométrio |
Humano |
||
|
Células-tronco pluripotentes induzidas (iPSC) |
Testículo |
Humano |
|
|
Espermatogonial (SSC) |
Testículo |
Macaco |
|
|
Oogonial (OSC) |
Ovário |
Mouse |
|
|
Líquido amniótico (AFSC) |
Ovário |
Mouse |
|
|
Medula óssea (BMSC) |
Ovário |
Mouse |
|
|
Embrionárias (ESC) |
Ovário |
Mouse |
|
|
Células progenitoras endometriais (EPC) |
Endométrio |
Mouse |
Tabela 1: Tipos de células-tronco em ART.
Edição de genes
A edição de genes na ART tem o potencial de reduzir doenças hereditárias, melhorar a seleção de embriões e aumentar as taxas de sucesso reprodutivo. Pode corrigir mutações em embriões associadas a doenças hereditárias, como fibrose cística, anemia falciforme e doença de Huntington, impedindo sua transmissão para as gerações futuras. Outra aplicação da edição de genes na ART é o aprimoramento da seleção de embriões — a triagem genética combinada com a edição pode melhorar a qualidade do embrião ao selecionar embriões com o maior potencial de implantação e desenvolvimento bem-sucedidos. A edição de genes também pode ajuda a tratar a infertilidade identificando e corrigindo as causas genéticas da infertilidade, como anormalidades cromossômicas ou mutações que afetam a função dos gametas.
O sistema CRISPR-Cas9 é a ferramenta mais proeminente na edição de genes. Visando sequências de DNA específicas, o CRISPR-Cas9 pode adicionar, excluir ou alterar genes, tornando-se uma tecnologia valiosa no tratamento de distúrbios genéticos hereditários em embriões criados por fertilização in vitro.
No entanto, essa técnica é controversa devido ao potencial de "bebês projetados" e consequências não intencionais. Atualmente, a edição de genes em seres humanos, especialmente a edição de linha germinativa, que afeta óvulos, espermatozoides ou embriões e pode ser transmitida para as gerações futuras, é altamente restrita ou proibida em muitos países devido a preocupações.
Algumas patentes notáveis foram atribuídas nesse campo recentemente; por exemplo, a Fujita Academy recebeu uma patente em 2024 para um método de teste de aneuploidia cromossômica de embriões usando RNA não codificante para tratamento de infertilidade. Esse processo testa embriões cultivados in vitro e cria um perfil de RNA extracelular realizando aprendizado de máquina e determinando a presença ou ausência de aneuploidia cromossômica.
Métodos novos e adicionais em ART
Nossa análise da Coleção de conteúdo do CAS revela vários outros métodos novos que estão ganhando força na ART:
Triagem genética
Uma das tendências mais significativas na ART é a integração de técnicas avançadas de rastreio genético. O Teste genético pré-implantação (PGT) tornou-se cada vez mais sofisticado, possibilitando a detecção de anomalias cromossômicas e distúrbios de gene único em embriões antes da implantação.
- A técnica PGT-A (rastreamento de aneuploidia) rastreia anormalidades cromossômicas, principal causa de falha na implantação e do aborto espontâneo. Os avanços na nova geração de sequenciamento (NGS) melhoraram a precisão e a eficiência do PGT-A, levando a taxas de sucesso mais altas nos ciclos de FIV.
- O PGT-M (distúrbios monogênicos) é usado para identificar embriões portadores de mutações genéticas específicas, permitindo que casais com doenças hereditárias tenham filhos saudáveis. O desenvolvimento do CRISPR-Cas9 e de outras ferramentas de edição de genes aumentou ainda mais o potencial para corrigir defeitos genéticos no estágio embrionário.
- O teste PGT-SR (rearranjos estruturais) é projetado para indivíduos com translocações ou inversões cromossômicas, ajudando a identificar embriões com estruturas cromossômicas equilibradas.
Esses avanços não somente aumentam a probabilidade de uma gravidez bem-sucedida, como também reduzem o risco de transmissão de distúrbios genéticos, oferecendo uma abordagem mais personalizada à medicina reprodutiva.
Terapias de substituição mitocondrial
A terapia de substituição mitocondrial (MRT), também conhecida como doação mitocondrial, é uma técnica que visa evitar a transmissão de distúrbios do DNA mitocondrial (mtDNA) de mãe para filho. Isso envolve a substituição de mitocôndrias defeituosas em um óvulo ou embrião por mitocôndrias saudáveis de um doador.
A MRT foi utilizada para criar embriões com material genético de três indivíduos: a mãe, o pai e um doador mitocondrial (os chamados "bebês de três pais"). A MRT traz problemas éticos relacionados à modificação genética e aos efeitos de longo prazo sobre as gerações do Futuro. Entretanto, esse procedimento é benéfico para mulheres com distúrbios mitocondriais que desejam ter filhos geneticamente relacionados. Atualmente, a tecnologia é regulamentada de formas variadas entre os países, com alguns permitindo seu uso sob diretrizes rígidas e outros proibindo.
Há algumas diferenças importantes entre MRT e edição de genes, conforme descrito na Tabela 2:
| Funcionalidade | Edição de genes | Terapia de substituição mitocondrial |
|---|---|---|
|
Alvo |
DNA nuclear |
DNA mitocondrial |
|
Escopo |
Amplo (doenças, características, viabilidade) |
Específico (somente doenças mitocondriais) |
|
Preocupações éticas |
Bebês projetados, edições germinativas |
Bebês com três pais, preocupações com a identidade |
|
Técnicas |
CRISPR, edição de bases, edição primária |
Transferência pronuclear (PNT), transferência do fuso materno (MST), transferência do corpo polar (PBT) |
Injeção intracitoplasmática de espermatozoides (ICSI)
A ICSI é um procedimento de ART que envolve a injeção de espermatozoides vivos diretamente no citoplasma de um óvulo maduro com uma ferramenta de micromanipulação. O óvulo fertilizado é então cultivado e transferido como na FIV. Representa um refinamento da FIV e é o tratamento mais comum e bem-sucedido para a infertilidade masculina causada por problemas de esperma, como baixa contagem de espermatozoides, baixa motilidade ou morfologia anormal, ou quando tentativas anteriores de FIV falharam. As taxas de sucesso são semelhantes à FIV, mas a ICSI pode melhorar consideravelmente as taxas de fertilização em casos de infertilidade masculina.
Sistemas aprimorados de cultura de embriões
Há muitas maneiras de melhorar os sistemas de cultura de embriões, incluindo um novo tipo de design de plataforma de cultura que cria um microambiente melhor para os embriões. Novas formulações de meios, incluindo antioxidantes para reduzir o dano oxidativo e melhorar o desenvolvimento do blastocisto, também estão sendo pesquisadas, assim como os sistemas baseados em perfusão que usam fluxo dinâmico de meios em vez de cultura estática.
Os avanços em imagens de lapso de tempo e meios de cultura otimizados também permitem o monitoramento constante do desenvolvimento do embrião, possibilitando uma melhor seleção para transferência e aumentando as taxas de implantação.
Aprimoramentos da criopreservação
As técnicas de criopreservação em ART foram aprimoradas de várias maneiras, incluindo vitrificação, processo de congelamento rápido que evita a formação de cristais de gelo, melhorando assim as taxas de sobrevivência de gametas e embriões congelados. Os pesquisadores também estão desenvolvendo crioprotetores aprimorados e otimizados; por exemplo, tanques de vapor que armazenam tecidos na fase de vapor do nitrogênio em vez de mergulhá-los em nitrogênio líquido oferecem melhores taxas de sobrevivência para óvulos, espermatozoides e embriões congelados.
Inovações na preservação da fertilidade
Técnicas como a criopreservação de tecido ovariano e o desenvolvimento de ovários artificiais estão avançando, beneficiando pessoas que enfrentam tratamentos médicos que afetam a fertilidade. A técnica de rejuvenescimento ovariano é usada para estimular os ovários a produzir novos óvulos, principalmente em mulheres com reserva ovariana diminuída ou falência ovariana prematura. Pode incluir a injeção de plasma rico em plaquetas (PRP) nos ovários para estimular o reparo do tecido e a produção de óvulos, ou células-tronco para regenerar o tecido ovariano. A técnica ainda é experimental com resultados variados nos primeiros estudos.
Tecnologias não invasivas e automatizadas
Imagens de lapso de tempo e o monitoramento constante de embriões sem a necessidade de manuseio manual melhoram a seleção de embriões e reduzem o estresse sobre os embriões. Os sistemas de FIV automáticos estão sendo integrados aos laboratórios para melhorar a eficiência e a uniformidade de processos como fertilização e transferência de embriões. Estão sendo desenvolvidas formas não invasivas de testes genéticos para avaliar a saúde genética dos embriões, como o uso de meios de cultura em vez de biópsia invasiva, para minimizar os riscos.
Úteros artificiais
A pesquisa sobre ectogênese, ou tecnologia de útero artificial, visa apoiar o desenvolvimento de embriões fora do corpo humano. Essa tecnologia oferece soluções para pessoas que não conseguem levar a gravidez a termo devido a razões médicas ou anatômicas e promove o cuidado neonatal dando suporte a bebês extremamente prematuros.
Pesquisa de ART em modelos animais
Como muitos métodos de ART levantam preocupações éticas e legais, os pesquisadores precisam contar com modelos animais para desenvolver e otimizar essas técnicas. Os modelos animais são indispensáveis na pesquisa de ART devido às suas semelhanças biológicas e fisiológicas com os seres humanos e ao seu papel no estudo dos processos reprodutivos específicos da espécie. Além disso, eles oferecem um ambiente controlado para estudar os mecanismos de reprodução, testar novas tecnologias e avaliar a segurança e a eficácia das intervenções de ART.
Modelos animais comuns em pesquisas de ART incluem:
- Roedores (camundongos e ratos) devido a seus curtos ciclos reprodutivos, facilidade de manipulação genética e baixo custo.
- Pecuária (bovinos, ovinos e caprinos), que pode contribuir para a eficiência agrícola e a conservação da vida selvagem, adaptando técnicas para espécies ameaçadas de extinção.
- Primatas não humanos porque são os modelos mais próximos dos humanos em biologia reprodutiva.
- Peixe-zebra, que têm um modelo único de embriogênese precoce devido à sua fertilização externa e embriões transparentes.
- Modelos de vida selvagem que auxiliam os esforços globais de conservação, aumentando a diversidade genética e a recuperação populacional.
Os modelos animais continuam sendo indispensáveis na pesquisa de ART, servindo como uma ponte para garantir que as aplicações em humanos sejam seguras e eficazes. Na Tabela 3, comparamos as técnicas usadas em modelos animais e humanos:
| Técnica | Animais modelo | Humanos |
|---|---|---|
|
FIV e ICSI |
Totalmente estabelecido; otimizado em animais |
Amplamente utilizado clinicamente |
|
Edição de genes |
Comumente usado para pesquisa e testes |
Limitado à pesquisa; sem uso clínico da linha germinativa |
|
Criopreservação |
Bem estudado em animais |
Usado clinicamente de forma rotineira |
|
Mitocondrial |
Testado extensivamente em animais |
Aprovado em alguns países para uso clínico |
|
Úteros artificiais |
Bem-sucedido em ovelhas |
Fase pré-clínica; sem aplicações em humanos |
|
IVG (gametas de células-tronco) |
Os gametas funcionais foram obtidos em camundongos |
Ainda não aplicável |
Desafios e considerações éticas
Embora as metodologias ART sejam imensamente promissoras, apresentam dificuldades únicas e considerações éticas. A segurança também deve ser considerada, pois os efeitos de longo prazo de muitos procedimentos ainda são desconhecidos. Consequentemente há várias áreas problemáticas quanto à implementação dessas inovações:
- Ética relacionada ao embrião: Criar mais embriões do que o necessário levanta preocupações sobre o que acontece com os embriões não utilizados. Alguns consideram o descarte de embriões como algo eticamente problemático.
- Direitos parentais e da criança: O uso de doadores de óvulos e espermatozoides e substitutos introduz complexidades legais e emocionais em relação aos direitos parentais e ao direito da criança de conhecer suas origens genéticas. O uso de gametas ou embriões de indivíduos falecidos levanta questões sobre o consentimento e o bem-estar da criança resultante. Preconceitos sociais e obstáculos legais podem afetar o acesso de casais do mesmo sexo ou indivíduos únicos à ART.
- Questões legais e regulatórias: as práticas e leis de ART variam entre os países, levando a inconsistências éticas. Pessoas que viajam para países com leis de ART mais brandas podem explorar brechas, complicando a supervisão ética e a aplicação. O uso de IA e dados genéticos na ART também levanta preocupações sobre a confidencialidade do paciente e o potencial uso indevido de informações confidenciais.
Talvez as questões mais complicadas envolvam a ética genética e tecnológica. Tecnologias como a CRISPR usadas em ART levantam preocupações sobre consequências não intencionais, mudanças hereditárias e implicações sociais da alteração da genética humana. De fato, as alterações feitas nas células germinativas são hereditárias, o que significa que afetam as gerações futuras. Isso gera questões éticas porque as gerações futuras não podem consentir com essas modificações.
Há temores de que a edição de genes possa ser usada para aprimoramentos não terapêuticos (por exemplo, seleção de inteligência, aparência ou capacidade atlética), levando à desigualdade social e a práticas semelhantes à eugenia. Além disso, alguns grupos argumentam que alterar o DNA humano é "brincar de Deus" ou interfere nos processos naturais.
As preocupações com a segurança também devem ser abordadas antes que as inovações de ART possam ser amplamente utilizadas em ambientes clínicos. Mais uma vez, há preocupações com a edição de genes devido à falta de dados suficientes sobre as consequências de longo prazo e possíveis efeitos fora do alvo. Mutações indesejadas podem ter consequências graves para os indivíduos e para as gerações futuras, o que torna crucial conhecer completamente os possíveis efeitos de longo prazo antes da aplicação clínica. Até mesmo ferramentas precisas de edição de genes, como o CRISPR, podem às vezes fazer edições em locais não intencionais do genoma ("off-target effects"), o que pode levar a complicações de saúde imprevistas.
As agências regulatórias estão se envolvendo com a comunidade científica para estabelecer estruturas para o uso seguro e ético das tecnologias de edição de genes. Há uma urgência crescente em envolver o público em debates sobre as implicações éticas, legais e sociais da edição de genes. A Organização Mundial da Saúde (OMS) solicitou um Registro Global de pesquisas de edição de genes humanos e uma supervisão mais rigorosa, e o Comitê Internacional de Bioética da UNESCO recomendou uma moratória para a edição de linhas germinativas.
Vários países têm regras diferentes em relação à ART. Por exemplo, em 2023, o Reino Unido aprovou terapias baseadas em CRISPR para o tratamento de doenças do sangue como anemia falciforme e beta-talassemia, marcando um passo significativo para a edição de genes somáticos. A edição da linha germinativa nos EUA não é proibida, mas é fortemente restrita, e em muitos outros países, incluindo nações europeias e Austrália, a prática é proibida.
O futuro da ART
As tecnologias emergentes em ART estão ampliando os limites da medicina reprodutiva, oferecendo esperança aos indivíduos que enfrentam infertilidade, ao mesmo tempo levantando profundas questões éticas e sociais. Da seleção de embriões baseada em IA à gametogênese in vitro e edição de genes, esses avanços prometem redefinir a paternidade.
No entanto, a aplicação dessas inovações na prática clínica exige uma consideração cuidadosa da segurança, da acessibilidade e das implicações éticas para garantir um uso equitativo e responsável. Quando uma inovação ART se mostra bem-sucedida em modelos animais, ela avança para ensaios clínicos em humanos, começando com estudos pequenos e cuidadosamente monitorados. Inovações como imagens com lapso de tempo e seleção de embriões baseada em IA passaram da teoria ou da pesquisa em animais para o uso humano após uma validação rigorosa.
As questões relacionadas à ART são complexas e a ciência ainda tem muito a aprender até que mais dessas descobertas importantes possam ser levadas à prática clínica. No entanto, como mostra nossa análise, abordagens inovadoras às tecnologias reprodutivas são um farol de esperança e um testemunho da engenhosidade científica.