世界保健機関(WHO)は、適切な治療を受けても死滅/不活化しない微生物を「耐性菌」と定義しています。耐性菌の増加には多数の要因があります。米国疾病予防管理センター(CDC)によると、毎年280万件以上の抗生物質耐性菌感染が発生し、35,000人以上が死亡しています。心配なことに、世界銀行の予測では、この数は2050年までに年間1,000万人まで増加する可能性があるということです。
そのため、WHOは薬剤耐性菌を健康上の主要な懸念事項トップ10のうちのひとつと宣言しており、新たな解決策が早急に求められています。
抗生物質薬耐性には多数の要因が存在する
抗生物質耐性は、内在的な要因と後天的な要因の両方から生じます。内在的要因には、細胞壁透過性、薬剤標的の修飾、薬剤排出ポンプの活性化、そして抗生物質の酵素分解などがあります。後天的な獲得耐性は、新たな遺伝物質の獲得や生存を媒介する細菌ゲノムの変異によって生じます。
図1. 細菌で見られる一般的な抗菌剤耐性のうち、変異や耐性プラスミドに由来するものの4つのメカニズム。A. 細胞壁の透過性が変化し、細菌への抗菌薬の侵入を減少または阻止する。B. 薬剤標的の改変/欠失によって薬剤の結合力が低下し、有効性が低下する。C. 排出ポンプが抗菌治療に反応して発現し、抗生物質が効果を発揮する前に排出されてしまう。D. 酵素分解によって抗生物質の効力が阻害される。新しい抗菌治療の必要性
抗生物質にはさまざまな種類があります。それらは、それぞれの構造、そして体内で細菌にどのように作用するかによって分類されます。
表1. 抗生物質のさまざまなクラス
さまざまな治療法が確立されているにもかかわらず、多くの感染症が既存抗生物質による治療に耐性を持ち始めています。関連死の増加が推定されることと相まって、細菌感染症への対処方法を再考することが急務となっています。
新しい抗菌剤が直面する課題
抗菌剤耐性が増加している背景にはさまざまな側面があるものの、抗菌剤耐性の発生率に対して新しい治療法の開発速度が遅いことから、その状況はさらに悪化しています。
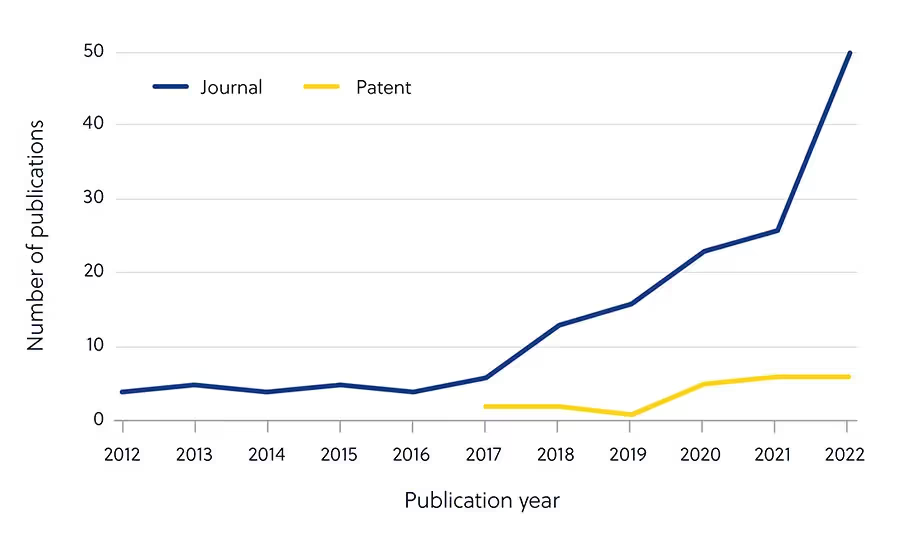
このことは抗菌剤耐性に関する学術誌の発表件数と比較して、特許件数の割合が低いことから明らかです(図2)。これは、新しい抗菌薬の開発にあたり、学術機関の研究者がより重要な役割を担っていること、そしてそういった取り組みはすぐ市販薬には結びつかないことを示しています。
図2. 過去10年間(2012年~2022年)における抗菌研究分野の年間論文発表件数と特許件数(それぞれ青と黄色の棒で示す)。これは、抗菌開発を困難にしているいくつかの要因によって説明することができます。微生物が抗菌剤に抵抗するために利用できる多くの内在的または後天的なメカニズム(図1)以外にも、開発を困難にしている幅広い要因があります(図3)。
抗菌剤に耐えられる細菌がでてきたことにより、抗生物質に対する切実なニーズがあるにもかかわらず、高額な開発コストと長い開発期間と相まって(図3)、ここ数十年は市場に出回る種類が少なくなっています。
バイオフィルム
細菌は、バイオフィルムつまり層状の細胞で増殖すると、抗生物質の浸透に耐えることができます。バイオフィルムは、カテーテルやペースメーカー、人工関節、義歯、コンタクトレンズ、人工心臓弁、そしてインプラントなどで増殖します。細菌は、バイオフィルムつまり層状の細胞で増殖すると、抗生物質の浸透に耐えることができます。バイオフィルムは、カテーテルやペースメーカー、人工関節、義歯、コンタクトレンズ、人工心臓弁、そしてインプラントなどで増殖します。
グラム陰性菌の外膜
グラム陰性菌には、多くの薬剤を通さない二重層の外膜があり、そのためグラム陽性菌に作用するさまざまな薬剤に対しても自然耐性があります。
投資利益率
候補分子の成功率が低いことと、投資利益率が低いことが大きな課題になっています。
タイムライン
最初に候補分子が発見されてから、有効な抗生物質が市場に出るまでに10~15年かかる場合があります。
図3. 抗菌開発を複雑にさせる要因.
従来の抗生物質の代替品
新しい抗生物質を上市するのは時間がかかります(図3)。そこで、代替抗生物質が抗菌剤耐性との闘いに役立っています。
| 緊縮応答の阻害 |
細菌が宿主内において長期間生存していると、それは多くの場合無症候性ですが、再活性化や再感染を引き起こす可能性があります。これら長期生存細菌は「persister細菌」と呼ばれます。緊縮応答は、細菌が極度の飢餓状態に対抗するメカニズムであり、持続的な感染の発症に寄与していると考えられています。このプロセスを阻害することで、抗生物質に対する細菌の脆弱性を高められる可能性があります |
| 細菌ワクチン |
細菌感染をワクチンで予防すると、抗生物質の消費量の削減につながり、抗生物質耐性の改善に役立つと考えられます。2021年のWHO報告書には、60種を超える臨床開発中のワクチンと90種を超える前臨床開発中のワクチンの詳細が記載されています。 |
| 抗菌ペプチド |
抗菌ペプチドは、低分子抗生物質の代替品として人気を集めています。抗菌ペプチドは一般的に短いペプチド(アミノ酸100個未満)で、広範囲の抗菌活性を有します。Antimicrobial Peptide Database(抗菌ペプチドデータベース)によると、2022年11月現在、3,000種類以上の抗菌ペプチドが存在します。 |
| グリコペプチド |
Gグリコペプチドは、細胞壁の生合成を阻害することにより、主にグラム陽性菌に対して抗菌活性を示します。このグループで一般的に使用されているのはバンコマイシン、テイコプラニン、テラバンシン、ダルババンシン、そしてオリタバンシンなどですが、多くの新しい選択肢が開発、研究、そして最適化されています。 |
| リポペプチドとリポグリコペプチド |
ダプトマイシンは、グラム陽性菌に対して現在使用されている唯一のリポペプチドで、細菌の細胞膜を破壊することによって機能します。その抗菌効果は、カルシウムの存在およびカルシウムとの結合に依存しているようです。サイズが大きいため経口投与では吸収が悪く、よって静脈内投与される傾向があります。 |
| バクテリオファージ |
バクテリオファージは、細菌細胞に感染し、ウイルスDNAを注入することで細菌を死滅させる能力を持つウイルスです。このウイルスは細胞内で複製し、新しい細菌細胞を感染させる目的でその複製が放出されるときに細胞溶解を引き起こします。ただし、バクテリオファージ療法をより有効なものにするためには、経口投与後の腸内細菌種を標的としたin vivoでの有効性が低いなど、いくつかの課題に対処する必要があります。 |
表2.. 従来の抗生物質の代替品
抗菌剤の将来
素材を活用して薬物送達方法の強化を行うことにより、局所的で持続性があり、かつ刺激依存性のある抗菌活性をもたらすことができます。従来の投与方法以外で抗菌薬の送達を実現する方法はいくつかあります。インプラントやカテーテルなどの医療器具は感染源となることもありますが、これは抗菌性の材料を使用することで、予防できる場合があります。同様に、人が触れることの多い表面に抗菌コーティングを施すことで、微生物の感染を減らし、洗浄の必要性を最小限に抑えることができます。
ハイドロゲル
抗生物質とともに、薬物送達や創傷治癒で使用されます。ハイドロゲルは体細胞や体液に触れてin situで作用するため、これを利用して抗菌ペプチドなどの拡散性またはゲル結合性の抗生物質を投与させることができます。
ナノ粒子
ナノ粒子はサイズが小さいため、薬物を効果的に送達することができます。表面修飾を利用して特定の標的や部位に合わせて調整することができるほか、界面化学と組成によって活性のタイミングや薬物の放出、そして作用持続時間を制御することもできます。
複合材料
複合材料は、複数の材料を組み合わせて使用するもので、歯科用インプラントなどの医療機器に使用されています。抗菌活性を発揮する各種材料は、感染症の治療と予防の両方に有効であることが証明されています。
フィルムやコーティング
病院の入院患者の健康を改善して生存率を向上させる有効な方法として、医療器具による感染の可能性を下げることが挙げられます。それを行うための効果的なフィルムやコーティングの2つの例として、紫外線や可視光線を利用する方法と、微生物の付着を防ぐ活性酸素種を発生させる方法があります。
スキャフォールドとインプラント
創傷や骨の治癒に有用で、一般的に表面積対体積比が高く、ハイドロゲルよりも持続性が高いのが特徴です。カチオン性ポリマー、銅ナノ粒子、また一酸化窒素放出剤などを用いたインプラントが有望な効果を示しています。
図4 抗生物質の使用量を削減できる素材とソリューション
人工知能(AI)の進歩に伴い、新しい潜在的候補分子を同定するアルゴリズムを使った抗菌薬開発が加速しています。論文公開件数は着実に増加している一方、それに応じた特許出願数の上昇はまだ起きていないため、抗菌剤のAI研究のほとんどがまだ学術研究の段階にあることを示唆しています(図5)。
図5. AIを用いた抗菌開発に関する論文件数と特許申請数の急速な増加(論文 - 青、特許 - 黄)多剤耐性菌の増加は人間の健康に憂慮すべき脅威をもたらし、新規抗生物質と抗菌性材料の開発が急がれています。AIの普及はまだ始まったばかりですが、将来的な取り組みの合理化とタイムラインの短縮が期待されています。AIが化学に与える影響については、当社のInsight Report、大規模言語モデルの台頭、さまざまな新しいアプローチでバイオマテリアルが治療現場でどのように使用されているかをご覧ください。