Resumen
Los extremófilos, organismos que prosperan en entornos extremos, desafían nuestra comprensión de cómo se desarrolla y se adapta la vida. Estos organismos presentan una diversidad notable y adaptaciones bioquímicas únicas, como las extremoenzimas y los mecanismos celulares resistentes al estrés. Los extremófilos han desarrollado vías bioquímicas para producir compuestos bioactivos con una estabilidad y bioactividad increíbles. Estos metabolitos extremófilos, que incluyen péptidos antimicrobianos, extremoenzimas, agentes anticancerígenos, antioxidantes y otros, tienen un inmenso potencial para aplicaciones en numerosas industrias, como la farmacéutica, la biotecnológica, la biorremediación, la agricultura, la producción de biocombustibles y muchas más. Los recientes avances en genómica, metagenómica y biología sintética han acelerado el descubrimiento de nuevos compuestos bioactivos a partir de estos organismos resistentes, lo que ofrece soluciones innovadoras a retos globales como la resistencia a los antibióticos, la catálisis industrial y la sostenibilidad medioambiental.
Introducción: ¿Qué son los extremófilos?
La vida en la Tierra muestra una asombrosa capacidad para adaptarse incluso a los entornos más inhóspitos. Los organismos conocidos como extremófilos se desarrollan en condiciones que antes se consideraban incompatibles con la vida, como las abrasadoras fuentes hidrotermales, los lagos altamente ácidos o alcalinos, las aguas hipersalinas y los desiertos helados de la Antártida. El estudio de estos microorganismos resistentes ha revolucionado nuestra comprensión de los límites de la vida, ofreciendo conocimientos fundamentales sobre la biología evolutiva, la biotecnología e incluso la astrobiología.
Los extremófilos se clasifican en función de las condiciones extremas en las que habitan. Entre ellos se incluyen los termófilos (altas temperaturas), los psicrófilos (temperaturas bajo cero), los acidófilos y alcalófilos (pH extremo), los halófilos (alta salinidad), los barófilos (alta presión) y los xerófilos (sequedad extrema), entre otros. Sus estrategias de supervivencia suelen incluir enzimas especializadas conocidas como extremoenzimas, estructuras biomembranosas únicas, mecanismos de reparación del ADN y vías metabólicas que les permiten soportar tensiones fisicoquímicas extremas.
El descubrimiento de los extremófilos ya ha tenido un profundo impacto. En biotecnología, la extremoenzima Taq polimerasa, derivada del termófilo Thermus aquaticus, revolucionó la tecnología PCR, mientras que las enzimas de los halófilos y alcalófilos se utilizan en detergentes, procesamiento de alimentos y tratamiento de residuos. Además, los extremófilos desempeñan un papel crucial en la biorremediación, descomponiendo los contaminantes en entornos extremos donde los microbios convencionales fracasan.
Desde una perspectiva astrobiológica, los extremófilos sirven como análogos de la posible vida extraterrestre. Los metanógenos subterráneos del permafrost, las arqueas metabolizadoras de azufre de las fuentes hidrotermales y las bacterias resistentes a la radiación proporcionan pistas sobre cómo podría persistir la vida en cuerpos celestes como Marte, Europa o Encélado. El estudio de los extremófilos tiende así un puente entre la biología de la Tierra y la búsqueda de vida más allá de nuestro planeta.
Sin embargo, a pesar de su importancia, muchos aspectos de la biología de los extremófilos siguen sin explorarse. ¿Cómo evolucionan bajo presiones barométricas extremas? ¿Qué especies desconocidas se esconden en los nichos ecológicos más remotos de la Tierra? ¿Se puede aprovechar aún más su bioquímica única para desarrollar tecnologías sostenibles? Soluciones innovadoras como la minería metagenómica de especies no cultivables, la expresión heteróloga en huéspedes modelo y los sistemas de administración asistidos por nanotecnología están ayudando a resolver estas cuestiones esenciales.
En este informe, exploramos los datos de la CAS Content Collection™, el mayor repositorio de información científica curado por humanos, para comprender mejor los avances de la investigación en el campo de los extremófilos. Desde las profundidades del océano hasta las zonas de exclusión nuclear, estos diminutos organismos están impulsando enfoques innovadores para retos científicos que abarcan el descubrimiento de fármacos, la remediación ambiental y mucho más.
Tipos de extremófilos y cómo sobreviven
El término «extremófilo» fue acuñado por MacElroy en 1974 para referirse a los organismos que pueden vivir en entornos extremos. Aunque incluyen algunas especies de protozoos, algas y hongos, la mayoría de los extremófilos son procariotas, clasificados dentro de los dominios Archaea y Bacteria, con adaptaciones metabólicas y fisiológicas únicas que les permiten sobrevivir en estos entornos hostiles.
Como se ha señalado, los extremófilos viven en entornos increíblemente calientes o fríos, en entornos de alta salinidad o pH extremo, y en entornos de presión extremadamente alta, como las fosas marinas profundas. También hay extremófilos con resistencia a la radiación que pueden sobrevivir en desiertos y emplazamientos nucleares. Por ejemplo, Cladosporium chernobylensis, un hongo de la zona de exclusión de Chernóbil, presenta diversas estrategias de supervivencia, como la reparación del ADN y la producción de melanina. Como se muestra en la tabla 1, la variedad de extremófilos abarca muchos entornos inhóspitos:
| Tipo | Condición extrema | Organismos representativos | Hábitats naturales | Adaptaciones clave | Aplicaciones |
|---|---|---|---|---|---|
| Termófilos | Altas temperaturas (45–80 °C) | Thermus aquaticus, Pyrococcus furiosus | Aguas termales, respiraderos geotérmicos | Enzimas termoestables, lípidos de membrana modificados | PCR (Taq polimerasa), catálisis industrial |
| Hipertermófilos | Temperaturas muy altas (>80°C) | Methanopyrus kandleri (122 °C) | Fumarolas hidrotermales | Girasa inversa del ADN, proteínas chaperonas | Biorreactores para procesos en condiciones extremas |
| Psicrófilos (criófilos) | Bajas temperaturas (<15 °C) | Psychrobacter, Polaromonas | Hielo polar, océano profundo | Proteínas anticongelantes, membranas flexibles | Detergentes para lavado en frío, conservación de alimentos |
| Acidófilos | pH bajo (<3) | Picrophilus torridus (pH -0,06) | Drenaje ácido de minas, piscinas volcánicas | Bombas de protones, paredes celulares resistentes a los ácidos | Biolixiviación de metales, limpieza de drenaje ácido de minas |
| Alcalófilos | pH alto (>9) | Natronomonas pharaonis (pH 11) | Lagos de soda, suelos carbonatados | Antiportadores Na⁺/H⁺, transportadores especializados | Enzimas detergentes, procesamiento textil |
| Halófilos | Alta salinidad (2–5 M NaCl) | Halobacterium salinarum | Salinas, lagos hipersalinos | Acumulan solutos compatibles (p. ej., KCl), bacteriorrodopsina para obtener energía | Bioplásticos, producción de sal solar |
| Piezófilos (Barófilos) | Alta presión (>400 atm) | Pseudomonas bathycetes (fosa de las Marianas) | Fosas hadales, subsuelos profundos | Proteínas estabilizadas por presión, ácidos grasos insaturados | Biotecnología de aguas profundas, degradación de residuos bajo presión |
| Radiófilos | Alta radiación ionizante | Deinococcus radiodurans | Depósitos de residuos nucleares, desiertos | Reparación eficiente del ADN, complejos antioxidantes Mn²⁺ | Limpieza de residuos nucleares, fármacos radioprotectores |
| Xerófilos | Desecación extrema | Chroococcidiopsis (costras del desierto) | Desiertos, alimentos deshidratados | Acumulación de trehalosa, protección del ADN/proteínas | Cultivos resistentes a la sequía, estabilización de vacunas |
| Oligótrofos | Escasez de nutrientes | Pelagibacter ubique (océanos) | Océano abierto, aguas subterráneas profundas | Metabolismo ultraeficiente, genoma de pequeño tamaño | Tratamiento de aguas residuales, bioprocesamiento con bajos niveles de nutrientes |
| Metalotolerante | Altas concentraciones de metales pesados | Ferroplasma acidarmanus (Cu/As) | Relaves mineros, residuos industriales | Bombas de eflujo de metales, proteínas metalotioneínas | Biorremediación de metales tóxicos |
| Anaerobio | Entornos sin oxígeno | Metanógenos, Clostridium | Microbiomas intestinales, sedimentos profundos | Aceptores de electrones alternativos (p. ej., SO₄²⁻, CO₂) | Producción de biogás, estudios de la microbiota intestinal |
| Endolitos | Interior de las rocas | Chroococcidiopsis (rocas antárticas) | Valles secos de la Antártida, subsuelo | Pigmentos resistentes a los rayos UV, metabolismo lento | Modelos de terraformación, detección de biofirmas |
| Capnófilos | Altas concentraciones de CO2 | Campylobacter | Cavidades de mamíferos, aguas residuales | Fijación de carbono, fermentación láctica capnófila | Biofijación de CO₂, cultivo de bacterias patógenas |
| Poli-extremófilos | Múltiples extremos (p. ej., termoacidófilos) | Sulfolobus acidocaldarius (75°C + pH 3) | Fuentes termales ácidas volcánicas (75 °C + pH 3) | Combinaciones de las adaptaciones anteriores | Estudios análogos espaciales, enzimas industriales multipropósito |
Los extremófilos exhiben mecanismos de supervivencia extraordinarios que les permiten colonizar los entornos más inhóspitos de la Tierra. Estos microorganismos han desarrollado sofisticadas adaptaciones bioquímicas, estructurales y genómicas para soportar temperaturas extremas, fluctuaciones de pH, alta salinidad, desecación y radiación. Algunos de sus mecanismos de supervivencia clave incluyen:
- Protección del ADN y las proteínas: los extremófilos protegen su material genético y sus proteínas de la desnaturalización y el daño mediante diversos métodos:
- Proteínas de choque térmico (HSP): las chaperonas como la HSP70 en Pyrococcus furiosus evitan el plegamiento incorrecto de las proteínas a altas temperaturas.
- Girasa inversa: presente en los hipertermófilos, esta enzima introduce superespirales positivas para estabilizar el ADN a temperaturas superiores a 100 °C.
- Reparación del ADN resistente a la radiación: Deinococcus radiodurans utiliza la recombinación homóloga y la reparación por escisión de nucleótidos para reensamblar los cromosomas destrozados tras una exposición extrema a la radiación.
- Adaptaciones de la membrana y la pared celular: los extremófilos modifican sus membranas para mantener la fluidez y la integridad mediante:
- Lípidos unidos por éter: arqueas como Sulfolobus utilizan lípidos tetraéter para resistir el calor y la acidez extremos.
- Membranas monocapa: algunos hipertermófilos forman una monocapa lipídica para mejorar la estabilidad térmica.
- Paredes celulares resistentes a los ácidos: Las especies de Picrophilus mantienen los gradientes de protones con membranas impermeables a un pH de 0.
- Regulación osmótica en halófilos: los halófilos sobreviven a la alta salinidad mediante:
- Solutos compatibles: Halobacterium salinarum acumula iones K⁺ y osmolitos orgánicos (p. ej., betaína) para equilibrar la presión osmótica.
- Estrategia de sal: algunos halófilos incorporan altas concentraciones internas de sal utilizando enzimas halófilas especializadas que solo funcionan a una salinidad cercana a la saturación.
- Flexibilidad metabólica: muchos extremófilos utilizan fuentes de energía no convencionales:
- Litotrofía: Acidithiobacillus ferrooxidans oxida el hierro y el azufre en minas ácidas.
- Metanogénesis anaeróbica: los metanógenos como Methanopyrus kandleri producen metano en los respiraderos hidrotermales.
- Radiosíntesis: algunas bacterias utilizan la radiólisis del agua procedente de la desintegración radiactiva para generar energía en entornos subterráneos profundos.
- Criptobiosis y letargo: algunos extremófilos entran en animación suspendida bajo estrés:
- Anhidrobiosis: los tardígrados y ciertas bacterias (p. ej., Chroococcidiopsis) sobreviven a la desecación completa produciendo trehalosa para proteger las estructuras celulares.
- Formación de esporas: las especies Bacillus y Clostridium forman endosporas resistentes al calor, la radiación y los productos químicos.
Descubrimientos recientes de nuevos extremófilos
Los recientes avances en ecología microbiana y genómica han ampliado significativamente nuestra comprensión de la diversidad de los extremófilos, revelando nuevos taxones y estrategias de adaptación previamente inexploradas en entornos extremos. La secuenciación de alto rendimiento y la genómica unicelular han descubierto linajes crípticos dentro de las arqueas y bacterias que habitan en fuentes hidrotermales, lagos hiperácidos, capas de hielo polares y biosferas subterráneas profundas. Los estudios metagenómicos de las comunidades extremófilas han identificado vías metabólicas únicas, como nuevos mecanismos quimiolitotróficos en termófilos de aguas profundas y sistemas fotosintéticos híbridos en arqueas halófilas.
El descubrimiento de Asgard arquea en aguas termales ha resultado interesante, ya que ha proporcionado nuevos conocimientos sobre la evolución de los eucariotas y el aislamiento de bacterias resistentes a la radiación de vertederos nucleares con capacidades de reparación del ADN sin precedentes. Los científicos también descubrieron una nueva L-asparaginasa de tipo II a partir de una cepa de Bacillus subtilis CH11 halotolerante, aislada de los salares peruanos. El desarrollo de variantes de L-asparaginasa con mayor estabilidad y eficiencia es un objetivo crucial debido al uso generalizado de esta enzima en la industria alimentaria y en el tratamiento del cáncer.
Recientemente se han descrito comunidades procariotas distintas en cuevas, con taxones especializados que se adaptan a las condiciones energéticas y nutricionales locales. Se ha descubierto una nueva especie, Pseudocandona movilaensis, en las aguas sulfurosas de la cueva de Movile, en Rumanía, con un ecosistema quimioautotrófico único en el que la vida se sustenta mediante la oxidación del sulfuro de hidrógeno en lugar de la fotosíntesis. Además, se han desarrollado bacterias extremófilas, en particular halófilas, en minas de cobre en desuso.
Las bacterias extremófilas, concretamente las bacterias Candidate Phyla Radiation (CPR), son un grupo fascinante de microorganismos, en particular las que se han encontrado recientemente en entornos ácidos de drenaje de minas. Se caracterizan por su tamaño ultrapequeño, sus genomas reducidos y su dependencia de las interacciones con los organismos huéspedes.
Deinococcus radiodurans y sus parientes, al igual que otros miembros de la familia Deinococcaceae, son conocidos por su extraordinaria resistencia a la radiación, especialmente en entornos con altos niveles de radiación ionizante, como el interior o las proximidades de los reactores nucleares. Han desarrollado sistemas eficaces para reparar el daño causado al ADN por la radiación y otras tensiones, como la desecación.
Además, técnicas independientes del cultivo han revelado la «materia oscura microbiana» en entornos extremos, lo que sugiere una reserva de diversidad filogenética y funcional sin explotar. Estos descubrimientos no solo redefinen los límites de la vida en la Tierra, sino que tienen profundas implicaciones para la astrobiología, la biotecnología y la resiliencia al cambio climático.
Sin embargo, siguen existiendo retos para cultivar estos organismos y traducir los conocimientos genómicos en una comprensión funcional. Las investigaciones futuras deberían integrar enfoques multiómicos con métodos de cultivo avanzados para explorar las funciones ecológicas y el potencial biotecnológico de estos extremófilos recién descubiertos.
Compuestos bioactivos de los extremófilos
Los extremófilos producen compuestos bioactivos únicos con posibles aplicaciones en medicina, industria y biotecnología (véase la tabla 2). Estos metabolitos secundarios, entre los que se incluyen enzimas, agentes antimicrobianos y antioxidantes, muestran una estabilidad y funcionalidad notables en condiciones adversas. Los recientes avances en la bioprospección de extremófilos han descubierto nuevos compuestos con propiedades terapéuticas, entre las que se incluyen actividades anticancerígenas, antiinflamatorias y antimicrobianas. Además, las enzimas derivadas de extremófilos (extremoenzimas) son valiosas en los procesos industriales debido a su robustez en condiciones extremas de pH, temperatura y salinidad. Estos compuestos ofrecen soluciones novedosas a los retos que plantean la resistencia a los medicamentos, la catálisis industrial y la sostenibilidad medioambiental.
Estudios recientes han revelado que más del 40 % de los compuestos bioactivos microbianos siguen sin descubrirse, y que los extremófilos representan un importante recurso sin explotar. Los sistemas CRISPR-Cas (derivados del Streptococcus thermophilus) y la Taq polimerasa (del Thermus aquaticus) se encuentran entre las herramientas biotecnológicas derivadas de extremófilos más exitosas. Los halófilos, termófilos y acidófilos producen antimicrobianos, agentes anticancerígenos y polímeros biodegradables con relevancia industrial.
| Tipo de extremófilo | Compuestos bioactivos clave |
|---|---|
| Termófilos | Enzimas termoestables (ADN polimerasas, proteasas), péptidos antimicrobianos (sulfolobicinas) |
| Psicrófilos | Proteínas anticongelantes, enzimas activas en frío (lipasas, proteasas) |
| Halófilos | Bacterioruberina (antioxidante), halocinas (péptidos antimicrobianos) |
| Acidófilos/Alcalófilos | Celulasas estables al ácido, proteasas alcalófilas |
| Piezófilos (Barófilos) | Enzimas resistentes a la presión, EPS (exopolisacáridos) bioactivos |
| Radioresistente | Enzimas reparadoras del ADN, compuestos radioprotectores |
Los avances en diversas tecnologías ómicas y bioinformáticas han revelado muchos metabolitos secundarios, péptidos y extremoenzimas hasta ahora desconocidos que muestran una notable bioactividad en condiciones extremas. Estas exoenzimas y metabolitos secundarios ofrecen ventajas sobre los fármacos convencionales, entre ellas la termoestabilidad (útil para el almacenamiento y la administración), estructuras novedosas (que eluden los mecanismos de resistencia existentes) y una alta especificidad (que reduce los efectos fuera del objetivo).
Los descubrimientos innovadores incluyen:
- Péptidos antimicrobianos hipertermostables procedentes de termófilos de las profundidades marinas que alteran las membranas bacterianas mediante novedosos mecanismos de formación de poros.
- Pigmentos resistentes a la radiación procedentes de especies de Deinococcus que muestran una potente actividad antioxidante a través de vías únicas de eliminación de radicales libres.
- Antibióticos estables al ácido procedentes de Sulfolobus con puentes tioéter modificados que se dirigen a patógenos resistentes a los fármacos a través de mecanismos duales de inhibición de la pared celular y despolarización de la membrana.
Las adaptaciones estructurales que confieren bioactividad en condiciones extremas son notables, como la incorporación de aminoácidos D en bacteriocinas halófilas, el plegamiento resistente a la presión en compuestos piezófilos y las modificaciones crioprotectoras en metabolitos psicrófilos. También son dignos de mención los objetivos moleculares de estos compuestos, entre los que se incluyen sus interacciones con las membranas microbianas (p. ej., la unión de lípidos II por lipopéptidos termófilos), la inhibición de enzimas esenciales (p. ej., la inhibición del proteasoma por salinosporamidas derivadas de las profundidades marinas) y la interferencia con el metabolismo de los ácidos nucleicos (p. ej., la intercalación del ADN por metabolitos bacterianos resistentes a la radiación).
Los métodos de descubrimiento innovadores han revolucionado la bioprospección de extremófilos, incluyendo la minería genómica guiada por metaómica, la expresión heteróloga en plataformas de biología sintética y el cribado de actividad de alto rendimiento en condiciones extremas simuladas. Estos nuevos métodos han dado lugar a aplicaciones traslacionales en medicina, como los antibióticos de última generación dirigidos a los patógenos ESKAPE multirresistentes ESKAPE pathogens. En la agricultura, se han identificado bioestimulantes basados en extremolitos, y las enzimas estables en disolventes para la química verde están cambiando la biotecnología industrial.
Los investigadores están abordando los retos de la escalabilidad de los compuestos y la optimización de la estructura-actividad con soluciones propuestas que aprovechan el modelado computacional y la ingeniería de vías basadas en CRISPR. Esta síntesis del descubrimiento de bioactivos extremófilos y la comprensión de sus mecanismos proporciona una hoja de ruta para la investigación futura y una base para el desarrollo de soluciones innovadoras a los retos globales de salud y medio ambiente.
La tabla 3 muestra los fármacos/agentes activos disponibles derivados de extremófilos y sus aplicaciones. Entre ellos se incluyen ejemplos aprobados por la FDA, como la L-asparaginasa y la Taq polimerasa; candidatos preclínicos prometedores, como las halocinas, que combaten la resistencia a los antibióticos; y la bacteriorrubina, útil en el tratamiento del cáncer.
| Fuente extremófila | Agente bioactivo | Enfermedad objetivo/Aplicación | Mecanismo de acción |
|---|---|---|---|
| Agentes anticancerígenos | |||
| Thermus thermophilus (termófilo) | L-asparaginasa | Leucemia linfoblástica aguda (LLA) | Agotan la asparagina, matando de hambre a las células cancerosas |
| Halobacterium salinarum (halófilo) | Bacterioruberina | Cáncer de mama/colon | Antioxidante, induce la apoptosis |
| Picrophilus torridus (Acidófilo) | Proteasas estables al ácido | Cáncer de páncreas (tumores ácidos) | Activa los profármacos en microambientes tumorales con pH bajo |
| Deinococcus radiodurans (Radioresistente) | Complejos de manganeso | Protección contra la radiación (terapia contra el cáncer) | Elimina las ROS y protege las células sanas |
| Agentes antimicrobianos y antifúngicos | |||
| Haloferax mediterranei (Halófilo) | Halocinas | MRSA, infecciones por pseudomonas | Rompe las membranas celulares bacterianas |
| Sulfolobus solfataricus (Termoacidófilos) | Sulfolobicinas | Candida albicans (infecciones fúngicas) | Se une al ergosterol (membrana fúngica) |
| Colwellia psychrerythraea (Psicrófilo) | Proteínas anticongelantes | Prevención de biopelículas (implantes) | Inhibe la adhesión bacteriana |
| Terapias para enfermedades neurodegenerativas | |||
| Pyrococcus furiosus (hipertermófilos) | Chaperoninas | Enfermedad de Alzheimer/Parkinson | Previene el plegamiento incorrecto de las proteínas |
| Deinococcus radiodurans (bacterias radiorresistentes) | Superóxido dismutasa | Enfermedad de Parkinson | Reduce el estrés oxidativo en la enfermedad de Parkinson |
| Antiviral y edición genética | |||
| Streptococcus thermophilus (termófilo) | CRISPR-Cas9 | Terapia génica contra el VIH | Edición genética para extirpar el ADN viral |
| Thermus aquaticus (termófilo) | Taq polimerasa | Diagnóstico viral (VIH, VPH, COVID-19) | Amplificación por PCR del ADN viral |
| Agentes antiinflamatorios e inmunomoduladores | |||
| Alteromonas macleodii (profundidad marina) | Exopolisacáridos | Artritis reumatoide | Suprime el TNF-α (antiinflamatorio) |
| Antioxidantes y agentes protectores contra los rayos UV | |||
| Halófilos | Bacterioruberina | Nutracéuticos y cosméticos antienvejecimiento | Antioxidante cuatro veces más potente que el β-caroteno |
| Cianobacterias, microalgas, Pyrococcus sp. (termófilo) | Aminoácidos similares a la micosporina (MAA) | Protectores solares naturales en productos para el cuidado de la piel | Fuerte capacidad de absorción en las regiones UV-A y UV-B |
| Extremozimas industriales | |||
| Thermus aquaticus | Taq polimerasa | Amplificación por PCR en biología molecular | Evita la desnaturalización de la enzima durante la etapa de calentamiento |
| Acidófilos | Lacasas | Biodegradación de colorantes textiles y biorremediación | Facilitan la biodegradación y la desintoxicación de los colorantes textiles al catalizar su oxidación |
| Psicrófilos | Proteasas activas en frío | Detergentes ecológicos y procesamiento de alimentos | Desestabilizan el sitio activo, mejoran la flexibilidad y permiten que la enzima permanezca activa a bajas temperaturas |
A pesar de su potencial, persisten los retos en su cultivo y extracción. Muchos extremófilos siguen siendo difíciles de cultivar y se necesitan más ensayos clínicos. Las investigaciones futuras deberían aprovechar la metagenómica y la biología sintética para aprovechar estas moléculas bioactivas de manera eficiente.
Aun así, las presiones evolutivas únicas que sufren los extremófilos han dado lugar a compuestos bioactivos con propiedades incomparables y mecanismos de acción novedosos. A medida que avancen las tecnologías de descubrimiento, estos organismos desempeñarán un papel fundamental a la hora de abordar los retos sanitarios y medioambientales a nivel mundial. La investigación sistemática de sus compuestos bioactivos no solo amplía nuestro arsenal farmacológico, sino que también proporciona conocimientos fundamentales sobre la adaptabilidad de la vida.
Panorama de la investigación y nuevos avances
Nuestro análisis de la CAS Content Collection reveló que el número de documentos relacionados con los extremófilos se ha triplicado en los últimos 25 años. El número de patentes es relativamente bajo, alrededor del 5 % del total de documentos, pero el número anual de patentes se ha multiplicado por cuatro desde el año 2000 (véase la Figura 1).
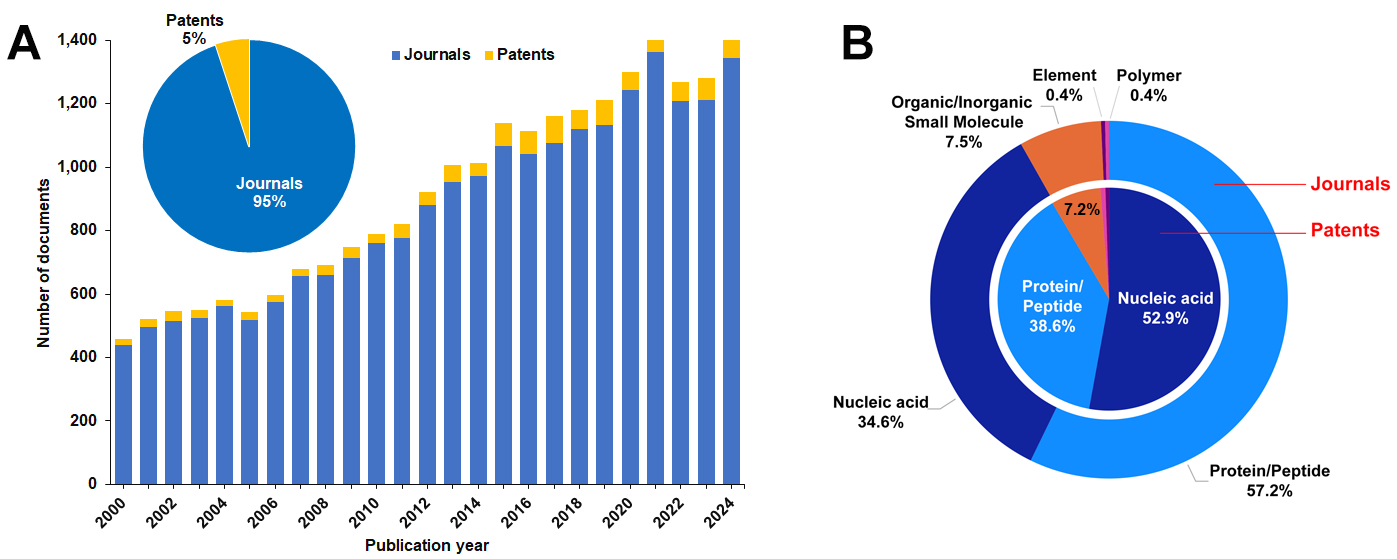
Nuestro análisis indica que las proteínas/péptidos y los ácidos nucleicos son los más asociados a los extremófilos. En las patentes, los ácidos nucleicos representan menos del 50 %, mientras que en las revistas dominan las proteínas/péptidos, con alrededor del 60 % de las publicaciones. Las moléculas pequeñas están representadas en alrededor del 8 % de los documentos (véase la figura 1B).
También examinamos la distribución de los tipos de extremófilos en la bibliografía relacionada (véase la figura 2).

A partir de estos análisis, hemos extraído una serie de conclusiones significativas:
El mayor número de documentos relacionados con los extremófilos se refiere a los oligótrofos, organismos que se desarrollan en entornos pobres en nutrientes
Los entornos oligotróficos, como los océanos abiertos, las profundidades subterráneas y los desiertos, cubren la mayor parte de la Tierra. Por lo tanto, los oligótrofos impulsan procesos clave como el secuestro de carbono en océanos pobres en nutrientes, el ciclo del nitrógeno y el fósforo en suelos áridos y el mantenimiento de la diversidad microbiana en ecosistemas extremos. Su capacidad para desarrollarse con recursos mínimos los hace valiosos para la biorremediación, la bioenergía (p. ej., pilas de combustible microbianas con necesidades mínimas de sustrato), así como para nuevas enzimas y compuestos bioactivos que se adaptan a la escasez extrema. A medida que los entornos pobres en nutrientes se expanden debido al cambio climático, comprender a los oligótrofos ayuda a predecir las respuestas microbianas a los cambios en los ecosistemas y los cambios en el almacenamiento de carbono en los océanos que se calientan.
Además, los oligótrofos sobreviven en condiciones similares a las de Marte, Europa o Encélado, donde los nutrientes son escasos. Estudiarlos ayuda a identificar posibles formas de vida extraterrestre, a desarrollar estrategias de detección de vida para misiones espaciales y a comprender los mecanismos de supervivencia en estos entornos. La Tierra primitiva tenía nutrientes limitados, lo que hace que los oligótrofos sean posibles análogos de la vida antigua. Su estudio proporciona pistas sobre cómo se adaptaron los microorganismos primordiales y los orígenes de las vías metabólicas en condiciones de bajos nutrientes.
Los extremófilos que han experimentado un mayor crecimiento en publicaciones en los últimos cinco años son los poliextremófilos (~51 %), los metalófilos (~47 %) y los radiófilos (~36 %)
- Los poliextremófilos, organismos que se desarrollan en múltiples condiciones extremas simultáneamente, han despertado recientemente un gran interés científico porque amplían los límites de la vida y ofrecen una visión sin precedentes de la biología, la astrobiología y la biotecnología. Los poliextremófilos producen enzimas multifuncionales y biomoléculas estables en condiciones industriales extremas. A medida que la Tierra se enfrenta al aumento de las temperaturas, la acidificación de los océanos y la desertificación, los poliextremófilos ayudan a predecir la resiliencia microbiana en ecosistemas en colapso, el ciclo del carbono en el permafrost en deshielo y la evolución bajo rápidos cambios ambientales.
- Los metalófilos son microorganismos que se desarrollan en entornos con altas concentraciones de metales tóxicos (p. ej., arsénico, mercurio, cadmio, uranio). Desempeñan un papel fundamental en la limpieza de sitios contaminados, como residuos mineros e industriales, vertederos nucleares y aguas cargadas de mercurio y arsénico. Su capacidad para inmovilizar o transformar metales tóxicos ofrece una alternativa económica y ecológica a la limpieza química. Los metalófilos también son fundamentales en la biominería, donde extraen metales valiosos como el cobre, el oro y los elementos de tierras raras de minerales de baja ley, lo que reduce la necesidad de utilizar productos químicos tóxicos como el cianuro en la minería. Los metalófilos producen biomoléculas únicas para sobrevivir a la toxicidad de los metales, entre ellas péptidos que se unen a los metales y sideróforos que podrían proporcionar fuentes de nuevos antibióticos. Contienen enzimas que desintoxican los metales pesados, lo que podría ser útil en el desarrollo de fármacos para quimioterapia, y tienen compuestos resistentes a la radiación. Ningún otro extremófilo interactúa con los metales tóxicos de forma tan íntima, lo que los hace esenciales para los avances medioambientales, industriales y astrobiológicos.
- Los radiófilos se desarrollan en entornos de alta radiación, como los vertederos de residuos nucleares, los rayos cósmicos en el espacio o los depósitos de minerales radiactivos. Los radiófilos como el Deinococcus radiodurans sobreviven a dosis de radiación miles de veces superiores a las letales para los seres humanos gracias a sus enzimas de reparación del ADN ultraeficaces. Esto podría dar lugar a nuevos tratamientos contra el cáncer, antioxidantes protectores y mecanismos de reparación del ADN. Los radiófilos también se están diseñando para limpiar la contaminación radiactiva: Geobacter sulfurreducens reduce el uranio, haciéndolo menos soluble en las aguas subterráneas; Rubrobacter radiotolerans sobrevive en el refrigerante de los reactores nucleares, descomponiendo los isótopos tóxicos; y los investigadores están intentando crear «superradiófilos» para la limpieza de Chernóbil/Fukushima.
Los extremófilos con el mayor porcentaje de patentes son los acidófilos (~11 %) y los termófilos (~9 %)
- Acidófilos: estos microorganismos son cruciales para la extracción de metales, la remediación del drenaje ácido de minas y la recuperación de elementos de tierras raras (p. ej., de teléfonos inteligentes y baterías desechados). Esto los convierte en actores clave en las estrategias de minería sostenible y economía circular. Los acidófilos producen enzimas tolerantes al ácido que se utilizan en la producción de biocombustibles (celulasas, xilanasas que funcionan a pH bajo), la industria alimentaria y los productos farmacéuticos, como el descubrimiento de nuevos antibióticos en aguas termales ácidas. Sus enzimas suelen superar a las convencionales en condiciones industriales adversas. Su estudio une la microbiología, la astrobiología, la industria y las ciencias ambientales, lo que los convierte en uno de los grupos de extremófilos más impactantes de la actualidad.
- Los termófilos —organismos que se desarrollan a altas temperaturas (normalmente entre 45 y 80 °C)— y los hipertermófilos (que crecen mejor a 80 °C y más) se han convertido en un foco importante de la investigación sobre extremófilos debido a su biología única y sus aplicaciones industriales. Producen extremoenzimas resistentes al calor que siguen siendo funcionales a altas temperaturas. Esto los ha convertido en muy valiosos para la PCR (reacción en cadena de la polimerasa). Como se ha señalado, la Taq polimerasa de Thermus aquaticus revolucionó la amplificación del ADN. También tienen importantes aplicaciones médicas y farmacéuticas, como las enzimas termoestables utilizadas en el diagnóstico y la síntesis de fármacos. Los termófilos producen nuevos compuestos antimicrobianos que ayudan en el descubrimiento de antibióticos, y también son vitales para la investigación del cáncer, ya que el estudio de las proteínas de choque térmico (HSP) en los termófilos ayuda a comprender las respuestas al estrés celular.
En la investigación sobre energías renovables y tratamiento de residuos, los termófilos participan en la producción de biocombustibles y biohidrógeno, la mejora del biogás y la biorremediación extrema. Las enzimas termoestables mejoran la elaboración de cerveza, la panadería y la producción láctea en la industria alimentaria, y las proteasas y lipasas termófilas mejoran la eliminación de manchas en los lavados a alta temperatura para obtener mejores detergentes. Con sus variadas aplicaciones, es comprensible que los termófilos se encuentren en la bibliografía sobre patentes y en usos comerciales.
Analizamos la CAS Content Collection para comprender mejor las tendencias de crecimiento en la investigación relacionada específicamente con las extremoenzimas y las biomoléculas (véase la figura 3):

La figura 4 muestra un mapa de calor de las coocurrencias relativas de los extremófilos pertenecientes a diversas clases con los tipos de extremoenzimas producidas:

Las oxidasas son las enzimas con el mayor número de documentos relacionados con los extremófilos
Las oxidasas se encuentran entre las extremoenzimas más estudiadas debido a su importancia ecológica, sus aplicaciones industriales y sus adaptaciones únicas a condiciones extremas. Muchos extremófilos (p. ej., termófilos, alcalófilos y halófilos) dependen de las oxidasas para respirar en entornos con oxígeno limitado o extremos. Además, algunas oxidasas ayudan a los extremófilos a hacer frente al estrés oxidativo en condiciones adversas. Su termoestabilidad es clave: las oxidasas de las bacterias termófilas permanecen activas a altas temperaturas, lo que resulta útil en la producción de biocombustibles, el procesamiento de alimentos y el tratamiento de residuos. Su tolerancia a pH, salinidad y disolventes extremos también es importante en procesos industriales duros.
Las oxidasas extremófilas suelen tener estructuras proteicas modificadas, como enlaces iónicos mejorados en los halófilos o pliegues compactos en los termófilos, que las hacen más resistentes. El estudio de estas adaptaciones ayuda en la ingeniería enzimática para aplicaciones que van desde la biorremediación hasta la medicina.
Las lacasas, nucleasas, glicosidasas y catalasas extremófilas muestran la mayor tendencia de crecimiento
Las lacasas extremófilas muestran una estabilidad única en condiciones industriales adversas, superando a otras enzimas debido a su termoestabilidad (activas a 70-100 °C para el procesamiento de biocombustibles y pulpa), resistencia al pH (funcionan en corrientes de residuos altamente ácidas/alcalinas) y tolerancia a los disolventes (funcionan en disolventes orgánicos para la síntesis farmacéutica). Esto las hace más viables industrialmente que muchas otras extremoenzimas, que pueden carecer de esa resistencia a múltiples fuentes de estrés. Los recientes avances en metagenómica, evolución dirigida y edición basada en CRISPR han permitido el descubrimiento de nuevas lacasas a partir de extremófilos no cultivables y la adaptación de lacasas a necesidades industriales específicas. Esto ha acelerado su desarrollo en comparación con otras extremoenzimas.
Otra clase de enzimas, las nucleasas, ha ganado una gran atención en los últimos años, rivalizando con las lacasas y otras extremoenzimas en aplicaciones biotecnológicas y médicas. Su capacidad para funcionar en condiciones extremas mientras mantienen una corte preciso del ADN/ARN las hace indispensables en campos de vanguardia como la edición del genoma, el diagnóstico y la biología sintética. Las nucleasas extremófilas (p. ej., las variantes termoestables de Cas9, las enzimas de restricción TaqI) están revolucionando la ingeniería genética porque su termoestabilidad les permite trabajar en PCR a alta temperatura y en flujos de trabajo de edición genética. Las nucleasas tolerantes a la sal y a los disolventes permiten la manipulación del ADN en condiciones de laboratorio no estándar, como el análisis directo de muestras ambientales. Las variantes modificadas genéticamente, incluidas las de las especies Pyrococcus o Thermus, mejoran la precisión y la eficiencia de los sistemas CRISPR-Cas. Por ejemplo, la nucleasa Thermus thermophilus (Tth) se utiliza en la PCR de inicio en caliente para evitar la amplificación inespecífica.
Las nucleasas extremófilas son esenciales para el diagnóstico molecular y las pruebas en el punto de atención. Las nucleasas termoestables son fundamentales para la detección rápida de ADN/ARN (p. ej., RT-PCR para COVID-19), mientras que las nucleasas halófilas funcionan en tampones de diagnóstico con alto contenido en sal, lo que mejora la vida útil de las pruebas que se pueden utilizar sobre el terreno. Las nucleasas resistentes a los ácidos y álcalis permiten la extracción de ADN de muestras complejas. Otros usos esenciales de las nucleasas extremófilas incluyen aplicaciones de biorremediación y antibiofilm, biología sintética y almacenamiento de datos de ADN, así como aplicaciones farmacéuticas y antivirales.
Las glicosidasas (o hidrolasas glicósidasas) de los extremófilos también han cobrado importancia recientemente debido a su capacidad única para descomponer carbohidratos complejos en condiciones extremas, lo que abre nuevas aplicaciones en biorrefinerías, medicina, tecnología alimentaria y biología sintética. Las glicosidasas extremófilas suponen un cambio revolucionario en la conversión de la biomasa vegetal en biocombustibles y productos bioquímicos, ya que su termoestabilidad (70-100 °C) permite una sacarificación eficiente de la lignocelulosa en condiciones industriales. Su tolerancia a los ácidos y álcalis permite la hidrólisis en los procesos de pretratamiento (p. ej., explosión de vapor, digestión ácida), y su resistencia a los disolventes permite su uso en líquidos iónicos para la descomposición de la biomasa.
Estas glicosidasas mejoran la eficiencia del procesamiento de alimentos y el desarrollo de nuevos productos: las α-amilasas termoacidófilas (p. ej., de Sulfolobus) mejoran la licuefacción del almidón a alta temperatura para la producción de jarabe de maíz; las β-galactosidasas adaptadas al frío (psicrofilas) producen leche sin lactosa con bajos costes energéticos; y las glicosidasas halófilas estabilizan los alimentos fermentados en condiciones de alta salinidad (p. ej., la salsa de soja o el kimchi). Las glicosidasas extremófilas también son importantes para la gestión de residuos, ya que el reciclaje enzimático de los residuos alimentarios y agrícolas es ahora obligatorio en la UE.
Las catalasas de extremófilos (extremocatalasas) son otra clase de extremoenzimas que está ganando rápidamente atención debido a su capacidad para desarrollarse donde la degradación del peróxido de hidrógeno (H₂O₂) es esencial. Salen activas a temperaturas elevadas, pH extremos, alta salinidad y estrés oxidativo, lo que abre las puertas a aplicaciones biotecnológicas, médicas y medioambientales de última generación. Su termoestabilidad (60-120 °C) es esencial para la eliminación de H₂O₂ en el blanqueo de textiles, el procesamiento de papel y la esterilización de alimentos. Su resistencia a los álcalis y ácidos (pH 3-11) funciona en el blanqueo del denim (pH 10-11) y el procesamiento de lácteos (pH 6-7) sin desnaturalización enzimática. Además, su tolerancia a los disolventes orgánicos se utiliza en la producción de biocombustibles, donde el H₂O₂ es un subproducto.
Entre los usos emergentes de las catalasas en biomedicina se incluyen la cicatrización de heridas, donde las extremocatalasas degradan el H₂O₂ en las heridas crónicas; la aceleración de la reparación de tejidos; las terapias antioxidantes, como el tratamiento potencial de trastornos de estrés oxidativo como el Alzheimer y el Parkinson; y la limpieza de lentes de contacto, ya que las catalasas halófilas previenen la irritación ocular inducida por el H₂O₂ en las soluciones desinfectantes.
Los exopolisacáridos producidos por extremófilos se han convertido en uno de los productos microbianos más valiosos
Estos azúcares complejos sintetizados por extremófilos poseen propiedades únicas que los hacen superiores a los polisacáridos convencionales. Presentan una termoestabilidad inigualable (hasta 130 °C para EPS de Thermus spp.); resistencia química (pH 0,5-13, disolventes orgánicos); capacidad de hidratación extrema (1000 veces su peso en agua); y resistencia a la radiación. Por ejemplo, el EPS de Sulfolobus acidocaldarius sigue siendo viscoso a 95 °C y pH 2, superando a todos los espesantes comerciales.
También se utilizan con éxito en muchas aplicaciones médicas. El EPS de Halomonas forma apósitos de hidrogel que reducen el tiempo de cicatrización de las heridas en un 40 %, previene la formación de biopelículas (90 % de inhibición del SARM) y se autoesteriliza en entornos salinos. En la administración de fármacos, las nanopartículas de EPS de Thermococcus sobreviven intactas al ácido del estómago, liberan los fármacos a temperaturas corporales precisas y se biodegradan después de 72 horas. Por último, en las terapias contra el cáncer, el EPS de Rhodothermus muestra una inhibición del crecimiento tumoral del 60 %, cero citotoxicidad para las células sanas y sinergia con los fármacos de inmunoterapia.
Para visualizar los conceptos principales, así como los tipos, temas y aplicaciones específicos relacionados con los extremófilos, utilizamos un mapa TrendScape que aprovecha el panorama de publicaciones (véase la figura 5):

Aplicaciones biotecnológicas e industriales de los extremófilos
Aplicaciones biomédicas:
Los compuestos bioactivos y las enzimas derivados de extremófilos están revolucionando las industrias farmacéutica y biomédica debido a su estabilidad y sus novedosos mecanismos. Ya han sido fundamentales para el desarrollo de la tecnología CRISPR-Cas9 y, aunque la famosa Cas9 de Streptococcus pyogenes tiene limitaciones en cuanto a estabilidad, las enzimas Cas adaptadas al calor, como Thermus thermophilus Cas9, funcionan a altas temperaturas. Las enzimas de los acidófilos también permiten la edición genética en entornos ácidos (p. ej., la ingeniería del microbioma intestinal). Los radiófilos como Deinococcus radiodurans ofrecen nuevas plantillas de reparación del ADN para mejorar la precisión de CRISPR y reducir los efectos fuera del objetivo.
Las biomoléculas y las extremoenzimas están impulsando nuevos descubrimientos en la investigación cardiovascular. Por ejemplo, las enzimas fibrinolíticas de termófilos como Geobacillus pueden disolver los coágulos sanguíneos de manera más eficiente que los trombolíticos actuales, con una mayor estabilidad a altas temperaturas y un tiempo de circulación más prolongado. Las proteínas antioxidantes de los radiófilos neutralizan el estrés oxidativo, un factor clave de la aterosclerosis y la insuficiencia cardíaca. Los lípidos extremófilos también son prometedores en la administración de fármacos cardiovasculares. Por ejemplo, los liposomas termoestables de los termófilos mejoran la administración dirigida de fármacos a las placas ateroscleróticas, mientras que los transportadores de membrana adaptados al frío de los microbios antárticos ayudan a que los fármacos penetren en las arterias calcificadas de forma más eficaz.
Las extremoenzimas también se dirigen a los agregados proteicos, lo que las hace potencialmente transformadoras para abordar enfermedades neurodegenerativas como el Alzheimer, el Parkinson y la ELA. Las proteasas termófilas (p. ej., las de Thermus aquaticus) degradan las fibrillas beta-amiloides y tau de forma más eficaz que las enzimas humanas, resistiendo el entorno oxidativo del cerebro. Las chaperonas adaptadas al frío evitan el plegamiento incorrecto de la α-sinucleína en el Parkinson, manteniendo la estabilidad de las proteínas en concentraciones bajas. Se ha informado de que la proteasa Pyrococcus furiosus reduce las placas amiloides en un 70 % en modelos de ratones transgénicos.
Además de estas aplicaciones biomédicas, se ha descubierto que los hipertermófilos como Thermococcus gammatolerans producen policétidos con propiedades antibacterianas y anticancerígenas, que actúan sobre patógenos multirresistentes y líneas celulares cancerosas. Las extremoenzimas también se utilizan en la síntesis de fármacos y en el desarrollo de sensores y herramientas de diagnóstico.
Por ejemplo, las enzimas activas en frío de los psicrófilos se están integrando en biosensores para detectar biomarcadores en entornos clínicos de baja temperatura, como la monitorización de la glucosa para la diabetes. Las proteínas halófilas como la bacteriorrodopsina de Halobacterium salinarum se utilizan en sistemas de diagnóstico activados por la luz. Estas aplicaciones demuestran el potencial de los extremófilos para revolucionar muchos aspectos de la biomedicina.
Aplicaciones ambientales:
La biorremediación, el uso de microorganismos para degradar o detoxificar los contaminantes ambientales, es un uso cada vez más frecuente de los extremófilos, especialmente en condiciones extremas en las que los microbios convencionales no pueden sobrevivir.
- Degradación de hidrocarburos: los psicrófilos como Alcanivorax borkumensis degradan los derrames de petróleo en entornos marinos fríos, como las aguas del Ártico al metabolizar los hidrocarburos y crear compuestos no tóxicos. Los termófilos, como Geobacillus thermodenitrificans, tratan los efluentes industriales contaminados con petróleo a altas temperaturas, lo que mejora la eficacia de la limpieza.
- Remediación de metales pesados: los acidófilos, como Acidithiobacillus ferrooxidans, extraen metales pesados como el cobre y el uranio de los residuos mineros mediante biolixiviación, lo que reduce la toxicidad ambiental. Los halófilos de los lagos hipersalinos, como Halomonas elongata, secuestran metales como el cadmio en los residuos industriales salinos, restaurando los sitios contaminados.
- Degradación de plásticos y xenobióticos: descubrimientos recientes destacan la capacidad de los extremófilos para degradar contaminantes sintéticos. Por ejemplo, un estudio de 2024 identificó una cepa psicrófila de Ideonella sakaiensis que produce PETasas activas en frío, enzimas que descomponen los plásticos de polietileno tereftalato (PET) en entornos fríos, lo que ofrece soluciones sostenibles para la gestión de los residuos plásticos.
Aplicaciones de biocombustibles y energías renovables:
Los extremófilos contribuyen a la producción de energía sostenible al permitir la síntesis eficiente de biocombustibles y el procesamiento de biomasa en condiciones extremas.
- Producción de bioetanol: las bacterias termófilas como Clostridium thermocellum producen celulasas que descomponen la biomasa lignocelulósica en azúcares fermentables para la producción de bioetanol. Su actividad a altas temperaturas reduce los riesgos de contaminación y acelera la hidrólisis, lo que reduce los costes de producción.
- Biogás e hidrógeno: las arqueas metanogénicas, como Methanothermobacter thermautotrophicus, se desarrollan en digestores anaeróbicos de alta temperatura, convirtiendo los residuos orgánicos en metano para biogás. Las bacterias piezófilas de los entornos marinos profundos, comoShewanella benthica, se están investigando para la producción de biohidrógeno en condiciones de alta presión, lo que ofrece una alternativa de energía limpia.
- Biocombustibles de algas: las microalgas halófilas, como Dunaliella salina, acumulan lípidos en condiciones de alta salinidad, que se procesan para obtener biodiésel. Su resistencia a los entornos salinos permite su cultivo en tierras no aptas para la agricultura, lo que preserva los recursos de agua dulce.
Aplicaciones en el procesamiento de alimentos y bebidas:
Los extremófilos mejoran el procesamiento de alimentos al proporcionar enzimas que funcionan en las condiciones extremas de la producción industrial de alimentos.
- Procesamiento de lácteos y bebidas: las proteasas y lipasas psicrófilas se utilizan en la maduración del queso y la clarificación de zumos, funcionando a bajas temperaturas para preservar el sabor y la calidad nutricional. Por ejemplo, las enzimas Pseudoalteromonas mejoran la hidrólisis de las proteínas de la leche en el almacenamiento en frío.
- Procesamiento de almidón y azúcar: las amilasas termófilas de Bacillus licheniformis hidrolizan el almidón en procesos de alta temperatura para la producción de jarabe que se utiliza en bebidas y confitería. Estas enzimas garantizan altos rendimientos y reducen los tiempos de procesamiento.
- Fermentación: las enzimas halófilas de la especie Halobacterium facilitan las fermentaciones salinas, como en la producción de salsa de pescado y salsa de soja, mejorando los perfiles de sabor en condiciones de alta salinidad.
Aplicaciones agrícolas:
Los extremófilos contribuyen a la agricultura sostenible a través de biopesticidas, la remediación del suelo y la mejora del crecimiento de las plantas.
- Biopesticidas: los antifúngicos péptidos de halófilos protegen los cultivos de patógenos como el Fusarium y reducen el uso de pesticidas químicos. Estos péptidos rompen las membranas fúngicas, lo que ofrece un método específico.
- Remediación del suelo: las bacterias acidófilas como Acidithiobacillus rioensis movilizan los metales pesados en los suelos contaminados, restaurando las tierras agrícolas. Su metabolismo basado en el azufre desintoxica las zonas afectadas por la minería.
- Tolerancia al estrés de las plantas: los osmoprotectores halófilos, como la ectoína de Halomonas elongata, mejoran la resistencia de las plantas a la salinidad y la sequía, lo que aumenta el rendimiento de los cultivos en las regiones áridas. Los ensayos de campo realizados en 2025 mostraron un aumento de la productividad del trigo en suelos salinos tratados con ectoína.
Materiales y procesos industriales:
Los extremófilos se utilizan en industrias como la textil, la del cuero y la cosmética, donde sus robustas enzimas y compuestos destacan en condiciones de procesamiento adversas.
- Procesamiento textil: las proteasas alcalófilas de Bacillus alkalophilus eliminan las manchas proteicas y facilitan el teñido en condiciones alcalinas, mejorando la calidad de los textiles y reduciendo el consumo de agua.
- Curtido del cuero: las enzimas halófilas y alcalófilas depilan y desengrasan las pieles en procesos de curtido con alto contenido de sal o pH alto. También sustituyen a los productos químicos tóxicos.
- Cosméticos: la ectoína y el β-caroteno de halófilos como Dunaliella salina se utilizan en cremas hidratantes y protectores solares, protegiendo la piel del daño de los rayos UV y la deshidratación gracias a su estabilidad en formulaciones con alto contenido en sal.
Perspectivas de futuro para los extremófilos
A pesar de su potencial, los extremófilos se enfrentan a retos a la hora de ampliar su uso. El cultivo de organismos exigentes y el alto coste de la purificación de enzimas son dos obstáculos importantes, junto con la ampliación de la producción. La metagenómica y la biología sintética están abordando estas cuestiones al permitir la expresión de genes extremófilos en huéspedes manejables como Escherichia coli.
Los avances en el cribado de alto rendimiento y la bioprospección impulsada por la inteligencia artificial también están acelerando el descubrimiento de nuevas enzimas y compuestos extremófilos. La integración de las tecnologías derivadas de los extremófilos con la nanotecnología y la química verde podría mejorar aún más su eficiencia y aplicabilidad.
Para aprovechar al máximo los beneficios potenciales de los extremófilos, los investigadores deben centrarse en varias direcciones clave:
- Explorar extremos poco estudiados: la investigación de entornos extremos menos estudiados (p. ej., el subsuelo profundo, los desiertos hiperáridos y las zonas de alta radiación) puede revelar nuevos extremófilos con adaptaciones sin precedentes.
- Conocimientos mecánicos sobre las estrategias de supervivencia: deben emplearse enfoques genómicos, proteómicos y metabolómicos avanzados para descifrar los mecanismos moleculares que subyacen a la resiliencia de los extremófilos.
- Biología sintética e ingeniería enzimática: el aprovechamiento de las biomoléculas derivadas de extremófilos mediante la modificación genética y la evolución dirigida podría mejorar su aplicabilidad industrial.
- Astrobiología y misiones espaciales: los extremófilos deben estudiarse más a fondo como modelos de posible vida extraterrestre, especialmente en análogos de Marte y lunas heladas como Europa y Encélado.
- Colaboraciones interdisciplinares: la combinación de microbiología, bioinformática, ciencia de los materiales e ingeniería acelerará los descubrimientos y las aplicaciones.
A medida que avanza la tecnología, los extremófilos seguirán transformando nuestra comprensión de la adaptabilidad de la vida e inspirando soluciones para algunos de nuestros mayores retos.
Para obtener más información, vea nuestro artículo de revista, Extremophiles: Unlocking Bioactive Compounds and Biotechnological Innovation from Life at the Edge.