
O que são colas moleculares?
As colas moleculares são pequenas entidades químicas que usam uma estratégia inovadora conhecida como degradação de proteína alvo induzida por proximidade (TPD), na qual proteínas patogênicas de interesse (POIs) são ligadas a enzimas digestivas naturais e destruídas (Figura 1). Essa abordagem efetivamente “cola” ou liga os POIs às ubiquitina ligases E3 do sistema ubiquitina-proteassoma, que normalmente funciona como um sistema de processamento de lixo celular. Essa abordagem criou novas classes de agentes terapêuticos com modos inteiramente novos com atividade em potencial empolgante contra várias doenças graves, como câncer, doenças inflamatórias e imunes e infecções, muitas das quais são impulsionadas pela expressão aberrante de uma proteína patogênica. Existem mais de 600 ubiquitina ligases E3 codificadas no genoma humano e, até o momento, apenas algumas foram exploradas usando a abordagem TPD, portanto, há um potencial considerável para desenvolver muito mais.
Pergunte aos especialistas da Dana-Farber, ao CEO da Neomorph e ao CAS à medida que exploram novas tendências em colas moleculares, degradação de proteínas direcionadas e proximidade induzida em um webinar da ACS ao vivo em 5 de outubro de 2022 às 14h EDT. Cadastre-se aqui.
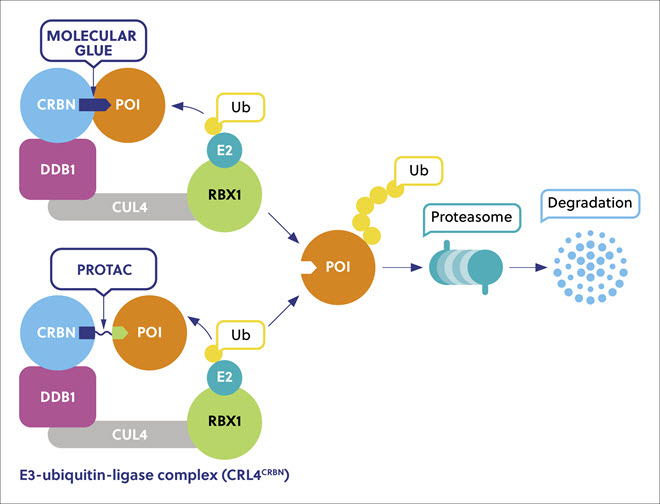
Os degradadores de proteínas são vantajosos porque atuam via ligação transitória em vez de ocupação competitiva e se dissociam após promover poliubiquitinação da POI. Portanto, um único degradador pode destruir muitas cópias de uma proteína patogênica, proporcionando alta eficiência contra proteínas anteriormente “invencíveis” em baixas doses. Os medicamentos inibidores de proteínas bloqueiam o sítio ativo de uma proteína patogênica, enquanto os degradadores removem todas as suas funções, proporcionando maior sensibilidade aos POIs e uma melhor chance de afetar as interações proteicas não enzimáticas.
O desenvolvimento de compostos de TPD que usam a degradação natural de proteínas pela ubiquitinação para fins terapêuticos avançou consideravelmente nas últimas duas décadas. A primeira patente de um degradador quimérico terapêutico para ligar uma POI à E3 ligase foi registrada pela Proteinix em 1999. Isto foi seguido por um estudo de prova de conceito no qual uma proteína associada ao câncer foi degradada com sucesso por uma quimera de direcionamento de proteólise (PROTAC). As primeiros PROTACs eram estruturas moleculares grandes; o primeiro relato de um degradador de receptor de andrógeno (AR) de pequena molécula usando nutlin-3 para o recrutamento de MDM2 foi publicado em 2008. A descoberta subsequente de miméticos de moléculas pequenas do peptídeo HIF1α acelerou o projeto racional de PROTACs moleculares pequenos. Até agora, poucos TPDs induzidos por proximidade chegaram a testes clínicos, mas dois PROTACs (ARV-110 e ARV-471), que têm como alvo o receptor de andrógeno e estrogênio avançaram para ensaios de Fase II, e muitos outros estão agora em desenvolvimento.
As colas moleculares e os PROTACs têm propriedades diferentes. As colas moleculares são pequenas moléculas que interagem com uma variedade de proteínas alvo de difícil previsão, exibindo atividades biológicas distintas ao induzir e potencializar a interação de duas proteínas que de outra forma não apresentam afinidade intrínseca entre si. Os PROTACs são moléculas bivalentes que consistem em duas porções, uma que se liga à POI e a outra à E3 ligase, unidas por um ligante. As colas moleculares são menores e espera-se que tenham melhores propriedades farmacológicas, maior permeabilidade da membrana, melhor absorção celular e melhor penetração da barreira hematoencefálica que os PROTACs. A identificação de cola molecular baseou-se principalmente na serendipidade, mas estão surgindo abordagens racionais de design cujo alvo são proteínas invencíveis. Após a descoberta inicial, o caminho prossegue para a definição, otimização e validação do esqueleto (Tabela 1).
Tabela 1. Caminho da descoberta de degradadores de cola molecular e design de medicamentos guiado por estrutura.
| Descoberta inicial | Definição de esqueleto |
| Otimização | Validação |
Têm sido descobertas colas moleculares de vários tipos; a mais conhecida é provavelmente a talidomida e seus análogos, e a lenalidomida e a pomalidomida, que têm como alvo a E3 ligase cereblon. Foram identificados vários outros mecanismos de ação das colas moleculares, incluindo degradação de proteínas mediada por autofagia, estabilização de subcomplexos de MEK, inibição de mutantes de KRAS, estabilização de polimerização de α-tubulina e degradação de proteína 12 de ligação a FK506 (FKBP12).
O cenário da pesquisa de cola molecular – conforme encontrado no CAS Content Collection™
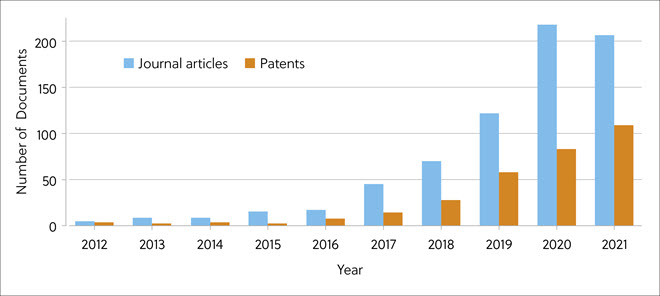
O CAS Content Collection™ é a maior coleção de conhecimento científico publicado com curadoria humana, adequada para análise quantitativa de publicações científicas globais em relação a variáveis como tempo, área de pesquisa, formulação, aplicação e composição química. Para avaliar os avanços recentes na pesquisa de colas moleculares, particularmente em química medicinal e descoberta de medicamentos, um novo relatório do CAS Insights analisou os dados de publicações relevantes de 2012 a 2021 do CAS Content Collection. Nesse período, houve um crescimento enorme de artigos publicados e patentes relacionadas a degradadores de proteínas (Figura 2).
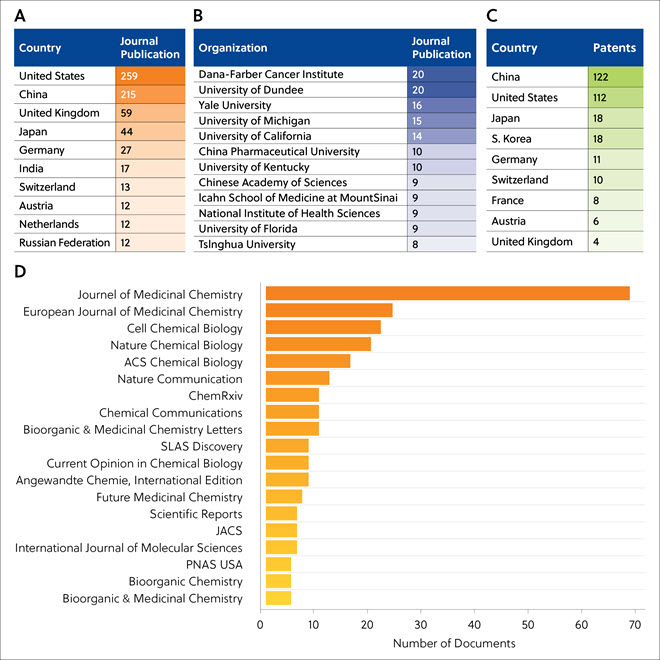
Publicações em periódicos científicos sobre degradadores de proteínas foram principalmente dos Estados Unidos, China, Reino Unido, Japão, Alemanha e outros (Tabela 2A). O Dana-Farber Cancer Institute e a University of Dundee publicaram o maior número de artigos científicos relacionados ao TPD (Tabela 2B). O maior número de registros de patentes relacionados a degradadores de proteínas foi da China e dos Estados Unidos (Tabela 2C). Os periódicos que frequentemente publicam artigos relacionados ao TPD estão apresentados na Tabela 2D, destacando a importância do TPD na pesquisa médica; o Journal of Medicinal Chemistry e o European Journal of Medicinal Chemistry têm o maior número de artigos relacionados ao TPD.
Tabela 2. Principais países (A), organizações (B) e periódicos científicos (D) que publicam artigos relacionados ao TPD e os principais países que registram patentes relacionadas ao TPD (C).
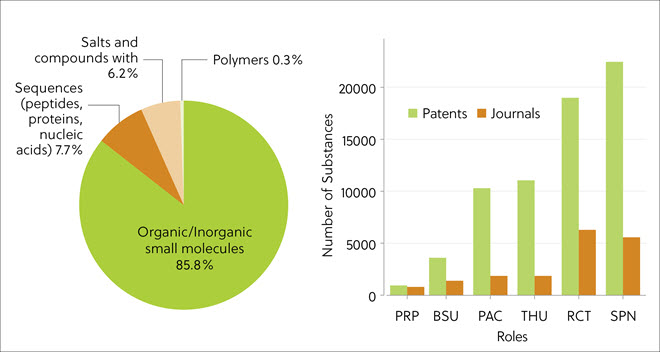
O tipo de TPD mais frequente nas publicações foram moléculas pequenas (85,8%), seguidas por biossequências (7,7%), incluindo peptídeos, proteínas, ácidos nucléicos e sais (Figura 3, painel esquerdo). Isso indica uma mudança nas primeiras moléculas quiméricas direcionadas a proteínas, que eram baseadas em peptídeos. Os degradadores de proteínas são sintetizados por meio de reações químicas em várias etapas, o que explica a predominância das funções relacionadas à síntese de SPN (preparo sintético) e RCT (reagente) nos resultados da análise da literatura (Figura 3, painel direito). Números significativamente maiores de compostos indexados no CAS Content Collection originados de patentes.
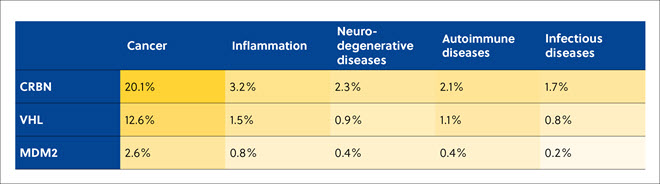
Na análise da literatura, CRBN, VHL e MDM2 foram os tipos mais populares de E3 ligases sendo usados para recrutar TPDs para induzir ubiquitinação e subsequente degradação proteassomal de proteínas alvo em câncer, inflamação, doenças neurodegenerativas, autoimunes e infecciosas (Tabela 3).
Tabela 3. Correlação do número de publicações relacionadas a degradadores de proteínas no CAS Content Collection para as três ligases E3 mais utilizadas com as doenças alvo. As porcentagens são do total de publicações relacionadas aos degradadores de proteínas.
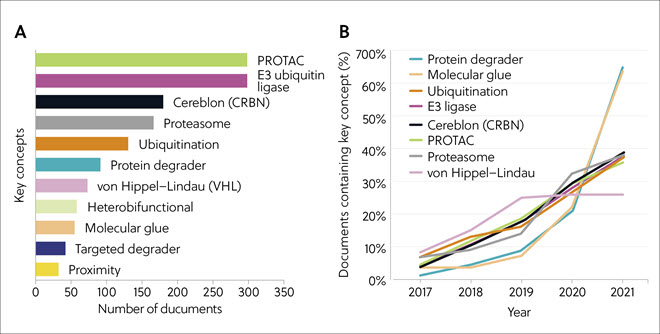
O maior número de publicações durante 2017 a 2021 foi em PROTACs e E3 ubiquitina ligases, seguido por cereblon, proteassoma e ubiquitinação (Figura 4A). Documentos sobre colas moleculares e degradadores de proteínas foram menos numerosos, mas mostraram crescimento e interesse explosivos a partir de 2019. Outros conceitos, incluindo ubiquitinação, E3 ligase, cereblon, PROTAC e proteassoma, também mostraram um forte crescimento contínuo ao longo de 2017 a 2021 (Figura 4B).
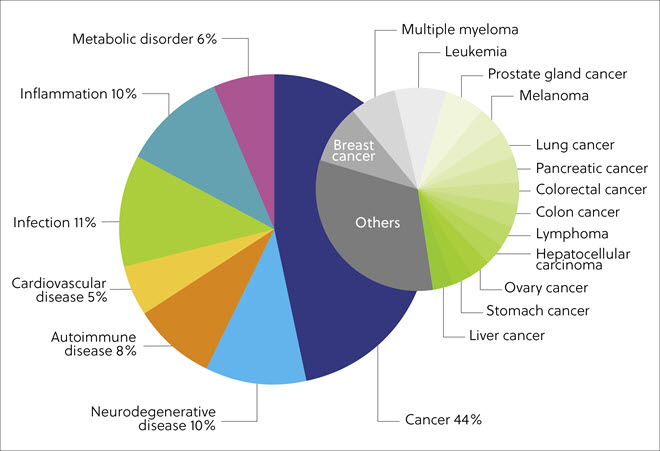
Uma análise das doenças visadas pelos degradadores de proteínas encontradas no CAS Content Collection mostrou que a maior parte (44%) das publicações estava associada a cânceres variados (por exemplo, câncer de mama e próstata, mieloma múltiplo e leucemia). Além disso, doenças infecciosas (11%), neurodegenerativas (10%), inflamatórias (10%), autoimunes (8%), metabólicas (6%) e cardiovasculares (5%) também foram altamente representadas (Figura 5).
Colas moleculares – descobertas e em desenvolvimento
O número de tipos e estruturas de cola molecular conhecidos já é considerável e está crescendo. As colas moleculares mais amplamente investigadas são pequenas moléculas que ligam a E3 ligase CRBN e as aril sulfonamidas que se ligam ao DCAF15. Outras colas moleculares que induzem a degradação de proteínas por meio de vários mecanismos de ação não E3 ligase incluem degradação de proteínas mediada por autofagia, estabilização de interação proteína-proteína, inibição de mutantes KRAS, estabilização de polimerização de microtúbulos e inibição do alvo de rapamicina em mamíferos (mTOR). Além disso, existem compostos naturais, como a ciclosporina A e a sanglifehrin A, que funcionam como colas moleculares. Esses desenvolvimentos indicam uma importante ampliação das abordagens de cola molecular e uma gama de ação potencialmente mais diversificada.
Embora muitas colas moleculares potenciais tenham sido identificadas, até agora, muito poucas foram avaliadas quanto à eficácia terapêutica na clínica e menos ainda receberam aprovação regulatória. Várias empresas em todo o mundo têm uma série de produtos baseados em colas moleculares em desenvolvimento pré-clínico para uso em uma variedade de cânceres e doenças neurodegenerativas e inflamatórias. Dentre essas empresas estão:
- Ranok (Hangzhou, China) – candidato a medicamento RNK05047 entra em ensaios clínicos no primeiro semestre de 2022 para o tratamento de tumores sólidos e linfomas
- Monte Rosa Therapeutics (Boston, MA, EUA) – iniciou atividades de habilitação de IND para seu programa principal visando GSPT1 para tratamento oncológico dentre outros. Pedido do IND a ser submetido ao FDA em meados de 2022. Fase de descoberta de medicamentos para outras colas moleculares direcionadas a tumores sólidos/líquidos, doenças autoimunes e doenças do sangue
- Plexium/Parceria com a Amgen (San Diego, CA, EUA) – fase principal de otimização de uma cola molecular de cereblon visando IKZF2 para o tratamento de doenças imunológicas e câncer
- Frontier Medicines/Parceria com a AbbVie (San Francisco, CA, EUA) – fase de descoberta de medicamentos para desenvolver medicamentos covalentes de moléculas pequenas contra alvos intratáveis de imunologia e oncologia
- f5 Therapeutics (San Diego, CA, EUA) – candidatos moleculares para vários tipos de câncer diferentes, esclerose múltipla, artrite reumatoide, esteato-hepatite não alcoólica e fibrose hepática
- Ambagon Therapeutics/Parceria com BMS e Merck (San Carlos, CA, EUA) – fase de descoberta de medicamentos com cinco compostos de tratamento oncológico de descoberta inicial
- Amphista Therapeutics (Londres, Reino Unido) – tratamentos de câncer com modo de ação não E3 ligase
- Proxygen/Parceria com a Boehringer Ingelheim (Viena, Áustria) – fase de descoberta de medicamentos para o tratamento de cânceres de pulmão e gastrointestinais
- Neomorph/Parceria com o Dana Farber Cancer Institute (San Diego, CA, EUA) – fase de descoberta de medicamentos para avançar seu pipeline de desenvolvimento de cola molecular contra alvos não passíveis de tratamento
- Seed Therapeutics/Parceria com a Lilly (Nova York, NY, EUA) – fase de descoberta de medicamentos com candidatos a pipeline de cola molecular para tratar câncer, doenças neurodegenerativas e doenças infecciosas. Seu composto principal tem como alvo o oncogene KRAS
- Pin Therapeutics (Seul, Coreia do Sul) – fase de descoberta de medicamentos
- Venquis Therapeutics (San Diego, CA, EUA) – fase de descoberta de medicamentos para câncer e doenças degenerativas
- IRB Barcelona/Parceria com Almirall (Barcelona, Espanha) – fase de descoberta de medicamentos para tratamento de doenças de pele
- Shanghai Dage Biomedical Technology Co., Ltd. (Xangai, China) – pipeline de colas moleculares que aborda alvos para câncer, doenças inflamatórias e doenças metabólicas. Principal fase de otimização para candidatos a cola molecular oncológica
- Triana Biomedicines (Waltham, MA, EUA) – lançada recentemente em abril de 2022 para estabelecer um pipeline de cola molecular racionalmente projetado para tratar doenças inadequadamente abordadas
- Evotec/Parceria com a BMS (Hamburgo, Alemanha) – fase de descoberta de medicamentos para desenvolver um pipeline de degradadores de cola molecular
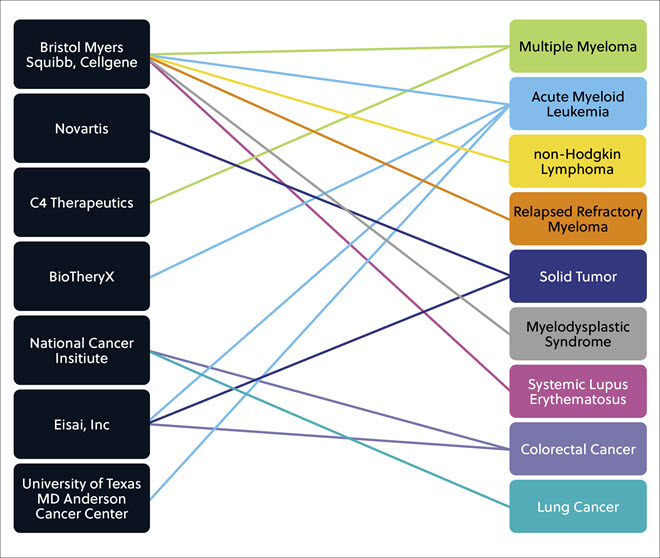
Várias outras empresas/instituições têm uma gama promissora de compostos de cola molecular em vários estágios de desenvolvimento clínico que visam tratar diversos tumores sólidos e líquidos, juntamente com condições inflamatórias e doenças autoimunes, como lúpus eritematoso sistêmico (Figura 6).
Perspectivas para colas moleculares como agentes terapêuticos – elas podem atender a necessidades médicas não atendidas?
Induzir a proximidade de proteínas alvo a enzimas degradativas que de outra forma não entrariam em contato próximo usando colas moleculares é uma abordagem empolgante com potencial para criar um grande número de agentes terapêuticos altamente novos contra uma ampla gama de doenças graves. O desafio agora é desenvolver a abordagem TPD, identificando compostos candidatos com atividades úteis e progredir para produtos clinicamente úteis.
O mecanismo de ação das colas moleculares e seus princípios de design são insuficientemente compreendidos e são necessárias mais pesquisas para criar novos compostos e explorá-los integralmente. Os métodos de descoberta de novas colas moleculares basearam-se em grande parte na triagem intensiva de alto rendimento, seguida de validação sistemática. Há uma necessidade de estratégias de projeto eficientes e racionais para aumentar o desenvolvimento de compostos novos e mais eficientes e avaliar sua atividade em várias indicações. Ferramentas computacionais para modelar e prever a ligação de colas moleculares e avanços na cristalização para melhorar a compreensão da ancoragem de proteínas são necessários para a transição do acaso ao design racional.
As pesquisas do CAS Content Collection mostram que a indução da degradação de proteínas usando colas moleculares está atraindo um interesse generalizado e um crescimento explosivo tanto em artigos científicos quanto em patentes. Embora os compostos direcionados à E3 ligase continuem a predominar, há também um forte interesse em compostos não E3 ligase e alguns degradadores de colas moleculares naturais, o que indica uma grande diversidade de agentes potenciais. A perspectiva para colas moleculares, portanto, parece ser promissora com o provável aparecimento de muitos outros agentes terapêuticos usando essa abordagem em um futuro próximo, que têm o intrigante potencial de atender a uma gama diversificada de necessidades não atendidas.
Baixe o relatório do CAS Insights para saber mais sobre o crescimento explosivo dos degradadores de colas moleculares, suas aplicações terapêuticas e como o interesse da pesquisa evoluiu na última década.
