El 24 de febrero, CAS, en colaboración con ACS, organizó un webinario con expertos en vacunas. Durante esa sesión, de una hora de duración, recibimos más de 120 preguntas de los participantes y, por desgracia, no pudimos responder a muchas de ellas en el tiempo disponible. A raíz de la reciente aprobación en Estados Unidos de la vacuna para la COVID-19 de Johnson & Johnson, muchas preguntas se centraron en la seguridad, la efectividad y la composición de las diferentes vacunas disponibles. Ante el gran interés suscitado, mi compañero Yu Shan Tsai y yo responderemos aquí a las preguntas más repetidas relacionadas con la vacuna para la COVID-19 y presentaremos un resumen de las iniciativas de investigación en curso para ayudar a la población a tomar decisiones fundamentadas.
¿En qué se diferencia la vacuna de Johnson & Johnson de las de Pfizer/BioNTech y Moderna?
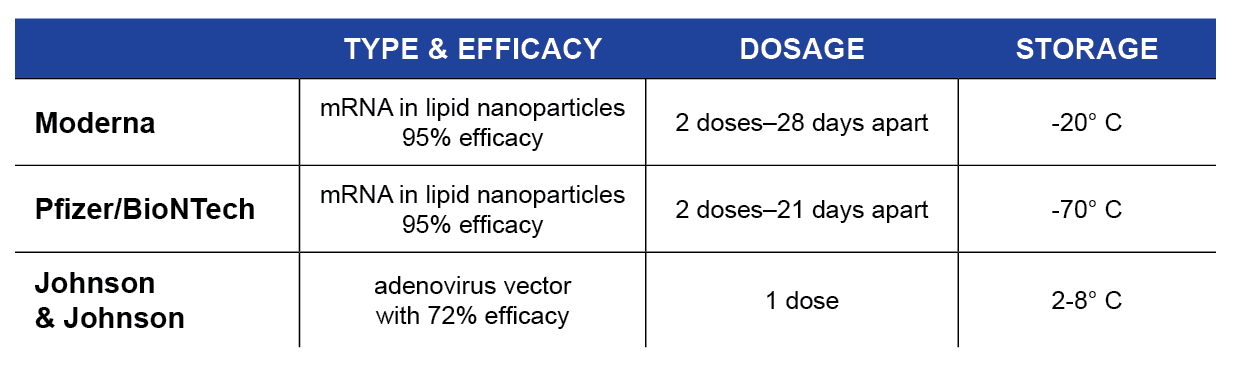
A diferencia de las vacunas de ARNm de Moderna y Pfizer/BioNTech, la vacuna de la COVID-19 de Johnson & Johnson es una vacuna de vector vírico de una única dosis que además se puede conservar a temperaturas de refrigeración normales. La plataforma de administración de vectores víricos no replicantes consiste en el uso de un virus inofensivo (adenovirus tipo 26) para transportar hasta las células del organismo un código genético con indicaciones para producir las proteínas de la espícula antigénicas (Janssen Biotech, 2021).
Si bien ambos tipos de vacunas transmiten a las células instrucciones para que comiencen a reconocer la proteína de la espícula del SARS-CoV-2 y preparen al ejército inmunitario para combatir el virus real, las vacunas de ARNm exigen la administración de dos dosis. En cambio, la vacuna de Johnson & Johnson consta de una sola dosis, lo que simplificaría y aceleraría considerablemente el proceso de vacunación. Otra ventaja de la vacuna de Johnson & Johnson es que se puede conservar a temperaturas de refrigeración normales, lo que sin duda facilitaría el acceso a esta vacuna en zonas rurales o menos desarrolladas en comparación con las vacunas de ARNm.
La vacuna de Johnson & Johnson presentó una efectividad del 72 % en términos de prevención de la enfermedad grave de COVID-19, que es inferior al 95 % notificado para las vacunas de Pfizer/BioNTech y Moderna. Sin embargo, la vacuna de Johnson & Johnson es la única probada contra la variante sudafricana y esto puede explicar en parte esta menor eficacia (Janssen Biotech, 2021). En esta entrada del blog hablaremos también de las distintas variantes.
¿Qué vacuna debo ponerme?
La respuesta directa a la pregunta de qué vacuna debería ponerse es "SÍ". Cuando empezamos a analizar con una mirada crítica los beneficios y riesgos de cada vacuna es fácil que el objetivo primordial se diluya entre tanta información. Lo cierto es que tenemos tres vacunas viables y seguras que son muy efectivas (casi en un 100 %) en términos de prevención de enfermedad grave y mortalidad asociadas a la COVID-19; la consideración de las vidas humanas es mucho más importante que las dispares tasas de eficacia determinadas según distintos parámetros en condiciones de laboratorio. El Dr. Anthony Fauci, asesor médico jefe de la Casa Blanca (Estados Unidos), recomienda la inmunización con la vacuna que esté disponible en el momento en el que a cada persona le llegue el turno de vacunación (Newburger, 2021).
Variantes del Reino Unido, Sudáfrica y Brasil: ¿qué significa esto?
Una variante vírica se define por la acumulación de mutaciones en el código genético del virus que empieza a divergir de la composición genética original identificada. Aunque las vacunas existentes han demostrado cierto grado de protección frente a la variante del Reino Unido (véase más adelante), lo realmente positivo es que la modificación de estas vacunas con las nuevas secuencias genéticas será probablemente mucho más rápida que el desarrollo de la vacuna original. Si bien las vacunas aprobadas en la actualidad son fundamentales para proteger a la población de las cepas más frecuentes, lamentablemente el distanciamiento social y el uso de la mascarilla seguirán siendo medidas básicas para reducir al mínimo posible la propagación de las nuevas variantes hasta la aprobación de las vacunas de refuerzo.
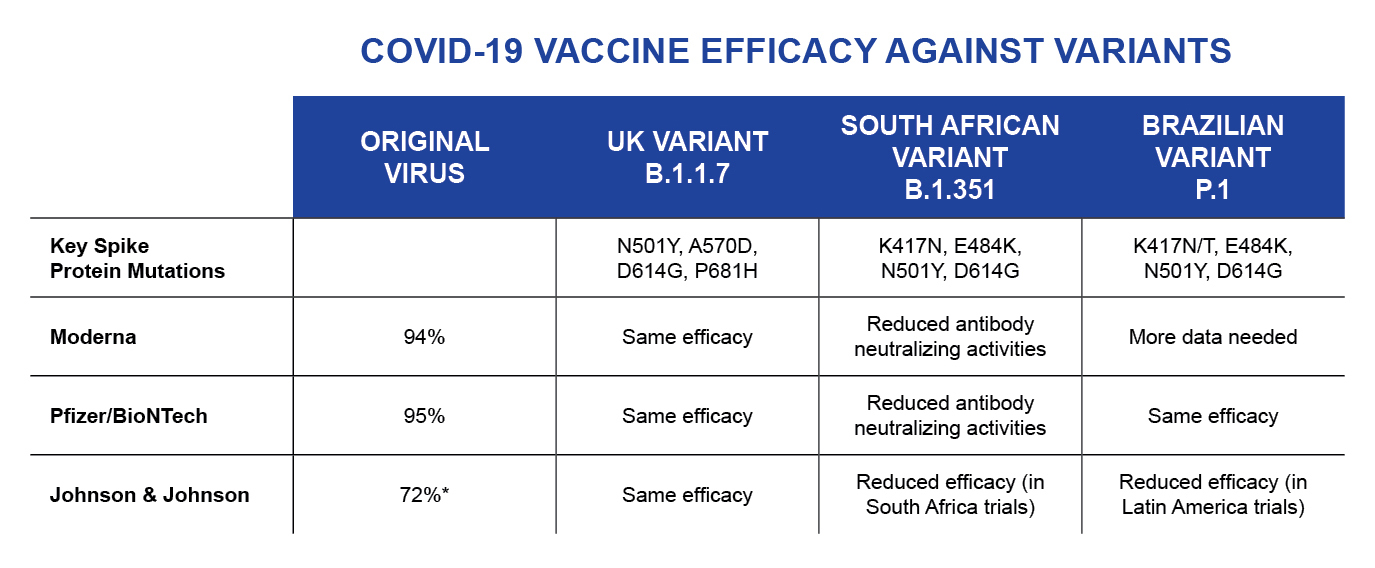
Las dianas de las vacunas actuales son las secuencias de la proteína de la espícula ancladas en la superficie del coronavirus SARS-CoV-2. Cuando esta proteína de la espícula experimenta una mutación notable, surge una nueva variante del virus, que puede propagarse con rapidez. Las mutaciones aminoacídicas específicas de cada variante se enumeran en la tabla que figura a continuación.
La variante británica (B.1.1.7), que surgió en el sureste de Inglaterra en septiembre de 2020, se propagó con rapidez a más de 50 países. Es probable que una propagación tan rápida se debiera a la posible mayor virulencia y transmisibilidad de esta variante. Afortunadamente, las vacunas Moderna y Pfizer/BioNTech reconocían esta variante, por lo que las personas que recibieron estas vacunas están tan protegidas frente a la enfermedad grave causada por la variante del Reino Unido como frente a la causada por el virus original del SRAS-CoV-2 (Wang et al., 2021).
La variante sudafricana (B.1.351) se identificó a finales de 2020 y se caracteriza por una mutación de la proteína de la espícula que afecta al dominio de unión al receptor. A diferencia de la variante británica, las respuestas inmunitarias provocadas por las vacunas actualmente disponibles no neutralizaban suficientemente esta variante. Estos datos corroboran la necesidad de desarrollar vacunas de refuerzo que contemplen estas mutaciones y la naturaleza rápidamente cambiante del código genético del virus en la población vacunada, así como de realizar ajustes en las secuencias genéticas de las vacunas previstas para la inoculación inicial (Tegally et al., 2020).
La variante brasileña (P.1) se está extendiendo rápidamente en este país y presenta mutaciones similares a las de la variante sudafricana. Esto supone que esta variante también escapa a los efectos protectores de las vacunas de ARNm actuales (Tegally et al., 2020).
Si bien estas son las variantes identificadas más destacadas, cabe mencionar que siguen surgiendo nuevas variantes (por ejemplo, en California y Nueva York). La mutación es una estrategia de supervivencia de los patógenos víricos; es necesario vigilar en todo momento estas mutaciones y ajustar las vacunas como corresponda a fin de proporcionar vacunas efectivas. Aquí se puede encontrar información adicional sobre la efectividad de las vacunas actuales frente a estas variantes.
¿Cuál es el impacto de la COVID-19 en los niños?
Los datos limitados relativos a la hospitalización y la mortalidad infantiles relacionadas con la COVID-19 transmitieron la percepción inicial de que la pandemia de coronavirus no afectaba a los niños. La realidad, sin embargo, es que la tasa de hospitalización infantil es considerable. Hasta octubre de 2020, 127 niños murieron debido a la enfermedad causada por el coronavirus (Anderson et al., 2020). Otro hecho que contribuye a esta idea errónea inicial es que los niños pueden presentar un cuadro sintomático diferente. Entre marzo y julio de 2020, se publicaron varios informes en los que se señalaba que la COVID-19 en los niños se puede presentar en forma de síndrome inflamatorio multisistémico (Anderson et al., 2020). Los niños no son adultos en miniatura; por mencionar algunas diferencias, no tienen la robustez inmunitaria, la superficie corporal, la masa muscular y la distribución de la grasa de los adultos. Por tanto, es necesario realizar más investigaciones y ensayos de vacunas centrados en los niños para confirmar la seguridad y la eficacia protectora de estas vacunas en la población pediátrica.
¿Deben vacunarse las mujeres embarazadas?
Es sabido que las mujeres embarazadas presentan un mayor riesgo de padecer enfermedad grave relacionada con la COVID-19 y, por extensión, de que se produzcan resultados adversos del embarazo. Un nuevo estudio ha revelado que las vacunas de la COVID-19 de Pfizer/BioNTech y Moderna son eficaces tanto en mujeres embarazadas como en madres lactantes, que pueden transmitir los anticuerpos protectores a los recién nacidos. En este estudio, realizado en varios centros de Massachusetts (Massachusetts General Hospital, Brigham and Women's Hospital y Ragon Institute of MGH, MIT and Harvard), se inscribieron 131 mujeres en el periodo de diciembre de 2020 a marzo de 2021.
Además, el 18 de febrero de 2021, Pfizer anunció la inscripción de 4000 mujeres embarazadas sanas en un ensayo clínico de fase 2/3 de su vacuna, actualmente en curso. La recomendación vigente del Comité Asesor sobre Prácticas de Inmunización (Advisory Committee on Immunization Practices) para las mujeres embarazadas o lactantes es que pueden decidir vacunarse si así se lo recomiendan sus médicos; sin embargo, por el momento, los datos disponibles sobre los posibles efectos en el feto y la producción y secreción de leche materna son insuficientes para fundamentar ninguna decisión.
¿Y en cuanto a la investigación de la vacunación de personas inmunodeprimidas?
Las personas inmunodeprimidas merecen siempre una consideración especial en lo que respecta a la vacunación. Dado que las vacunas de ARNm desarrolladas por Pfizer/BioNTech y Moderna fueron las primeras de su tipo, todavía no se había establecido un precedente relativo a la respuesta inmunitaria de este mecanismo de administración de fármacos en personas con disfunción inmunitaria. Si bien no se excluyó a las personas con VIH de los ensayos clínicos de las vacunas de ARNm, los datos son limitados. Los participantes en los ensayos clínicos con trastornos autoinmunes e inflamatorios no presentaron contraindicaciones para la vacunación en comparación con la población sana (Advisory Committee on Immunization Practices, 2020). No se notificaron casos de síndrome de Guillain-Barré después de la inmunización con las vacunas de Moderna y Pfizer/BioNTech; el síndrome de Guillain-Barré es un trastorno poco frecuente en el que el sistema inmunitario ataca por error a las neuronas (nervios). Las personas con síndrome de Guillain-Barré podían participar en el ensayo. En los ensayos de las vacunas de ARNm también participaron personas con parálisis de Bell, y las vacunas demostraron ser seguras también para estas personas. En la infografía que figura a continuación se resumen las recomendaciones del Comité Asesor sobre Prácticas de Inmunización para estas poblaciones de mayor riesgo.

Referencias:
Advisory Committee on Immunization Practices. (2020). COVID-19 ACIP Vaccine Recommendations. Obtenido en https://www.cdc.gov/vaccines/hcp/acip-recs/vacc-specific/covid-19.html.
Anderson, E. J., Campbell, J. D., et al. (2020). Warp Speed for COVID-19 Vaccines: Why are Children Stuck in Neutral? CID 2020. https://doi.org/10.1093/cid/ciaa1425
Gray, K. J., et al (2021). COVID-19 vaccine response in pregnant and lactating women: a cohort study. American Journal of Obstetrics and Gynecology. https://www.ajog.org/article/S0002-9378(21)00187-3/fulltext
Jackson, L. A., Anderson, E. J., Rouphael, N. G., Roberts, P. C., Makhene, M., Coler, R. N., McCullough, M. P., Chappell, J. D., Denison, M. R., Stevens, L. J., Pruijssers, A. J., McDermott, A., Flach, B., Doria-Rose, N. A., Corbett, K. S., Morabito, K. M., O'Dell, S., Schmidt, S. D., Swanson, P. A., Padilla, M., Mascola, J. R., Neuzil, K. M., Bennett, H., Sun, W., Peters, E., Makowski, M., Albert, J., Cross, K., Buchanan, W., Pikaart-Tautges, R., Ledgerwood, J. E., Graham, B.S., Beigel, J. H. (2020). An mRNA Vaccine against SARS-CoV-2 - Preliminary Report. New England Journal of Medicine 12 de noviembre de 2020 383(20): 1920-1931 https://doi.org/10.1056/NEJMoa2022483
Janssen Biotech, Inc. (2021). Janssen Ad26.COV2.S Vaccine for the Prevention of COVID-19. FDA Briefing Document. Obtenido en https://www.fda.gov/media/146217/download.
Newburger, E. (28 de febrero de 2021). Fauci says all three Covid vaccines highly effective, urges people to take shot most available. CNBC News. Obtenido de https://www.cnbc.com/2021/02/28/fauci-all-three-covid-vaccines-highly-effective-urges-people-to-take-available-shot.html.
Tegally, H., Wilkinson, E., Giovanetti, M., Iranzadeh, A., Fonseca, V., et al. (2020). Emergence and rapid spread of a new severe acute respiratory syndrome-related coronavirus 2 (SARS-CoV-2) lineage with multiple spike mutations in South Africa. medRxiv, 2020.12.21.20248640.
Walsh, E. E., Frenck, R. W., Falsey, A. R., Kitchin, N., Absalon, J., Gurtman, A., Lockhart, S., Neuzil, K., Mulligan, M. J., Bailey, R., Swanson, K. A., Li, P., Koury, K., Kalina, W., Cooper, D., Fontes-Garfias, C., Shi, P. Y., Türeci, Ö., Tompkins, K. R., Lyke, K. E., Raabe, V., Dormitzer, P. R., Jansen, K. U., Şahin, U., Gruber, W. C. (2020). Safety and Immunogenicity of Two RNA-Based Covid-19 Vaccine Candidates. New England Journal of Medicine 17 de diciembre de 2020 383(25):2439-2450. doi: 10.1056/NEJMoa2027906.
Wang, P., Nair, M. S., Liu, L., Iketani, S., Luo, Y., et al. (2021). Antibody Resistance of SARS-CoV-2 Variants B.1.351 and B.1.1.7. Nature. https://doi.org/10.1038/s41586-021-03398-2

