バイオ医薬品業界のイノベーションは、ポジティブな公衆衛生と商業的成果を綿密に監視するための推進力となります。 成功の尺度としてイノベーションを追跡することに高い関心があるにもかかわらず、それを効果的に測定する方法についての合意はほとんどありません。 世の中でよくあるように、製薬業界のイノベーションの評価は、それを評価する視点が元になっています。 アナリストが薬剤イノベーションに対し引用している主なメトリックは、新たに承認された薬剤の数、または開発パイプラインのさまざまな段階に入る薬剤候補の数という場合もあります。 これらのカウント数を基本とする測定値は、例えばファースト・イン・クラス(画期的医薬品)や画期的治療法の指定などのカウント数以外の結果ベースの指標に加えて有益であり、重要な進歩を浮き彫りにするものです。 また、追跡と比較が実に簡単にできるという利点もあります。 しかし、化学者の視点からの、新しい分子エンティティ(NME)固有の革新性を捉えることはできません。
最近ACS Medicinal Chemistry Lettersに掲載された新しい論文では、同僚のアラン・リプカス氏と私で、初期段階の合成化学の観点からこの問題を取り上げています。 その結果として、NMEの構造分析に基づき初期段階の薬剤イノベーションを測定および説明するための新しいアプローチを提唱します。 このアプローチは、既存の結果ベースの測定と併せて検討すると、製薬イノベーションの展望をより完全に把握するのに役立つ、というものです。
製薬業界全体でイノベーションは増加しているか、あるいは減少しているか? 方法論詳細と過去20年間の分析結果全容について、記事全文をご覧ください。
薬剤イノベーションの構造的枠組みを定義
構造的新規性に基づいた薬剤イノベーションの特徴づけに対する私たちの新しいアプローチは、分子フレームワークの概念に依存しています。 化学構造のフレームワークは、すべてのリングシステムとそれらを接続したチェーンフラグメントから成る下部構造として定義されます。 分子フレームワーク情報(スキャフォールドと形状レベル)と薬剤が承認された年を考慮した分類システムを使い、各NMEは、以下に示すように「パイオニア」「セトラー」「コロニスト」の3つのクラスのいずれかに割り当てられます。
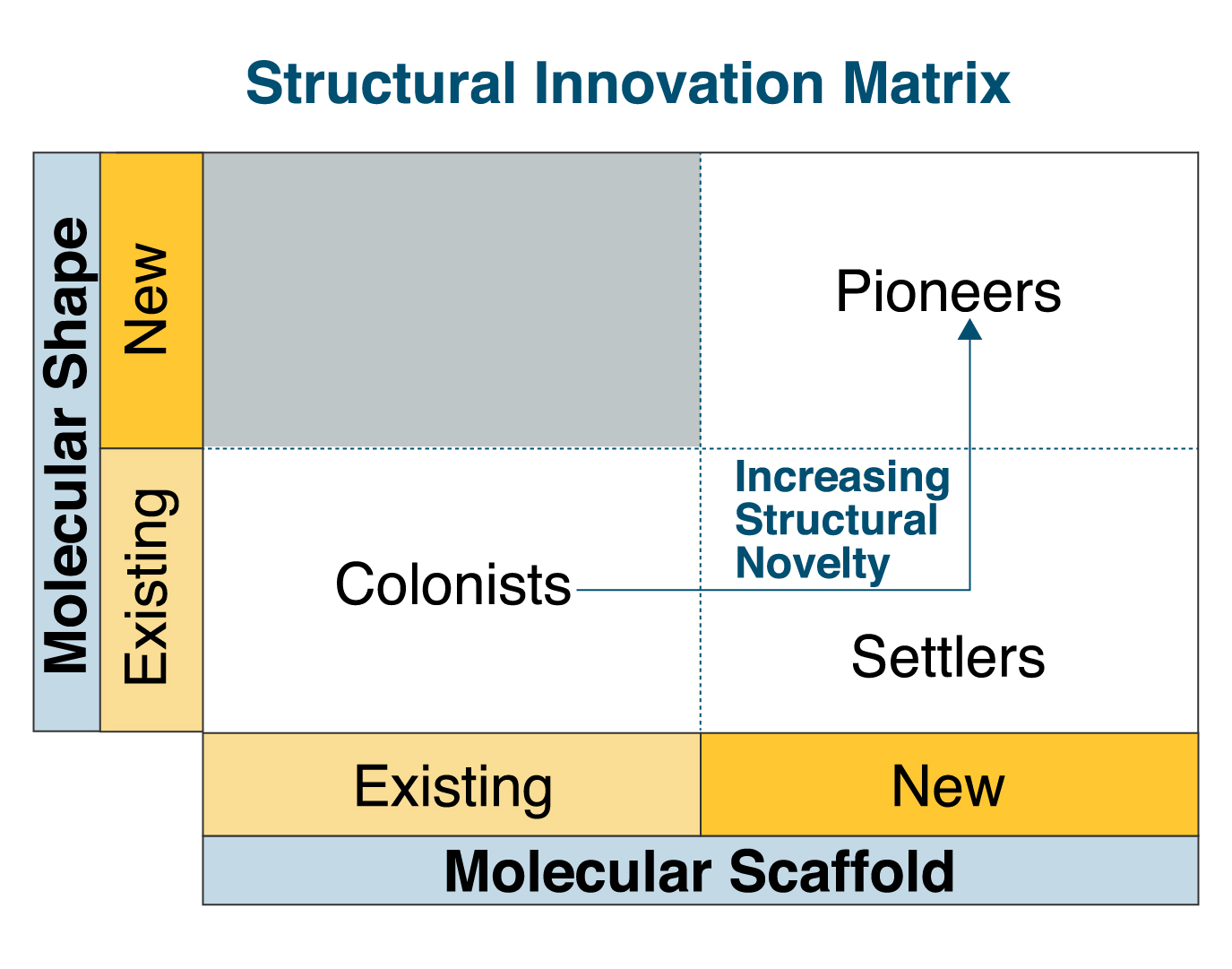
漸進的進歩を辿ったもの、あるいは完全に新構造のいずれにおいても、新薬についてFDAの承認を受けることは薬剤開発チームにとって大きな成果であり、また主要な成功の尺度です。 したがって、このフレームワークにおける3つのクラスはすべて、ある程度のイノベーションを表すものですす。 ただし、この調査における比較のため、「パイオニア」を最も革新的であるものと見なしました。
構造イノベーションを成果につなげる
イノベーションそのものを喜ぶことは良いですが、戦略的観点から有用であるとするためには、薬剤イノベーションの測定では、組織の目的に沿った前向きな結果と何らかの相関関係が示されなければなりません。 重要な医療ニーズに対応し、研究投資に大きな利益をもたらす画期的新薬を市場に投入することは医薬品イノベーションの頂点であると、多くの人に考えられています。 その尺度でいうと、CASの分析結果によると、現在の画期的新薬のほぼ65%が少なくとも1つのパイオニア成分を含んでいるとのことです。 パイオニアはまた、発売から5年以内に他のクラスの2倍以上の確率で画期的新薬(年間収益10億ドル以上)を実現させていることがわかりました。 さらに言うと、公衆衛生に対する薬の潜在的影響の代わりとして、米国FDAの画期的治療法の指定をものさしに使うと、私たちの研究結果では、パイオニアがこれらの有望な新しい治療法の源である可能性が大幅に(2.5倍以上)高いことを示しています。
画期的新薬のImbruvica(ibrutinib)は、構造イノベーションの強力な影響を実証しています。 Celera Genomicsが発見し、PharmacyclicsとJanssenが共同開発および商品化した、ファースト・イン・クラスのBrutonのチロシンキナーゼ(BTK)阻害剤は、2013年に米国FDAに承認されました。 2015年にAbbVieが約210億ドルでPharmacyclicsを買収したのは、同薬の治療効果や商業的可能性が主な理由でした。 構造的に新しいこのパイオニアは、これまでにさまざまな適応症に対して合計11のFDA承認を取得しています。米国FDAから3つ以上の画期的な治療指定を受けたのはわずか2つの小分子治療で、そのうちの1つにあたります。 Imbruvica(ibrutinib)は、2019年にすべての適応症で72億4000万ドルの総売上高を創出しました。
構造イノベーションの源を追跡
公衆衛生と商業上の利益を考えると、近年、パイオニアの数とパイオニアを発掘する組織の数が大幅に増えているのは当然のことといえるでしょう。 どちらのケースも過去10年間でほぼ倍増し、2000年から2009年の間には84のパイオニアが61の組織から発生し、2010年から2019年の間には109の組織によって164のパイオニアが生まれました。
医薬品革新の主な供給源を評価するために、パイオニアを2つのグループに分けました。AbbVie、AstraZeneca、Bayer、Bristol-Myers Squibb、Eli Lilly、GlaxoSmithKline、Johnson&Johnson、Merck&Co.、AbbVie、AstraZeneca、Bayer、Bristol-Myers Squibb、Eli Lilly、GlaxoSmithKline、Johnson&Johnson、Merck&Co.、Novartis、Pfizer、Roche、Sanofiなど、医薬品関連の収益に基づいて「ビッグファーマ」と定義する企業を供給源とするグループと、 および他の組織(残りのエコシステムまたはROE)が起源のもの。 初期段階の薬物発見のイノベーションに一貫して、NMEを開発した企業や薬剤の承認を確保した企業ではなく、NMEを発見した研究開発組織にクレジットを与えました。
この分析によると、以下のグラフが示すように、ビッグファーマから発生したパイオニアの総数を2000〜2009年と2010〜2019年で比較すると、ほぼ50%増加しており、ビッグファーマの大多数がパイオニア数の増加を見たことがわかります。 最も注目に値するのはBayer社で、2000〜2009年の間にはパイオニアの承認はありませんでしたが、2010〜2019年には4件が承認されました。 AbbVie社とBristol-Myers Squibb社もまた、この間に4件の増加が見られます。
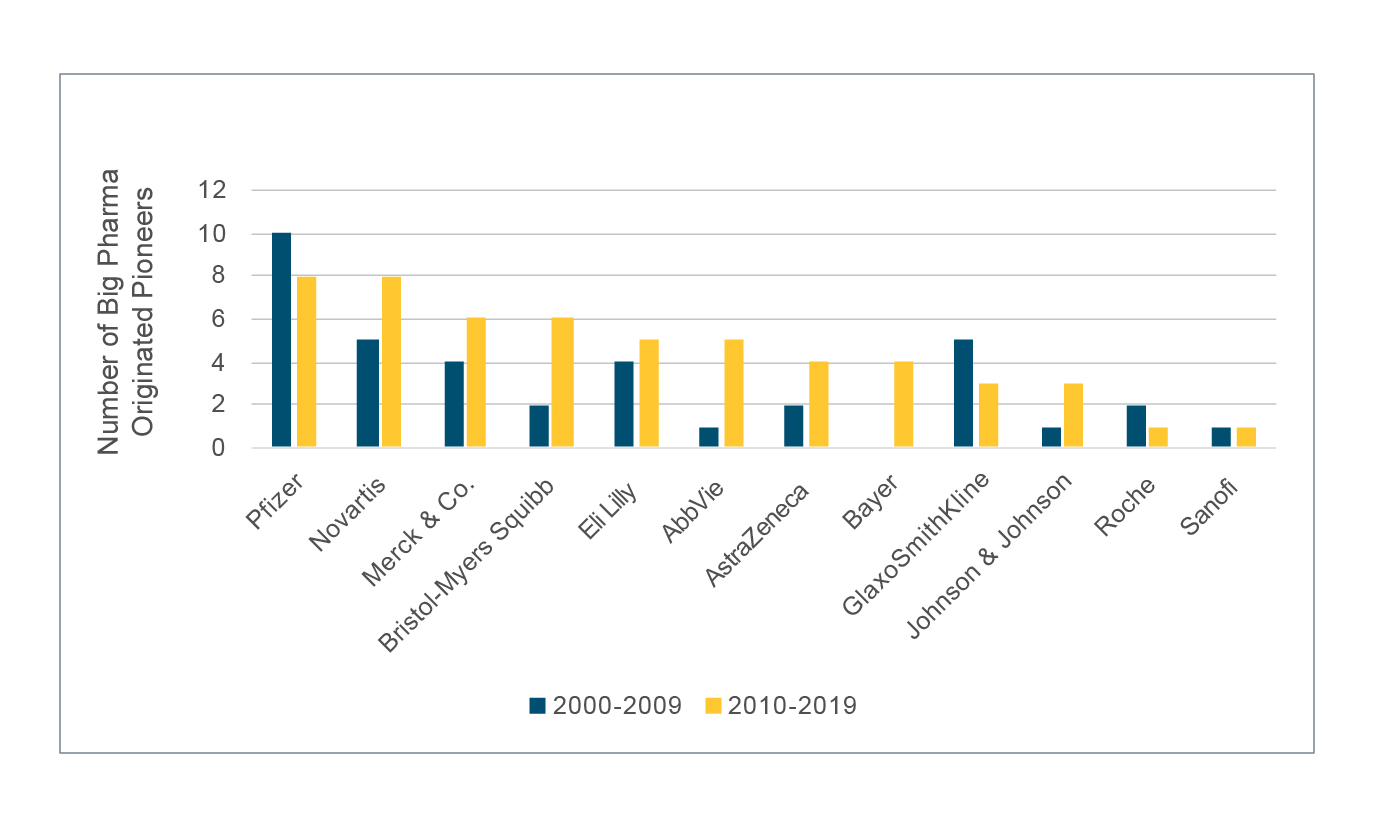
ROEから発生したパイオニアの数を2000〜2009年と2010〜2019年で比較すると、130%以上の増加が見られ、パイオニアを発見したROE企業の数はこの間で2倍になっています。 最も注目に値するのはGilead社、エーザイ薬品、シオノギ製薬, Vertex社で、2000〜2009年の間にはパイオニアの承認はありませんでしたが、2010〜2019年には4件以上が承認されました。
ビッグファーマから発生したパイオニアの数が全体的に増加しているにもかかわらず、この分析では、下のグラフに示すように、ビッグファーマとROEの間の構造的イノベーションのギャップが拡大していることもわかりました。 このシフトは、薬剤発見のプロセスにおけるインシリコ手法の重要性の高まりや、高品質の化合物ライブラリーの可用性の拡大など、参入の障壁を減らす要因によって起こっているのかもしれません。
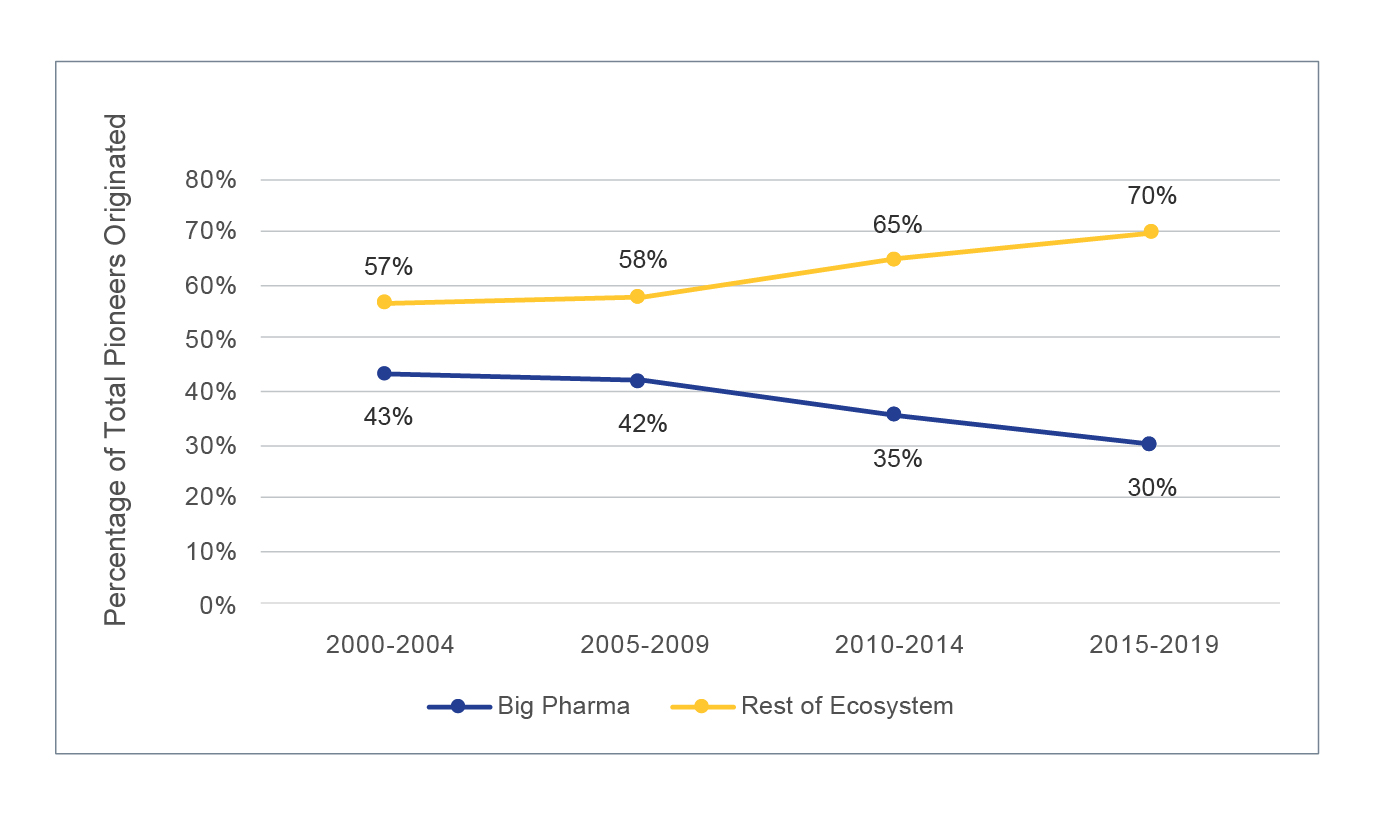
イノベーションの機会を最大化するための新しいアプローチの採用
これらの調査結果によると、イノベーションに関しては、以前ほどに企業の規模は有利でなくなったことを示唆しているようで、私の予測では今後も規模の有利性はさらに縮小していくものと思われます。 企業の研究開発能力の物理的規模は、イノベーションの量においては主な支配者でしたが、ブルートフォースの発見がインシリコ増強アプローチに取って代わられるにつれ、デジタルアセットと機能が競争市場を平準化してきているようです。
機械学習と高度な分析を通じて大量のデータセットから得られた洞察により初期段階における薬剤発見が加速し続けるにつれ、成功の可能性が最も高く見込まれる薬剤候補の優先順位付けを支援することで、競争においてはデータを最も効果的に活用し�より優れた薬剤をより短い時間で市場に投入する企業が優位な位置に立っています。 またこの効率性により、化学空間の新しい領域の探索をより完全なものとし、効果的な治療法を探す上で幅広い薬剤候補を検討することで、イノベーションを強化する機会が高まります。 最終的な病気の治療法がパイオニア、コロニスト、セトラーのいずれであるかはほとんど重要ではありませんが、薬剤候補の多様なポートフォリオを意図的に構築することは、経時的に見て平均して高い成功率につながる可能性があります。
この機会を利用するために、研究チームは、多様なイノベーションパイプラインを達成するにあたり、より野心的な形態の構造イノベーションと自然な人的リスクの災難を回避するという、根深い傾向を克服するための支援が必要になる場合があります。 あらゆる分野でリピートできるイノベーションを実現するには、構造化されたアプローチが必要であることが何度も実証されています。 この構造イノベーションのフレームワークにより、チームは、マクロとミクロのレベルで候補ポートフォリオを評価する機会を得ます。 マクロレベルの点から、各分野でどれだけ追求し、各タイプの構造イノベーションにどれだけの投資を行なっていますか。 ミクロレベルの点から、更に詳しい調査のために幅広いヒットを打ち出すにあたり、合成物ライブラリとトレーニングデータセットは十分に多様なものとなっていますか? これらの質問への回答として特定された機会を追求し、新しいテクノロジーがもたらす効率向上を取り入れることで、利益の増加ばかりか患者の転帰の改善も期待できます。
構造的な観点からのイノベーション機会の評価では、御社の研究開発の取り組みで利益が出そうですか?また、より革新的になるにはどのデータが貢献しそうですか? カスタム分析による独自の見識につきましては、CASサービスチーム までご連絡ください。

